Содержание
- 2. Цель урока: Повторить и закрепить знания учащихся о свойствах кислотных оксидов и кислот. Рассмотреть свойства соединения
- 3. Получение оксидов 1. Горение веществ (Окисление кислородом) а) простых веществ Mg +O2=2MgO S+O2=SO2 б) сложных веществ
- 4. 1)Сероводород горит на воздухе голубым пламенем при этом образуется сернистый газ или оксид серы(IV) 2H2S-2 +
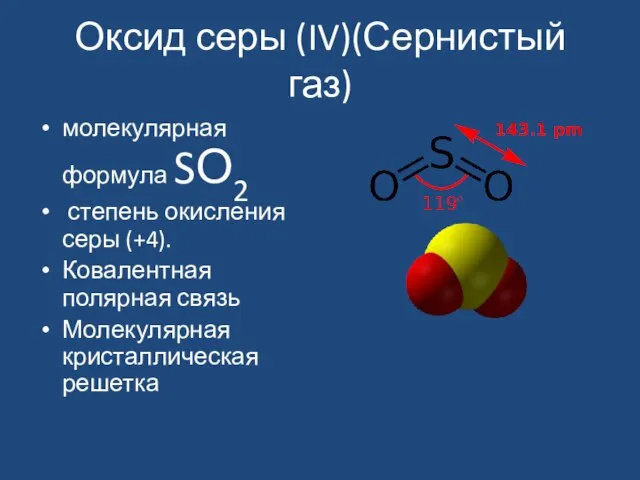
- 5. Оксид серы (IV)(Сернистый газ) молекулярная формула SО2 степень окисления серы (+4). Ковалентная полярная связь Молекулярная кристаллическая
- 6. Электронный баланс 1)S-2 -6е→ S+4 Восстановитель O2+4е → 2O -2 Окислитель 2) S0 -4е→ S+4 Восстановитель
- 7. Определение плотности по воздуху. Д воздух -? М(Воздух)= 29 г/моль М(H2S)=64г/моль Д воздух = 64:29=2,21 Д
- 8. Получение сернистого газа в промышленности. сжигание серы или обжиг сульфидов, в основном — пирита: 4FeS2+ 11O2
- 9. Получение оксида серы (IV) в лабораторных условиях воздействием сильных кислот на сульфиты и гидросульфиты. Образующаяся сернистая
- 10. Физические свойства. Оксид серы (IV), или сернистый газ, при нормальных условиях представляет собой бесцветный газ с
- 11. Нахождение в природе
- 12. Химические свойства кислотных оксидов ХИМИЧЕСКИЕ СВОЙСТВА КИСЛОТНЫХ ОКСИДОВ 1. Кислотный оксид +Вода= Кислота (р. соединения) СO2
- 13. Химические свойства оксида серы (IV) 1. Кислотный оксид +Вода= Кислота SO2 + H2O = H2SO3 2.
- 14. Химические свойства кислот 1. Изменяют окраску индикатора. 2.Реагируют с металлами в ряду активности до H2 (искл.
- 15. Уравнение диссоциации сернистой кислоты. H2SО3 → H+ + HSО3 - HSО3 - ↔ H+ + SО3
- 16. Качественная реакция на сульфиты. Взаимодействие соли с сильной кислотой, при этом выделяется газ с резким запахом
- 17. Окислительные свойства оксида серы (IV). 2H2S-2 + S +4O2 → 2H2O + 3S 0 S+4 +4е→
- 18. Восстановительные свойства оксида серы (IV) 2SO2+ O2 = 2SO2 SO2 + Br2 + 2H2O = H2
- 19. Применение оксида серы (IV). Большая часть оксида серы (IV) используется для производства серной кислоты. Используется также
- 20. Физиологическое действие на организм. SO2 очень токсичен. Симптомы при отравлении сернистым газом — насморк, кашель, охриплость,
- 21. Воздействие на атмосферу. Из-за образования в больших количествах в качестве отходов диоксид серы является одним из
- 23. Скачать презентацию



















 Объекты земельных отношений (ст. 6 ЗКРФ)
Объекты земельных отношений (ст. 6 ЗКРФ) Неизвестная Испания
Неизвестная Испания Лекция Тема: «ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ГОСУДАРСТВЕННОЙ СЛУЖБЫ».
Лекция Тема: «ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ГОСУДАРСТВЕННОЙ СЛУЖБЫ». Word Groups and Phraseological Units
Word Groups and Phraseological Units ОБУЧЕНИЕ ОСНОВАМ НАНОТЕХНОЛОГИЙ в условиях сельского лицея
ОБУЧЕНИЕ ОСНОВАМ НАНОТЕХНОЛОГИЙ в условиях сельского лицея Presentation Title Here Logo
Presentation Title Here Logo  Можно ли сделать звук видимым?
Можно ли сделать звук видимым? Проектирование системы теплоснабжения жилого района от ЦТП в г. Караганда
Проектирование системы теплоснабжения жилого района от ЦТП в г. Караганда Азбука питания
Азбука питания В поисках ценностей Детские программы, организованные при участии детей. Опыт работы на Открытом книжном фестивале и книжно
В поисках ценностей Детские программы, организованные при участии детей. Опыт работы на Открытом книжном фестивале и книжно Переход ОУ на свободное программное обеспечение
Переход ОУ на свободное программное обеспечение Сравнительный анализ героев сказки А.Н Толстого
Сравнительный анализ героев сказки А.Н Толстого 10 класс
10 класс Деды Морозы в разных странах
Деды Морозы в разных странах ЧЕЛОВЕК в мировой художественной культуре
ЧЕЛОВЕК в мировой художественной культуре Неорганические вяжущие вещества
Неорганические вяжущие вещества Электричество по воздуху
Электричество по воздуху Уважаемый посетитель сайта!
Уважаемый посетитель сайта! Свободная дислокация. Наглядное представление рекламного щита
Свободная дислокация. Наглядное представление рекламного щита Разнообразные факты о квадрате
Разнообразные факты о квадрате Философия, ее предмет, функции и структура Л1
Философия, ее предмет, функции и структура Л1 Презентация на тему Принтеры
Презентация на тему Принтеры Использование элементов ландшафтного дизайна в благоустройстве территории пришкольного участка
Использование элементов ландшафтного дизайна в благоустройстве территории пришкольного участка Презентация на тему Употребление числительных в речи
Презентация на тему Употребление числительных в речи  Имя существительное как часть речи 4 класс
Имя существительное как часть речи 4 класс История физической культуры
История физической культуры Презентация на тему Королевство Дания
Презентация на тему Королевство Дания  Новый год шагает по планете
Новый год шагает по планете