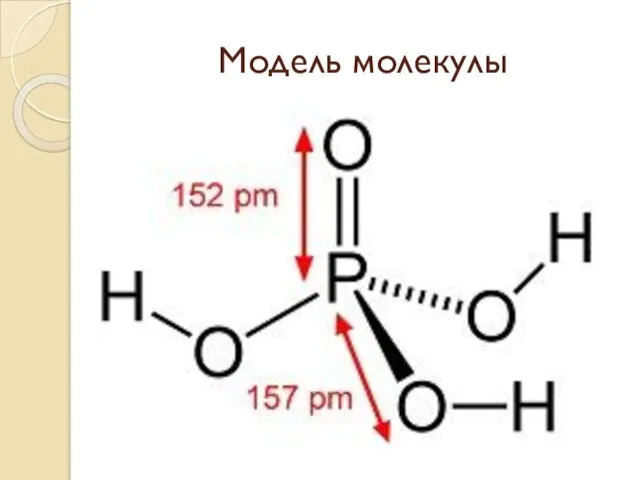
Слайд 2Состав и строение молекулы
Ее химическая формула – H3PO4, обозначение в качестве пищевой

добавки – Е338. Ортофосфорная кислота представляет собой бесцветные гигроскопичные кристаллы, хорошо растворимые в воде
(ортофосфорной кислотой называют ее 85%-ный раствор).
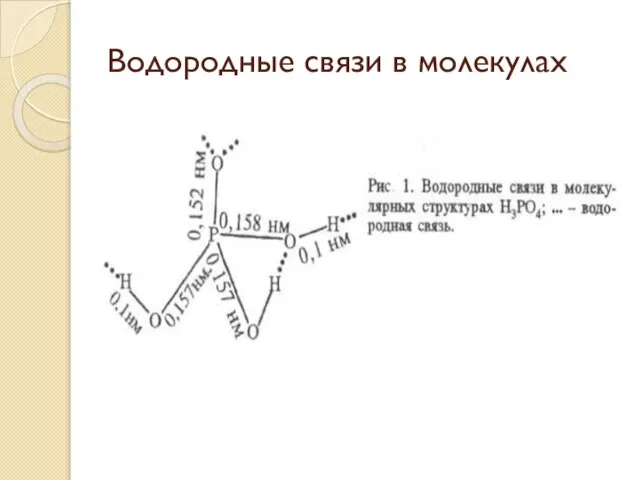
Слайд 4Водородные связи в молекулах
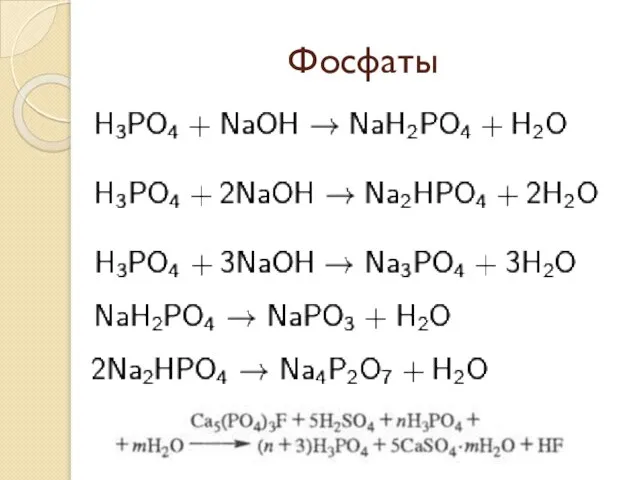
Слайд 5Получение
Фосфорную кислоту получают из фосфата:
Можно получить гидролизом пентахлорида фосфора:
Или взаимодействием с водой оксида фосфора(V), полученного сжиганием фосфора в кислороде:

Слайд 6Свойства
H3PO4 — трехосновная кислота средней силы. При взаимодействии с очень сильной кислотой, например,

с хлорной HClO4, фосфорная кислота проявляет признаки амфотерности — образуются соли фосфорила, например [Р(ОН)4]ClO4.
Отличительной реакцией ортофосфорной кислоты от других фосфорных кислот является реакция с нитратом серебра — образуется жёлтый осадок:
Слайд 7Свойства (качественная реакция)
Качественной реакцией на ион РО43− является образование ярко-жёлтого осадка молибденофосфата аммония:






 Европейский день соседей
Европейский день соседей Present simple (простое настоящее время)
Present simple (простое настоящее время) Мода-2014
Мода-2014 Программирование
Программирование  Роль филологических дисциплин в формировании стратегий смыслового чтения и работы с текстом в контексте ФГОС
Роль филологических дисциплин в формировании стратегий смыслового чтения и работы с текстом в контексте ФГОС Искитимский центр профессионального обучения
Искитимский центр профессионального обучения «ОСОБЕННОСТИ СЕМЕЙНОГО ВОСПИТАНИЯ»
«ОСОБЕННОСТИ СЕМЕЙНОГО ВОСПИТАНИЯ» Карта для первокурсника. Защита проекта
Карта для первокурсника. Защита проекта Как определить окончание по вопросу?
Как определить окончание по вопросу? Приоритетные направления деятельности ФАС России. Национальные ориентиры и международные проекты
Приоритетные направления деятельности ФАС России. Национальные ориентиры и международные проекты Программа «Участник молодежного научно-инновационного конкурса» («У.М.Н.И.К.») в рамках Фонда содействия развитию малых форм предп
Программа «Участник молодежного научно-инновационного конкурса» («У.М.Н.И.К.») в рамках Фонда содействия развитию малых форм предп Презентация на тему Жизнь и творчество Николая Носова
Презентация на тему Жизнь и творчество Николая Носова Жизнь на 162%
Жизнь на 162% Современные ленточнопильные станки
Современные ленточнопильные станки I know Delphi
I know Delphi Стиль модерн
Стиль модерн Подготовка отчёта об исследовании
Подготовка отчёта об исследовании Мера ответственности родителей за воспитание ребенка
Мера ответственности родителей за воспитание ребенка Научно-методический семинар по подготовке к итоговому сочинению 2016-2017. Победа и поражение
Научно-методический семинар по подготовке к итоговому сочинению 2016-2017. Победа и поражение Презентация на тему Снежный барс 2 класс
Презентация на тему Снежный барс 2 класс Детский лагерь отдыха Ирандык
Детский лагерь отдыха Ирандык Реклама McDonald’s
Реклама McDonald’s Потребность. Блага. Услуги. Ресурсы
Потребность. Блага. Услуги. Ресурсы Красота в искусстве и в жизни
Красота в искусстве и в жизни Бадминтон
Бадминтон Концепция Mazda Accessories
Концепция Mazda Accessories Что такое кроссфит
Что такое кроссфит Карточка. Радиоактивность
Карточка. Радиоактивность