Содержание
- 2. 5.1. ЗАКОН СОХРАНЕНИЯ И ПРЕВРАЩЕНИЯ ЭНЕРГИИ Первый закон термодинамики является частным случаем всеобщего закона сохранения и
- 3. К концу XVIII в. процесс превращения теплоты в работу был осуществлен, но без всяких теоретических расчетов
- 4. А — постоянная величина, называемая тепловым эквивалентом работы. Тепловой эквивалент единицы работы — величина размерная и
- 5. В 1843 г. англичанин Джоуль, а в 1844 г. русский академик Ленц установили соотношение между электрической
- 6. Таким образом, закон сохранения и превращения энергии, открытый М. В. Ломоносовым, но не получивший широкого развития
- 7. 5.2. ВНУТРЕННЯЯ ЭНЕРГИЯ Под внутренней энергией газа понимается вся энергия, заключенная в теле или системе тел:
- 8. Полную внутреннюю энергию тела принято обозначать U (Дж), а удельную внутреннюю энергию — u(Дж/кг) (5.2)
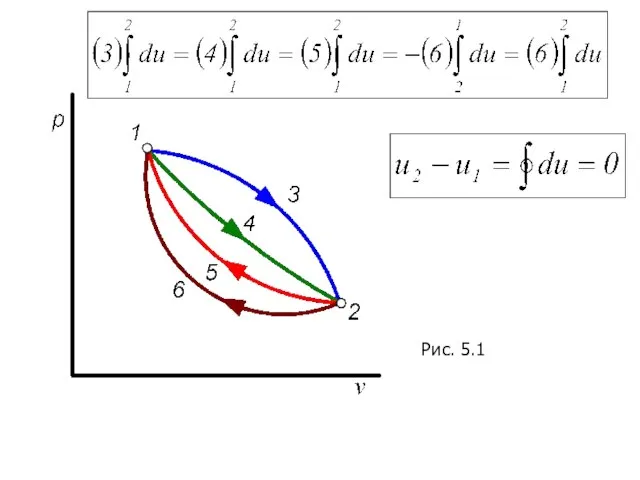
- 9. Рис. 5.1
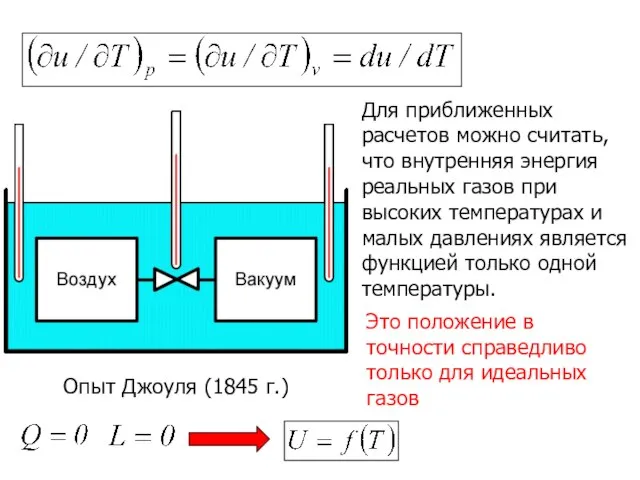
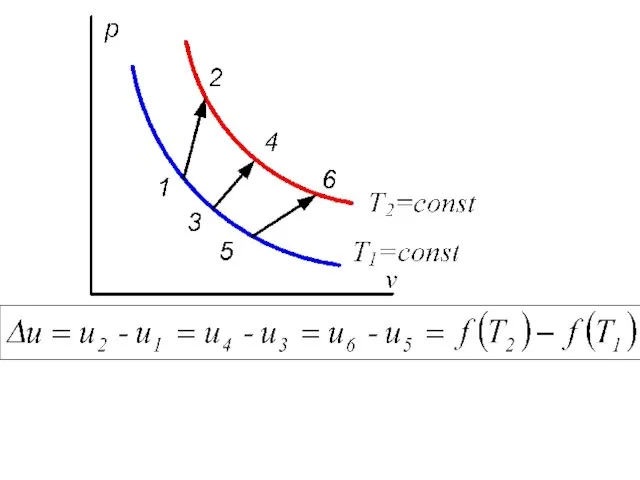
- 10. (5.3) Удельная внутренняя энергия идеального газа, в котором отсутствуют силы взаимодействия между молекулами, не зависит от
- 11. Для приближенных расчетов можно считать, что внутренняя энергия реальных газов при высоких температурах и малых давлениях
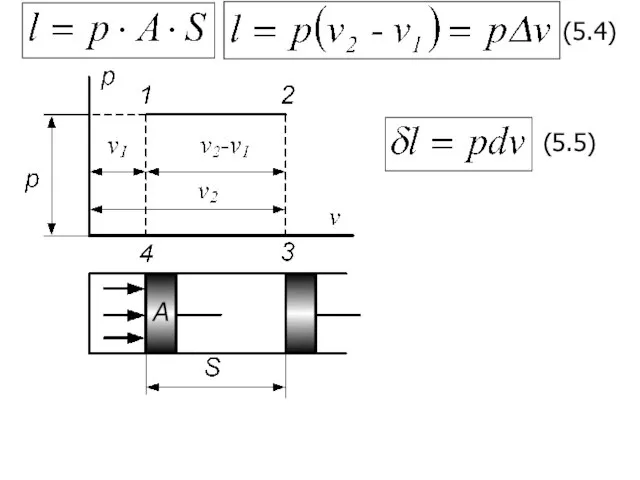
- 13. 5.3. АНАЛИТИЧЕСКОЕ ВЫРАЖЕНИЕ РАБОТЫ ПРОЦЕССА Передачу энергии от одного тела к другому, связанную с изменением объема
- 14. (5.4) (5.5)
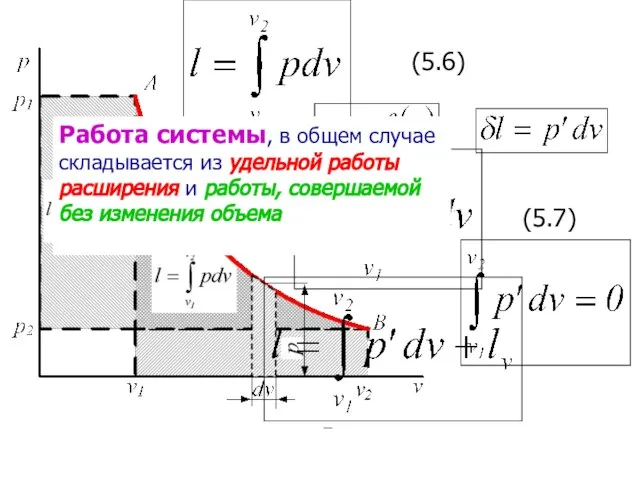
- 15. (5.6) (5.7) Работа системы, в общем случае складывается из удельной работы расширения и работы, совершаемой без
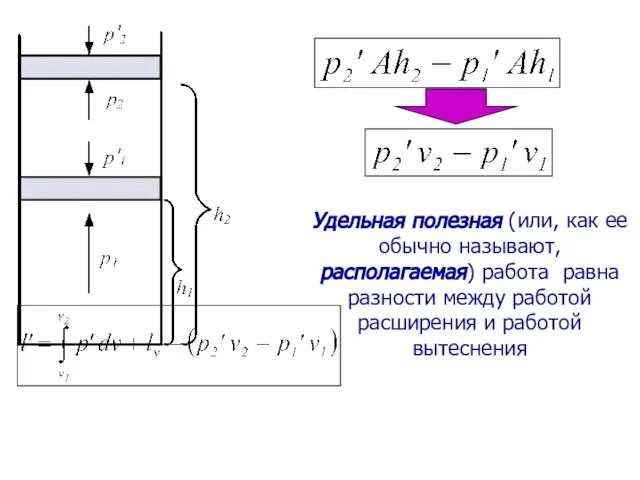
- 16. Удельная полезная (или, как ее обычно называют, располагаемая) работа равна разности между работой расширения и работой
- 17. Если v2 > v1 — газ расширяется, тогда Δv > 0 и dv > 0 —
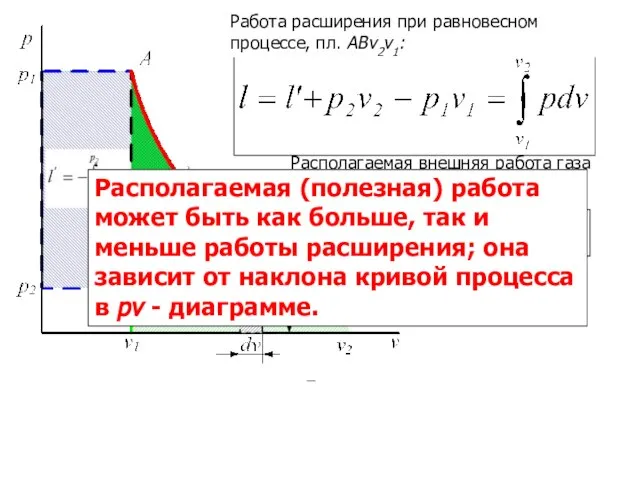
- 18. Работа расширения при равновесном процессе, пл. АВv2v1: Располагаемая внешняя работа газа (полезная), пл. АВр2p1: Располагаемая (полезная)
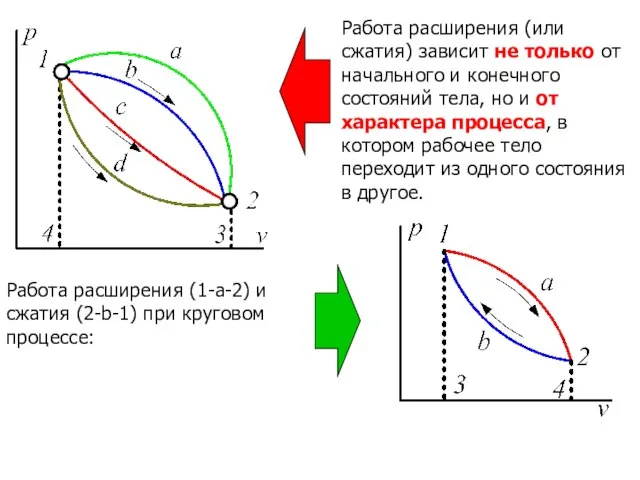
- 19. Работа расширения (или сжатия) зависит не только от начального и конечного состояний тела, но и от
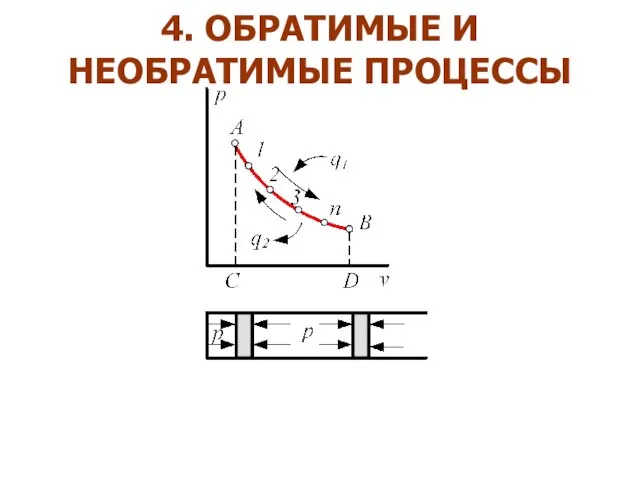
- 20. 4. ОБРАТИМЫЕ И НЕОБРАТИМЫЕ ПРОЦЕССЫ
- 21. Процессы, протекающие в прямом и обратном направлениях без остаточных изменений, как в самом рабочем теле, так
- 22. Необратимыми термодинамическими процессами являются: процессы расширения и сжатия с конечными скоростями всякий процесс, сопровождающийся трением процессы,
- 23. При расширении газа всегда - При сжатии газа - Обратимый процесс представляет собой некоторый предельный случай
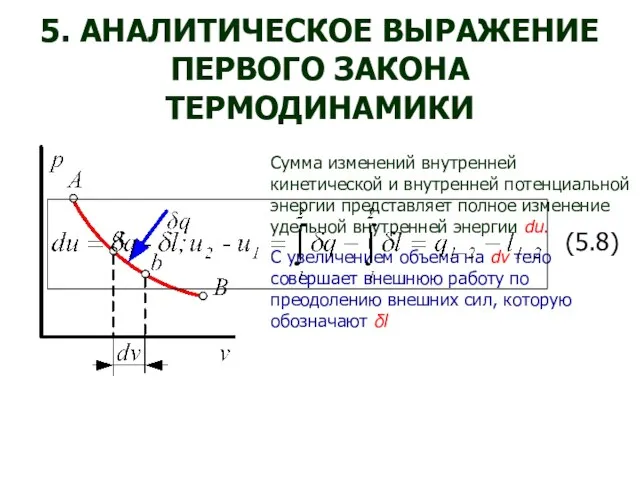
- 24. 5. АНАЛИТИЧЕСКОЕ ВЫРАЖЕНИЕ ПЕРВОГО ЗАКОНА ТЕРМОДИНАМИКИ Сумма изменений внутренней кинетической и внутренней потенциальной энергии представляет полное
- 25. изменение удельной внутренней энергии термодинамической системы равно алгебраической сумме полученной системой энергии в форме удельной теплоты
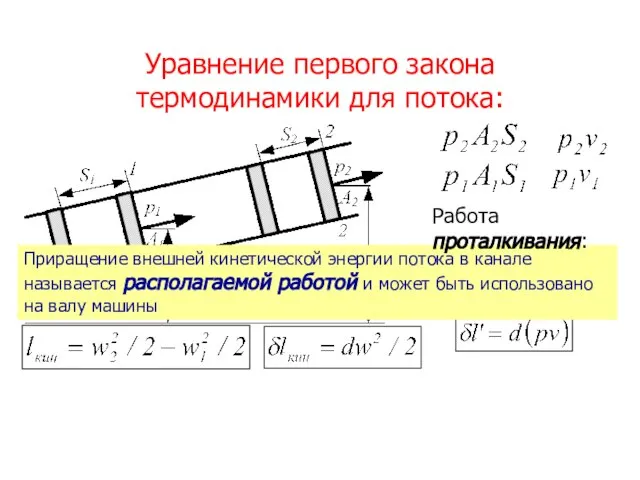
- 26. Уравнение первого закона термодинамики для потока: Приращение внешней кинетической энергии потока в канале называется располагаемой работой
- 27. Работа на изменение внешней потенциальной энергии потока в канале: В общем случае поток между сечениями канала
- 28. (5.10) Полученное уравнение первого закона термодинамики справедливо для любых рабочих тел и, в частности, для идеальных
- 29. (5.11) Уравнения (5.9) и (5.11) выражают первый закон термодинамики, а величину работы pdv можно приравнять правой
- 30. 6. ЭНТАЛЬПИЯ Удельная энтальпия, т.е. отношение энтальпии к массе тела, обозначается h и выражается в джоулях
- 31. (5.15) Удельная энтальпия системы определяется с точностью до некоторой аддитивной постоянной h0. Эту постоянную выбирают произвольно,
- 32. При p=const уравнение (5.13) превращается в (5.18) Дифференциал удельной энтальпии dh есть элементарное количество теплоты, участвующее
- 33. (5.21) Физический смысл энтальпии - удельная энтальпия h равна энергии расширенной системы — тела и окружающей
- 35. Скачать презентацию





















 Современные представления о регуляции метаболизма
Современные представления о регуляции метаболизма Делегирование полномочий в обучении персоналом и его карьерном росте (2)
Делегирование полномочий в обучении персоналом и его карьерном росте (2) Фабрика удобрений на дому. Эм- контейнер
Фабрика удобрений на дому. Эм- контейнер Months
Months 中文
中文 Планирование научно-исследовательской работы
Планирование научно-исследовательской работы Самые милые породы собак
Самые милые породы собак Шаги процесса изменения
Шаги процесса изменения Периметр многоугольника
Периметр многоугольника UN WOMEN Структура Организации Объединенных Наций ООН-женщины
UN WOMEN Структура Организации Объединенных Наций ООН-женщины Презентация на тему Россия на карте (2 класс)
Презентация на тему Россия на карте (2 класс) Варлам Тихонович Шаламов
Варлам Тихонович Шаламов Единая Система Муниципальных Сайтов
Единая Система Муниципальных Сайтов инновационный проект
инновационный проект Презентация на тему Ценности и идеалы
Презентация на тему Ценности и идеалы Электричество в быту
Электричество в быту Подземный сад
Подземный сад Правоотношения и правонарушения
Правоотношения и правонарушения Знакомство с буквой Хх
Знакомство с буквой Хх Приемная кампания 2012
Приемная кампания 2012 Заңды жауапкершілік ұғымы, түрлері, қағидалары
Заңды жауапкершілік ұғымы, түрлері, қағидалары Political Regimes
Political Regimes  Презентация без названия
Презентация без названия Для геймера. Игра и реальность. Ознакомительная версия
Для геймера. Игра и реальность. Ознакомительная версия Закрытое акционерное общество «Финансовая компания «Интерфин трейд»
Закрытое акционерное общество «Финансовая компания «Интерфин трейд» Драматургическая схема построения материала
Драматургическая схема построения материала Мораль Религия
Мораль Религия На страже закона. К 300-летию прокуратуры России
На страже закона. К 300-летию прокуратуры России