Содержание
- 2. 1. Два принципа первого закона термодинамики Первый закон термодинамики является частным случаем всеобщего закона о превращении
- 3. Примечание. В данном уравнении и в дальнейшем удобнее расчет вести на единицу вещества – кг, м3,
- 4. 2. Внутренняя энергия газа Внутренняя энергия – это сумма кинетических энергий частиц (молекул, атомов) газа и
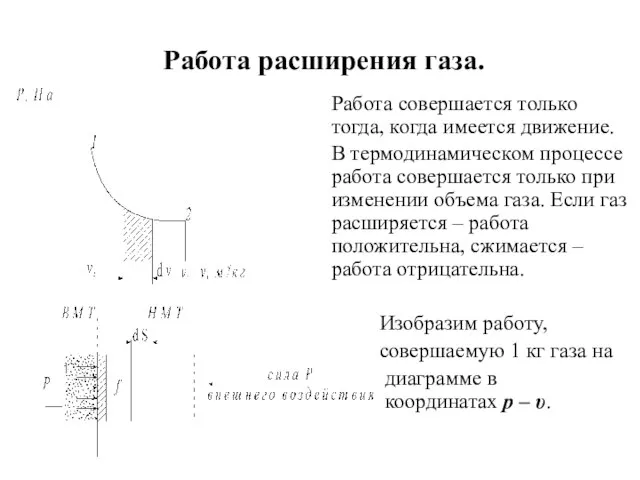
- 5. Работа расширения газа. Работа совершается только тогда, когда имеется движение. В термодинамическом процессе работа совершается только
- 6. Пусть в процессе 1-2 поршень перемещается из положения 1 – верхней мертвой точки (ВМТ) в положение
- 7. Учитывая, что fdS=dv, работа расширения газа на всем участке от v1 до v2 будет равна: При
- 8. 3. Энтальпия газа Энтальпия газа h, Дж/кг равна сумме внутренней энергии газа и произведения давления на
- 9. Изменение энтальпии равно: Учитывая, что получим: После интегрирования в пределах от Т1 до Т2 получим:
- 10. Энтропия газа Не всегда количество подведенной можно определить через изменение температуры тела. Например, вода кипит, а
- 11. Если количество подведённой теплоты не характеризуется соответствующим изменением температуры, то выражение (1) можно превратить в полный
- 13. Скачать презентацию









 МИХАЛЕВ А.С. старший преподаватель кафедры Физики им. В.А. Фабриканта Московского энергетического института
МИХАЛЕВ А.С. старший преподаватель кафедры Физики им. В.А. Фабриканта Московского энергетического института Тундра (4 класс)
Тундра (4 класс) Портфель заместителя директора по информатизации ОУ
Портфель заместителя директора по информатизации ОУ Gоршки от Vовочки. Проект
Gоршки от Vовочки. Проект Кто какую пользу приносит
Кто какую пользу приносит Человек иинформация
Человек иинформация Будем знакомы:Воспитатель 1-ой квалификационной категории Маргарян Ирина Александровна
Будем знакомы:Воспитатель 1-ой квалификационной категории Маргарян Ирина Александровна Пейзаж родной земли. Урок №1
Пейзаж родной земли. Урок №1 РАСПРЕДЕЛЕНИЕ ЖИЗНИ В БИОСФЕРЕ И ОПРЕДЕЛЯЮЩИЕ ФАКТОРЫ
РАСПРЕДЕЛЕНИЕ ЖИЗНИ В БИОСФЕРЕ И ОПРЕДЕЛЯЮЩИЕ ФАКТОРЫ Презентация на тему Устройства компьютера
Презентация на тему Устройства компьютера  Детский лагерь Юность
Детский лагерь Юность ИКТ на уроках английского языка
ИКТ на уроках английского языка Презентация на тему Тест по математике 2 класс
Презентация на тему Тест по математике 2 класс  Основные ошибки рекламодателей в интернете.
Основные ошибки рекламодателей в интернете. ПЕРСПЕКТИВЫ РАЗВИТИЯ НЕФТЕГАЗОПЕРЕРАБАТЫВАЮЩЕЙ И ГАЗОХИМИЧЕСКОЙ ПРОМЫШЛЕННОСТИРЕСПУБЛИКИ САХА (ЯКУТИЯ)
ПЕРСПЕКТИВЫ РАЗВИТИЯ НЕФТЕГАЗОПЕРЕРАБАТЫВАЮЩЕЙ И ГАЗОХИМИЧЕСКОЙ ПРОМЫШЛЕННОСТИРЕСПУБЛИКИ САХА (ЯКУТИЯ) WSEI. Навчання у Польщі
WSEI. Навчання у Польщі Страховая компания с 2021 г
Страховая компания с 2021 г Диагностика острого аппендицита при различных локализациях червеобразного отростка
Диагностика острого аппендицита при различных локализациях червеобразного отростка Автоматизация соноров в словах сложной звукослоговой структуры слова
Автоматизация соноров в словах сложной звукослоговой структуры слова Методы логистического анализа машиностроительной продукции
Методы логистического анализа машиностроительной продукции Внутренние воды северной Америки 7 класс
Внутренние воды северной Америки 7 класс Типы персональных компьютеров
Типы персональных компьютеров Презентация на тему Производство чугуна и стали
Презентация на тему Производство чугуна и стали  Ужель та самая Татьяна?
Ужель та самая Татьяна? Издательство DELTA PUBLISHING
Издательство DELTA PUBLISHING Қисық11А
Қисық11А Методические рекомендации по организации самостоятельных занятий спортом
Методические рекомендации по организации самостоятельных занятий спортом Щеглов Андрей Серафимович. Менеджер по продажам
Щеглов Андрей Серафимович. Менеджер по продажам