Содержание
- 2. ДОКАЗАТЕЛЬСТВО СУЩЕСТВОВАНИЯ МОЛЕКУЛ: 1.БРОУНОВСКОЕ ДВИЖЕНИЕ ОСНОВНЫЕ ПОЛОЖЕНИЯ МКТ Бибиков Д.Н.
- 3. ДОКАЗАТЕЛЬСТВО СУЩЕСТВОВАНИЯ МОЛЕКУЛ: 1.БРОУНОВСКОЕ ДВИЖЕНИЕ ОСНОВНЫЕ ПОЛОЖЕНИЯ МКТ Бибиков Д.Н.
- 4. ОСНОВНЫЕ ПОЛОЖЕНИЯ МКТ ДОКАЗАТЕЛЬСТВО СУЩЕСТВОВАНИЯ МОЛЕКУЛ: 2. ЭЛЕКТРОННЫЙ МИКРОСКОП Бибиков Д.Н.
- 5. ОСНОВНЫЕ ПОЛОЖЕНИЯ МКТ Бибиков Д.Н. РАЗМЕРЫ МОЛЕКУЛ
- 6. ОСНОВНЫЕ ПОЛОЖЕНИЯ МКТ ДОКАЗАТЕЛЬСТВО ДВИЖЕНИЯ МОЛЕКУЛ: 1. ДИФФУЗИЯ Бибиков Д.Н.
- 7. ОСНОВНЫЕ ПОЛОЖЕНИЯ МКТ Бибиков Д.Н.
- 8. ОСНОВНЫЕ ПОЛОЖЕНИЯ МКТ ДОКАЗАТЕЛЬСТВО ДВИЖЕНИЯ МОЛЕКУЛ: 1. ДИФФУЗИЯ Бибиков Д.Н.
- 9. Относительная масса Из химии известен закон постоянных отношений: «При образовании любого количества какого-либо химического соединения массы
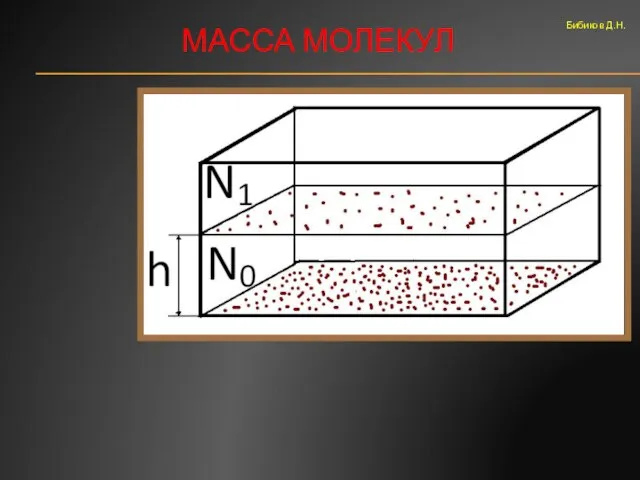
- 10. МАССА МОЛЕКУЛ Бибиков Д.Н.
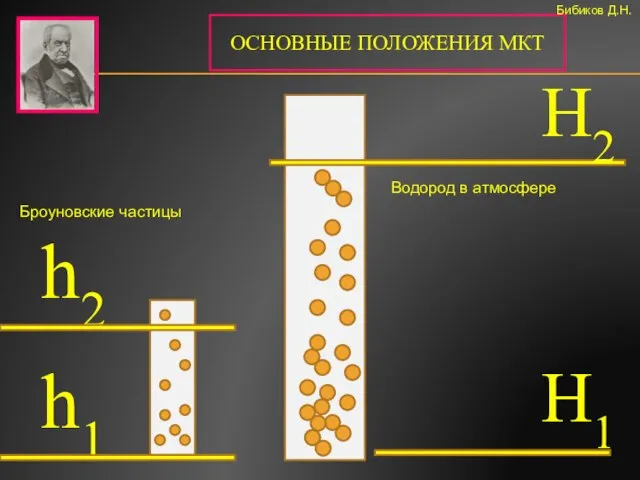
- 11. ОСНОВНЫЕ ПОЛОЖЕНИЯ МКТ Бибиков Д.Н. h2 H2 H1 h1 Водород в атмосфере Броуновские частицы
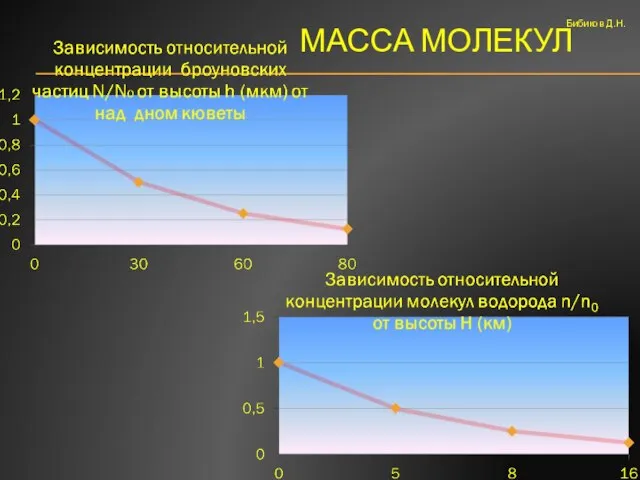
- 12. МАССА МОЛЕКУЛ Бибиков Д.Н.
- 13. МАССА МОЛЕКУЛ Графики подтверждают идентичность процессов, происходящих в вертикальном столбе атмосферы и в вертикальном столбе броуновских
- 14. Бибиков Д.Н.
- 15. Бибиков Д.Н.
- 16. Бибиков Д.Н.
- 17. Бибиков Д.Н.
- 18. Бибиков Д.Н.
- 19. Бибиков Д.Н.
- 20. Изменение концентрации частиц в атмосфере вдвое при изменении высоты на 5000м, а изменение концентрации броуновских частиц
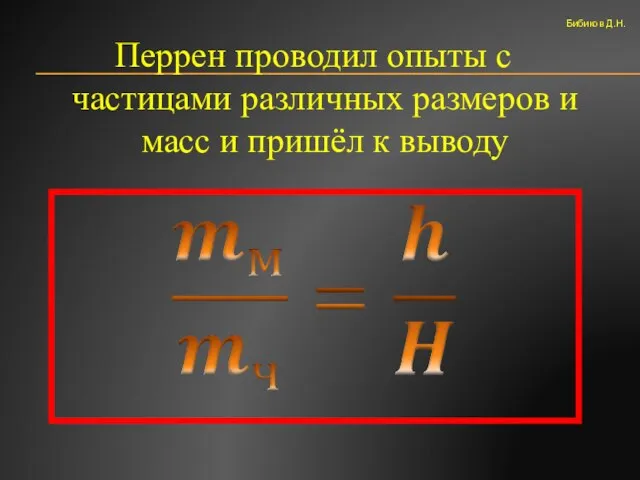
- 21. Перрен проводил опыты с частицами различных размеров и масс и пришёл к выводу Бибиков Д.Н.
- 22. Отсюда, зная массу броуновской частицы находим массу атома водорода Более точное mH=1,67х10-24 грамма Бибиков Д.Н.
- 23. Найдём отношение 1 грамма атомарного водорода к произведению относительной массы водорода на массу атома водорода в
- 24. Умножим числитель и знаменатель на 4 Но 4 а.е.м. это масса гелия, получается, что в веществе
- 25. Бибиков Д.Н.
- 26. Бибиков Д.Н.
- 27. Итак масса одной молекулы равна Число молекул в некоторой массе вещества Бибиков Д.Н.
- 28. Молекулы движутся т.е. имеют энергию движения Молекулы взаимодействуют т.е. имеют энергию взаимодействия Бибиков Д.Н.
- 29. Сумма кинетических энергий хаотического движения молекул и потенциальных энергий их взаимодействия называется внутренней энергией тела Бибиков
- 30. Агрегатные состояние вещества Wк >> Wп – газообразное состояние Wк ≈ Wп – жидкое состояние Wк
- 31. Идеальный газ Молекулы – материальные точки Молекулы не взаимодействуют Столкновение молекул абсолютно упругое Бибиков Д.Н.
- 32. Внутренняя энергия идеального газа равна сумме кинетических энергий молекул Кинетическая энергия молекул равна Бибиков Д.Н.
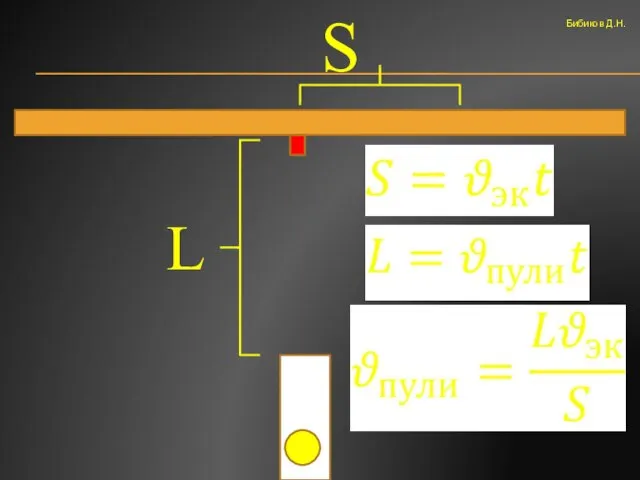
- 33. Бибиков Д.Н. S L
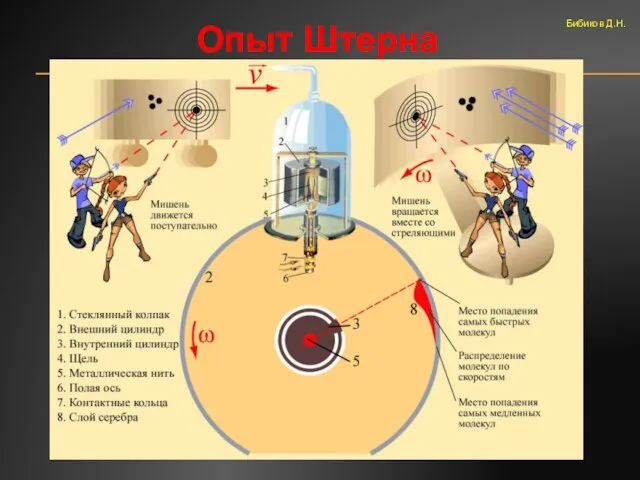
- 34. Опыт Штерна Бибиков Д.Н.
- 35. Распределение Максвелла Бибиков Д.Н.
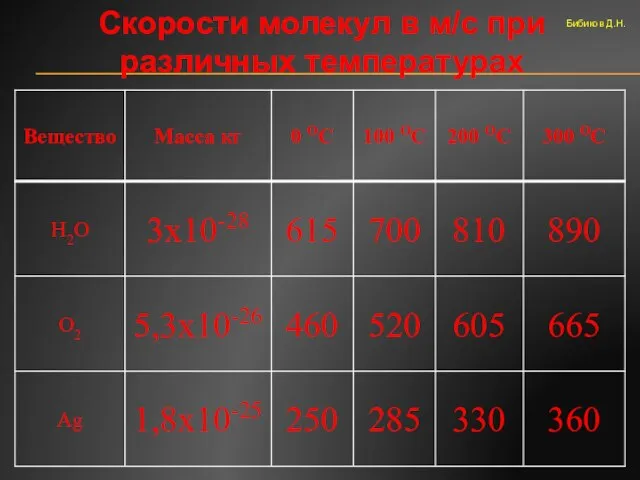
- 36. Скорости молекул в м/с при различных температурах Бибиков Д.Н.
- 37. Выводы из опыта Штерна Скорости молекул одного и того же вещества при одной и той же
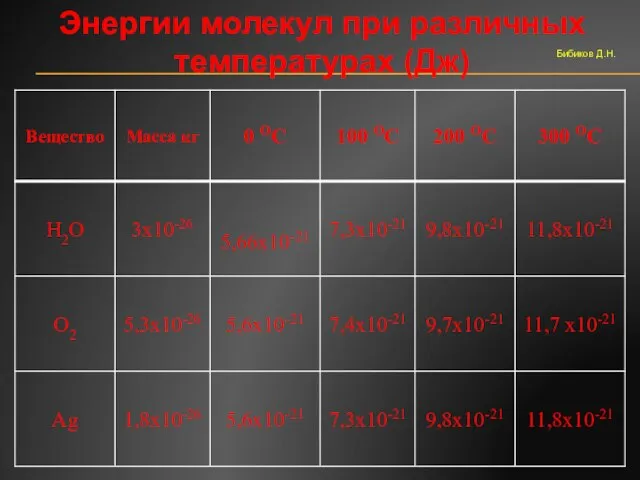
- 38. Энергии молекул при различных температурах (Дж) Бибиков Д.Н.
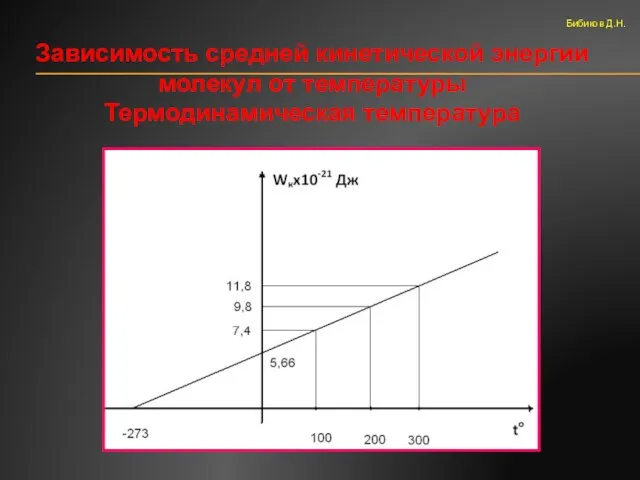
- 39. Зависимость средней кинетической энергии молекул от температуры Термодинамическая температура Бибиков Д.Н.
- 40. Уравнение прямой Wк=bt+Wo Wк=2,07х10-23t+5,66х10-21 Приведём к виду где k- постоянная Больцмана 1,38х10-23 Дж/К Бибиков Д.Н.
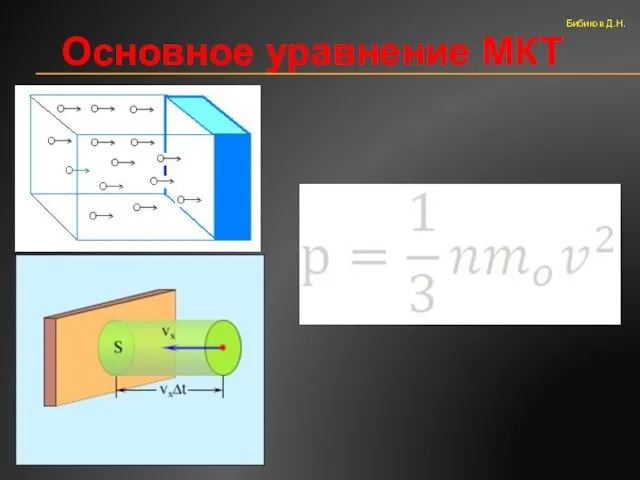
- 41. Основное уравнение МКТ Бибиков Д.Н.
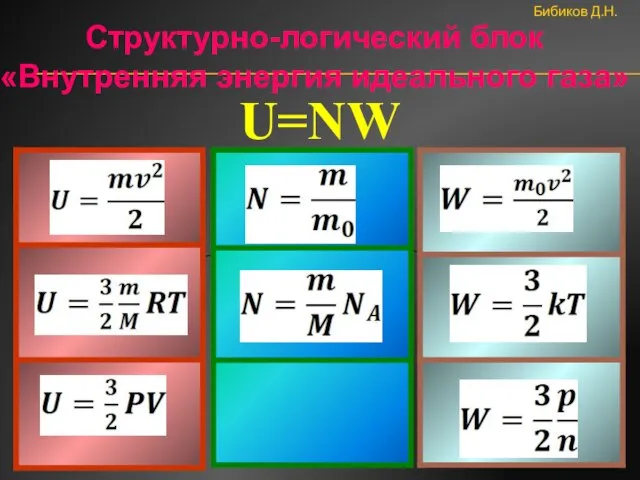
- 42. Бибиков Д.Н. Структурно-логический блок «Внутренняя энергия идеального газа» U=NW
- 43. Уравнение состояния Бибиков Д.Н.
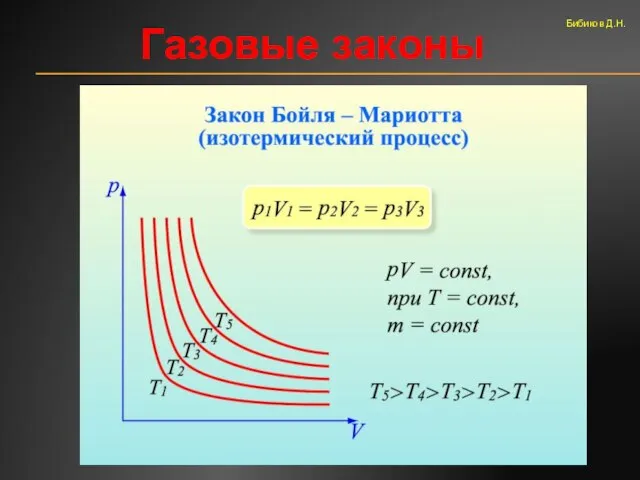
- 44. Газовые законы Бибиков Д.Н.
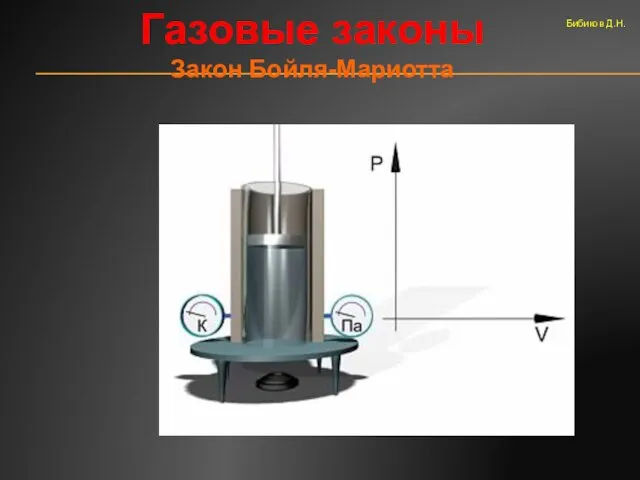
- 45. Газовые законы Закон Бойля-Мариотта Бибиков Д.Н.
- 46. Газовые законы Бибиков Д.Н.
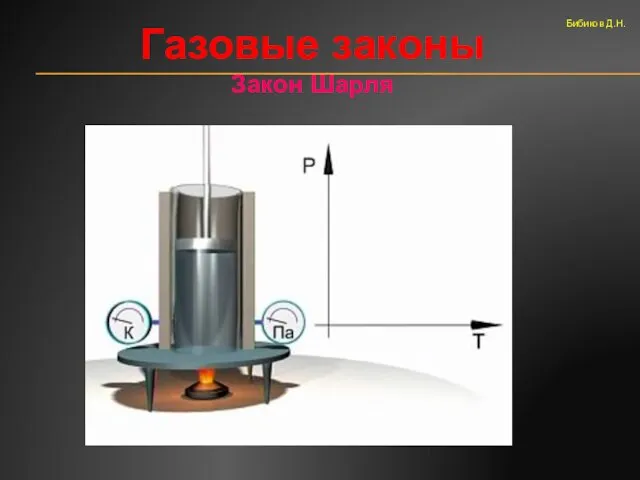
- 47. Газовые законы Закон Шарля Бибиков Д.Н.
- 48. Газовые законы Бибиков Д.Н.
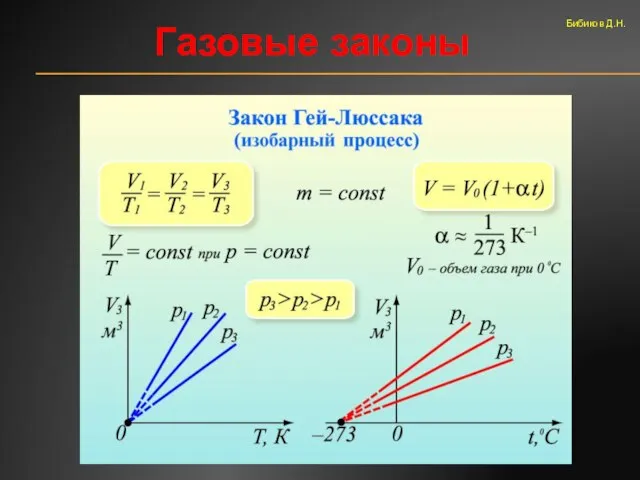
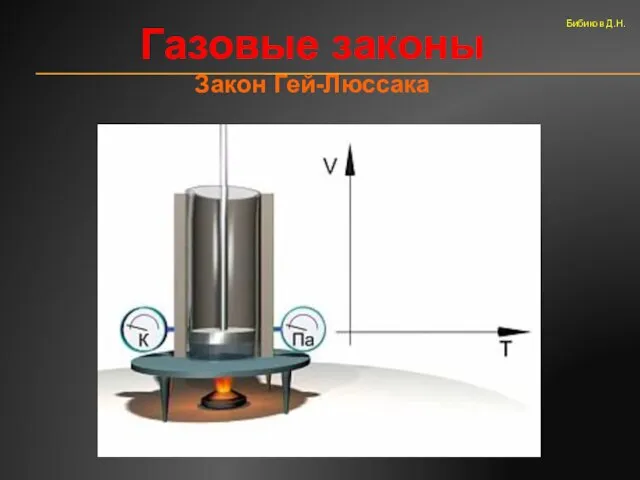
- 49. Газовые законы Закон Гей-Люссака Бибиков Д.Н.
- 50. ИЗМЕНЕНИЕ ВНУТРЕННЕЙ ЭНЕРГИИ Бибиков Д.Н.
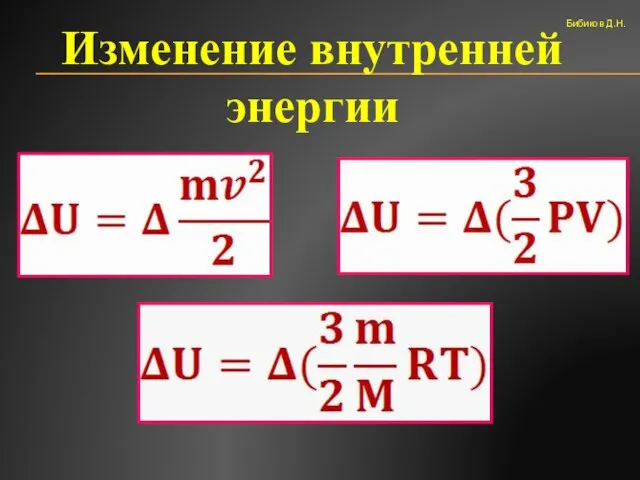
- 51. Изменение внутренней энергии Бибиков Д.Н.
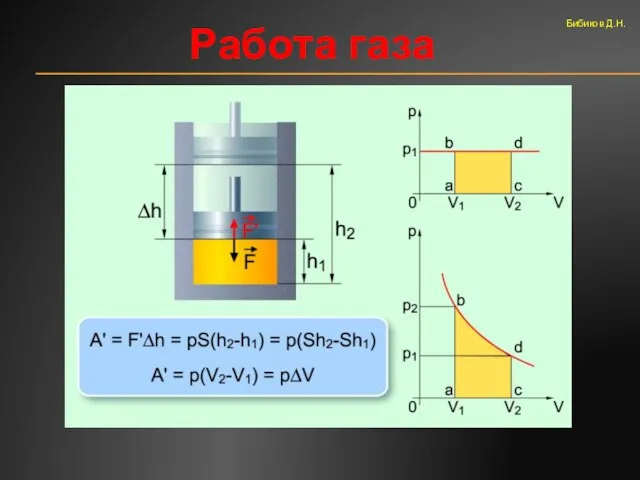
- 52. Работа газа Бибиков Д.Н.
- 53. КОЛИЧЕСТВО ТЕПЛОТЫ Бибиков Д.Н.
- 54. ПРИМЕНЕНИЕ ПЕРВОГО ЗАКОНА ТЕРМОДИНАМИКИ К РАЗЛИЧНЫМ ПРОЦЕССАМ Изохорный процесс А=0 ΔU=Q Изотермический процесс ΔU=0 Q=Aг Изобарный
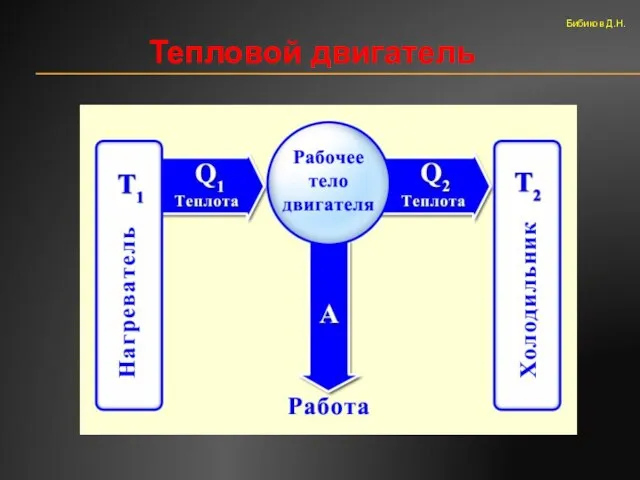
- 55. Тепловой двигатель Бибиков Д.Н.
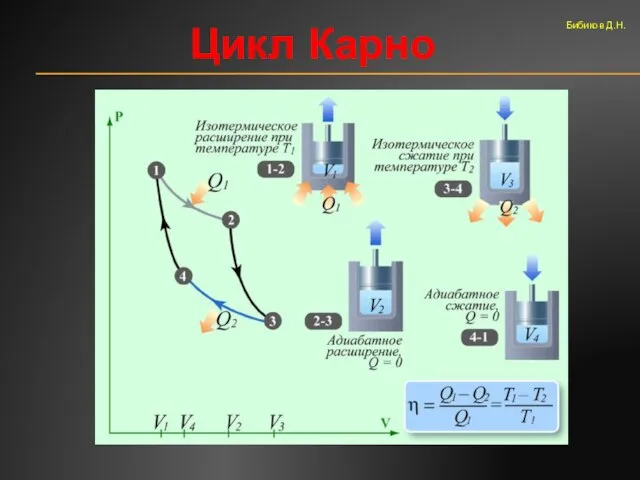
- 56. Цикл Карно Бибиков Д.Н.
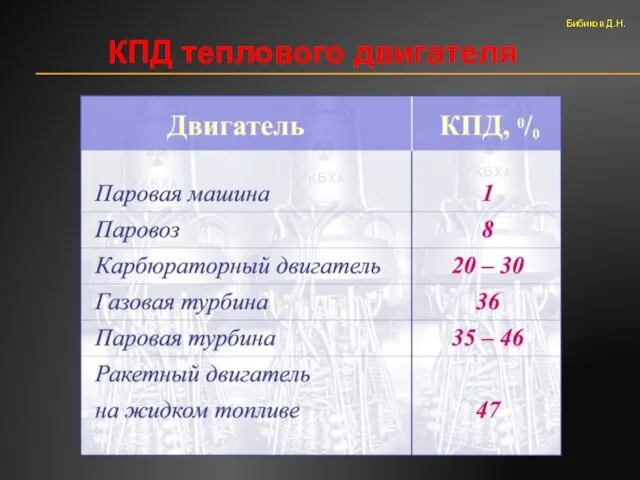
- 57. КПД теплового двигателя Бибиков Д.Н.
- 58. КПД теплового двигателя Бибиков Д.Н.
- 59. Бибиков Д.Н.
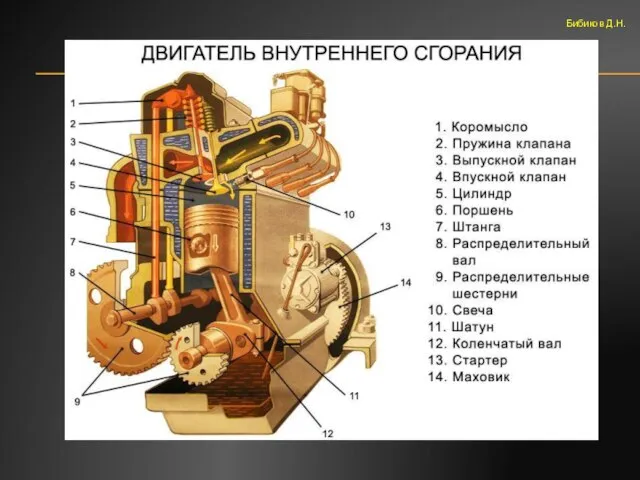
- 60. ЧЕТЫРЁХТАКТНЫЙ ДВИГАТЕЛЬ Бибиков Д.Н.
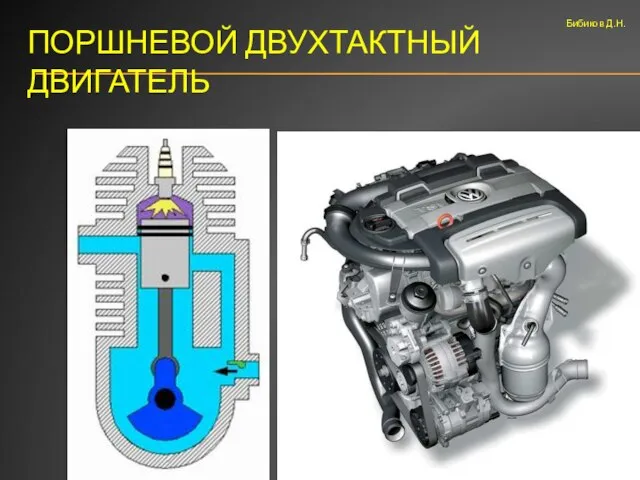
- 61. ПОРШНЕВОЙ ДВУХТАКТНЫЙ ДВИГАТЕЛЬ Бибиков Д.Н.
- 62. ДВИГАТЕЛЬ ВАНКЕЛЯ (РПД)
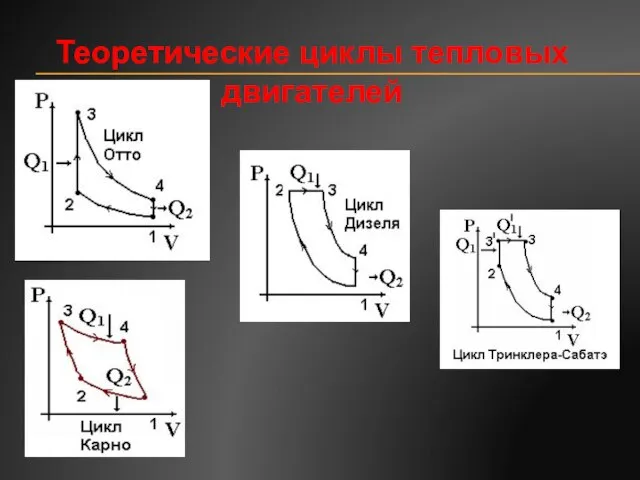
- 63. Теоретические циклы тепловых двигателей
- 64. Турбины
- 66. Скачать презентацию









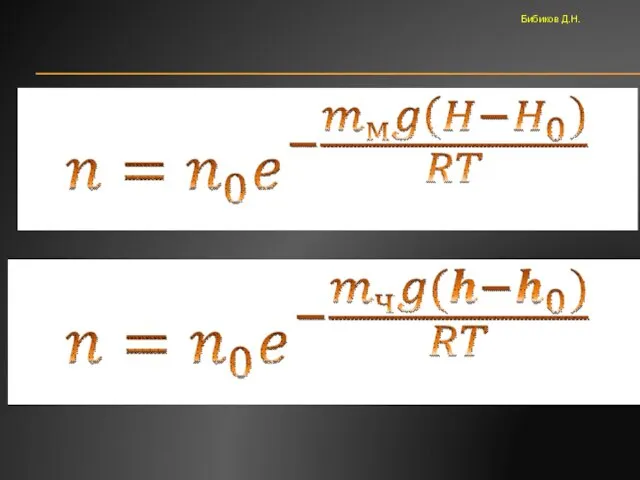


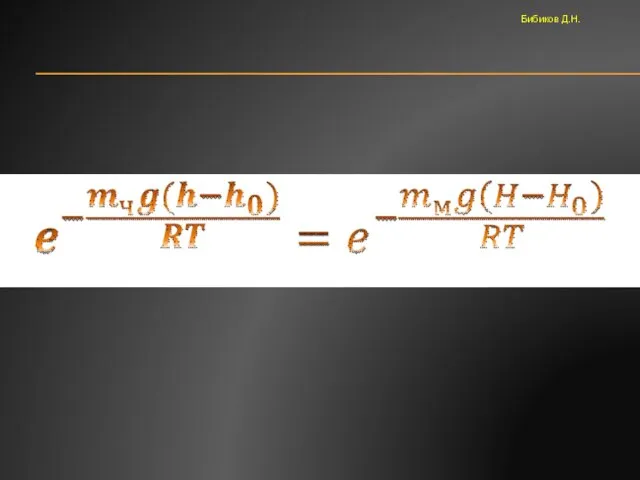


























 Навчальний пункт аварійнорятувального загону спеціального призначення Головного управління, місто Рубіжне, Луганська область
Навчальний пункт аварійнорятувального загону спеціального призначення Головного управління, місто Рубіжне, Луганська область 9
9 КОНТЕКСТНАЯ РЕКЛАМА.ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
КОНТЕКСТНАЯ РЕКЛАМА.ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ АВСТРАЛИЯ
АВСТРАЛИЯ Alpe. Медицинские пластыри
Alpe. Медицинские пластыри День государственного флага Российской Федерации
День государственного флага Российской Федерации К вопросу о Национальной лекарственной политике в России
К вопросу о Национальной лекарственной политике в России Улицы в лицах
Улицы в лицах Замятин
Замятин «Не стыдно не знать,
«Не стыдно не знать, ФИЗИОЛОГИЯ МЫШЦ
ФИЗИОЛОГИЯ МЫШЦ  МОБИЛЬНЫЕ ТЕЛЕФОНЫ SONIM:РЕШЕНИЯ ДЛЯ БИЗНЕСА
МОБИЛЬНЫЕ ТЕЛЕФОНЫ SONIM:РЕШЕНИЯ ДЛЯ БИЗНЕСА Толерантность в школе
Толерантность в школе Группа компаний Стройкомплект
Группа компаний Стройкомплект ОБЪЕДИНЕННАЯ РАБОЧАЯ ГРУППА ПО РЕФОРМИРОВАНИЮ СФЕР ЖКХ, СТРОИТЕЛЬСТВА И ЭНЕРГЕТИКИ
ОБЪЕДИНЕННАЯ РАБОЧАЯ ГРУППА ПО РЕФОРМИРОВАНИЮ СФЕР ЖКХ, СТРОИТЕЛЬСТВА И ЭНЕРГЕТИКИ Буква ю
Буква ю Презентация на тему Колумбия
Презентация на тему Колумбия Презентация на тему Вавилонский царь Хаммурапи и его законы
Презентация на тему Вавилонский царь Хаммурапи и его законы  Презентация на тему Полные квадратные уравнения (общая формула)
Презентация на тему Полные квадратные уравнения (общая формула)  Сущность и функции денег
Сущность и функции денег Раскадровка Презентации телеканала Семерка
Раскадровка Презентации телеканала Семерка Urok_15_Skazka_Fontan_kotory_umel_plavat
Urok_15_Skazka_Fontan_kotory_umel_plavat Итоги заседания общего собрания РАО 17.05.2018
Итоги заседания общего собрания РАО 17.05.2018 Международное право. Международно-правовые средства разрешения споров
Международное право. Международно-правовые средства разрешения споров «Вся гордость мира – от матери!»
«Вся гордость мира – от матери!» Педагогическая родословная моей семьи
Педагогическая родословная моей семьи Презентация на тему омонимы 3 класс
Презентация на тему омонимы 3 класс  Детская организация Тенгрин герл
Детская организация Тенгрин герл