Содержание
- 2. Проблемы этической экспертизы клинических исследований в РФ Правовые Методические Организационные Возможности легитимного решения
- 3. Правовые основы этической экспертизы Хельсинкская декларация ВМА Конвенция по защите прав человека и человеческого достоинства применительно
- 4. Методические основы этической экспертизы Международные этические правила биомедицинских исследований с включением людей Совета Международных организаций по
- 5. Правовые основы этической экспертизы в России Основы законодательства РФ об охране здоровья граждан (требует информированного согласия
- 6. Проблемы с правовой основой Федеральный закон «О лекарственных средствах» (ст. 37): «…Решение о проведении клинических исследований
- 7. Российское законодательство (после отмены ст. 16 ОЗоЗГ) Комитет по этике при Федеральном органе контроля качества ЛС:
- 8. Методические проблемы У разных ЭК подходы к оценке отличаются Различная структура и процедуры (СОПы) Различные способы
- 9. Проблема качества этической экспертизы Различное качество экспертизы Возможность лишенных обоснования решений и рекомендаций Отсутствие механизмов менеджмента
- 10. Организационные проблемы Под вопросом смысл рекомендаций ЛЭК, поскольку проблема – в их реализации Нежелание спонсоров обсуждать
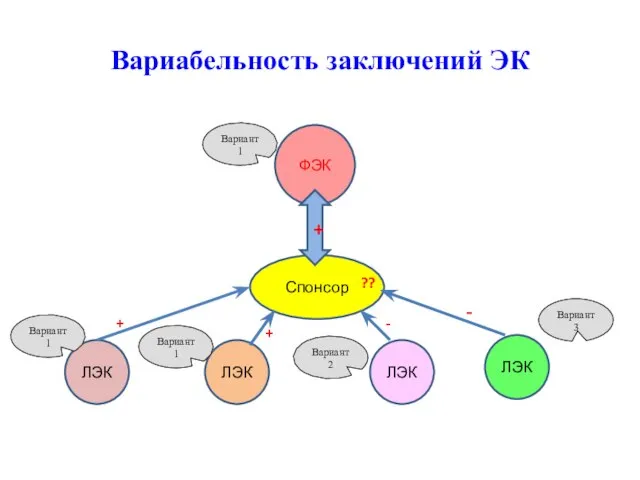
- 11. Вариабельность заключений ЭК ФЭК Спонсор ЛЭК ЛЭК ЛЭК ЛЭК + + + - - ?? Вариант
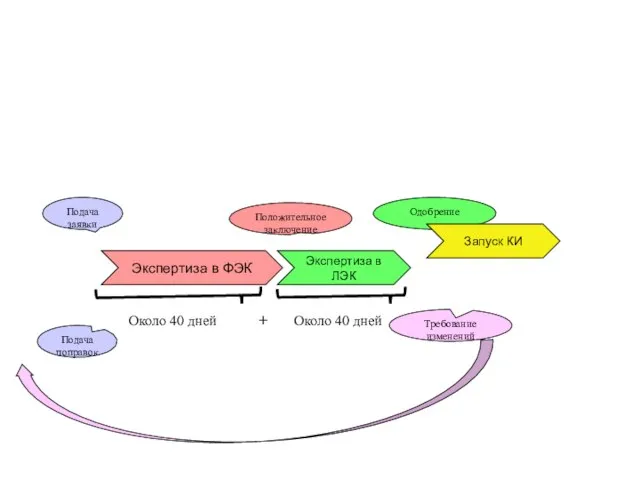
- 12. Экспертиза в ФЭК Подача заявки Экспертиза в ЛЭК Положительное заключение Одобрение Запуск КИ Около 40 дней
- 13. Подробное руководство по формату заявок и документации, представляемых при ходатайстве о вынесении заключения Комитета по этике
- 14. Возможные решения Локальные версии Работа ЭК с врачами-исследователями Информирование PI обо всех вотумах? Выработка консенсусных версий?
- 16. Скачать презентацию










 “ИНОВАТИВНА МРЕЖА ЗА РАЗВИТИЕНА СОЦИАЛНИ ПРЕДПРИЯТИЯ”
“ИНОВАТИВНА МРЕЖА ЗА РАЗВИТИЕНА СОЦИАЛНИ ПРЕДПРИЯТИЯ”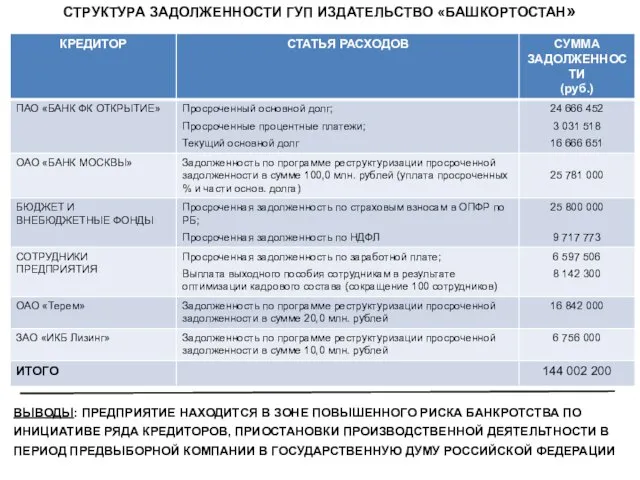 Проект реструктуризации задолженности ГУП Издательство Башкортостан
Проект реструктуризации задолженности ГУП Издательство Башкортостан Предупреждение заболеваний сердца и сосудов
Предупреждение заболеваний сердца и сосудов Где и как появились первые игрушки?
Где и как появились первые игрушки? Итоги работы секции языкознания: было представлено 5 работ.
Итоги работы секции языкознания: было представлено 5 работ. Внутренняя энергия
Внутренняя энергия Понятие и источники предпринимательского права
Понятие и источники предпринимательского права Управление контейнерным терминалом (CMS)
Управление контейнерным терминалом (CMS) Тема проповеди: Секрет 10 конвертов, или Как правильно планировать семейный бюджет
Тема проповеди: Секрет 10 конвертов, или Как правильно планировать семейный бюджет Здоровое питание. Правила
Здоровое питание. Правила Программы и файлы. Рабочий стол
Программы и файлы. Рабочий стол Олимпийские игры
Олимпийские игры Перспективные направления и формы работы с педагогами и обучающимися ММЦ ИТ Балаковского района
Перспективные направления и формы работы с педагогами и обучающимися ММЦ ИТ Балаковского района Оплодотворение и развитие организма
Оплодотворение и развитие организма Оздоровительные технологии в МОУ СОШ № 90 «Крепыш»
Оздоровительные технологии в МОУ СОШ № 90 «Крепыш» Евгений Родионов
Евгений Родионов Книжная полка:учебники и учебные пособия для преподавания русского языка как второго родного
Книжная полка:учебники и учебные пособия для преподавания русского языка как второго родного Новогодние традиции Южной Кореи
Новогодние традиции Южной Кореи Исследование функции на монотонность
Исследование функции на монотонность А.С. Пушкин и Костромской край
А.С. Пушкин и Костромской край Некрасов «Дедушка Мазай и зайцы»
Некрасов «Дедушка Мазай и зайцы» История Заглядинской средней школы
История Заглядинской средней школы Новый маршрут уралмашевского автобуса
Новый маршрут уралмашевского автобуса Неповторний Киев. Фотоальбом
Неповторний Киев. Фотоальбом Растровые светильники
Растровые светильники Составление связного высказывания с использованием предложений определенной структуры, в том числе на лингвистическую тему
Составление связного высказывания с использованием предложений определенной структуры, в том числе на лингвистическую тему Отделение лесного хозяйства ВГМХА
Отделение лесного хозяйства ВГМХА Использование информационных технологий в обучении истории и обществознания
Использование информационных технологий в обучении истории и обществознания