Содержание
- 2. ЦЕЛЬ УРОКА Цель деятельности педагога Интеграция школьных естественнонаучных предметов для дальнейшего развития и совершенствования химического образования
- 3. ЗАДАЧИ УРОКА Дидактические задачи. Обобщение знаний учащихся о растворах, осуществление коррекции знаний, создание условий для этих
- 4. ЗАДАЧИ УРОКА Развивающие задачи. Развитие логического мышления, а именно синтетико-аналитического на основе выполнения практических заданий, а
- 5. АКТУАЛИЗАЦИЯ ОСНОВНЫХ ПОНЯТИЙ МАССОВАЯ ДОЛЯ – отношение массы растворенного вещества к массе раствора. Например, водный раствор
- 6. АКТУАЛИЗАЦИЯ ОСНОВНЫХ ПОНЯТИЙ МОЛЯРНАЯ ДОЛЯ – отношение количества растворенного вещества (или растворителя) к сумме количеств веществ,
- 7. АКТУАЛИЗАЦИЯ ОСНОВНЫХ ПОНЯТИЙ МОЛЯРНАЯ КОНЦЕНТРАЦИЯ (МОЛЯРНОСТЬ) – отношение количества растворенного вещества (или растворителя) к объему раствора.
- 8. АКТУАЛИЗАЦИЯ ОСНОВНЫХ ПОНЯТИЙ Эквивалентная (нормальная) концентрация отношение числа эквивалентов растворенного вещества к объему раствора. Пример 2
- 9. РЕШЕНИЕ ЭКСПЕРИМЕНТАЛЬНО-РАСЧЕТНЫХ ЗАДАЧ ПО РАСТВОРАМ Оборудование: штатив с пробирками, растворы хлорид бария, серная кислота, коническая колба,
- 10. ЗАДАЧА №1 определение массы вещества по заданной концентрации ДАНО: m (BaSO4) = 23,3 ω (H2SO4) =
- 11. ЗАДАЧА № 2 определение объема раствора по известной его концентрации ДАНО: ω (H2SO4) = 96% ρ
- 12. АКТУАЛИЗАЦИЯ МЕЖПРЕДМЕТНЫХ ПОНЯТИЙ Диффузия – это движение молекул или ионов из области с высокой концентрации в
- 13. ОПЫТ №1 Изучение осмоса в живых растительных клетках Материал и оборудование эпидермис (кожица) лука или молодого
- 14. ОПЫТ №1 Изучение осмоса в живых растительных клетках Методика проведения опыта Скальпелем отделите другую полоску эпидермиса
- 15. ОПЫТ №1 Изучение осмоса в живых растительных клетках Результаты: учащиеся должны были определить, какие процессы происходили
- 16. ОПЫТ №2 Определение среднего осмотического давления клеточного сока в препарате растительных клеток методом начинающего плазмолиза Материал
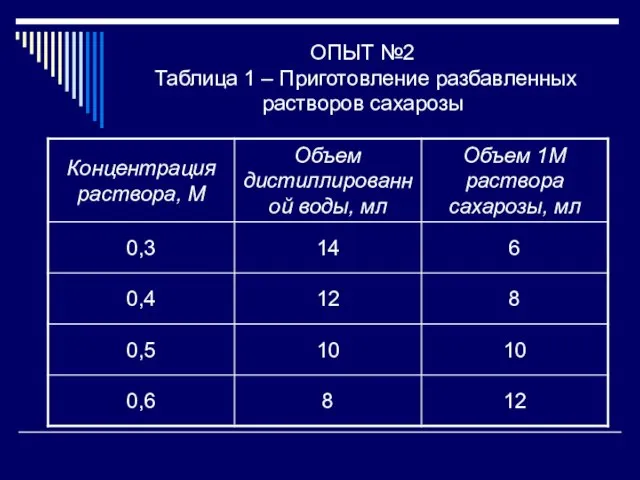
- 17. ОПЫТ №2 Таблица 1 – Приготовление разбавленных растворов сахарозы
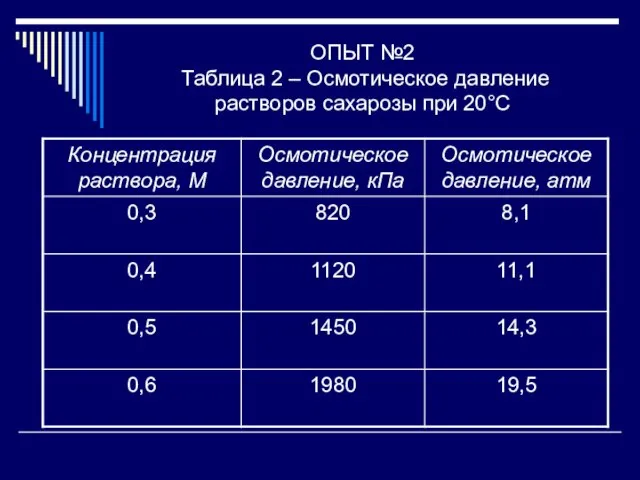
- 18. ОПЫТ №2 Таблица 2 – Осмотическое давление растворов сахарозы при 20°С
- 19. ПРОВЕРКА ПОЛУЧЕННЫХ ЗНАНИЙ ВОПРОСЫ Расскажите, как произвести плазмолиз опытным путем? В чем суть деплазмолиза? Существует ли
- 21. Скачать презентацию
















 Международная торговля услугами
Международная торговля услугами  Техника бега на средние дистанции
Техника бега на средние дистанции
 Э́двард Мунк
Э́двард Мунк «Развитие ипотечного кредитования в регионах РФ, практика и особенности» Директор Департамента кредитных операций ЗАО «Банк Жил
«Развитие ипотечного кредитования в регионах РФ, практика и особенности» Директор Департамента кредитных операций ЗАО «Банк Жил Презентация на тему Стратегия Казахстан - 2050
Презентация на тему Стратегия Казахстан - 2050  «Жить – значит иметь проблемы, решать проблемы – значит растиинтеллектуально».Д.П. Гуплдфорд, психолог`
«Жить – значит иметь проблемы, решать проблемы – значит растиинтеллектуально».Д.П. Гуплдфорд, психолог` В гонках участвуют черепахи.
В гонках участвуют черепахи. Имя прилагательноеОчень занимательное.Его вопросы чей? Какой?Запомнит ученик любой.Оно обозначаетПризнаки предметов.И без сущ
Имя прилагательноеОчень занимательное.Его вопросы чей? Какой?Запомнит ученик любой.Оно обозначаетПризнаки предметов.И без сущ Живопись в формировании эстетического взгляда на жизнь
Живопись в формировании эстетического взгляда на жизнь Enjoy English
Enjoy English Что такое экономика?
Что такое экономика? Военно-промышленный завод Fighting robots
Военно-промышленный завод Fighting robots  Суперконденсаторы для гибридного и электро-транспорта Мурышев Андрей Евгеньевич Проектный директор Наноцентра «Дубна»
Суперконденсаторы для гибридного и электро-транспорта Мурышев Андрей Евгеньевич Проектный директор Наноцентра «Дубна» Использование информационных компьютерных технологий в специальном (коррекционном) образовании
Использование информационных компьютерных технологий в специальном (коррекционном) образовании 1 1 Контекстная реклама для Авто: Авто-дилеры, авто-бренды, авто-СМИ. Наумов Алексей, ЗАО «Бегун»
1 1 Контекстная реклама для Авто: Авто-дилеры, авто-бренды, авто-СМИ. Наумов Алексей, ЗАО «Бегун» Игра «Кто хочет стать историком»
Игра «Кто хочет стать историком» Макетирование и поиск идей для позиционирования бренда Саровский кирпичный завод
Макетирование и поиск идей для позиционирования бренда Саровский кирпичный завод День рождения нашей крошки
День рождения нашей крошки Инфраструктура в борьбе за внедрение ЭДОИЛИ «Кому нужны системы ЭДО»
Инфраструктура в борьбе за внедрение ЭДОИЛИ «Кому нужны системы ЭДО» Напольная ваза «Фантазия»
Напольная ваза «Фантазия» Презентация на тему Свежие плоды
Презентация на тему Свежие плоды ИСПАНИЯ
ИСПАНИЯ Институты и субинституты финансового права
Институты и субинституты финансового права Теория фильтров А. Керкгоффа и К. Дэвиса
Теория фильтров А. Керкгоффа и К. Дэвиса Буквы О и Е после шипящих и Ц в суффиксах и окончаниях имен существительных
Буквы О и Е после шипящих и Ц в суффиксах и окончаниях имен существительных Физическая культура в жизни человека и общества
Физическая культура в жизни человека и общества Образ Александра Невского в искусстве
Образ Александра Невского в искусстве