Содержание
- 2. Химические реакции Обратимые Необратимые
- 3. Задание 1: Написать факторы, влияющие на скорость химических реакций
- 4. Задание 2 : Написать кинетические уравнения для химических реакций II вариант H2S + SO2 ⬄ S
- 5. Состояние системы, при котором скорость образования новых продуктов равна скорости их превращения в исходные вещества, называется
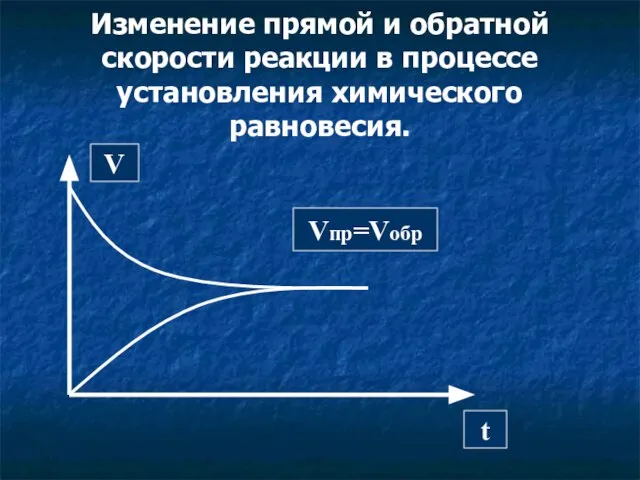
- 6. Изменение прямой и обратной скорости реакции в процессе установления химического равновесия. V t Vпр=Vобр
- 7. Равновесными концентрациями называются концентрации всех веществ системы, которые устанавливаются в ней при наступлении состояния химического равновесия
- 8. Константа равновесия – это отношение произведений концентраций продуктов реакций к произведению концентраций исходных веществ
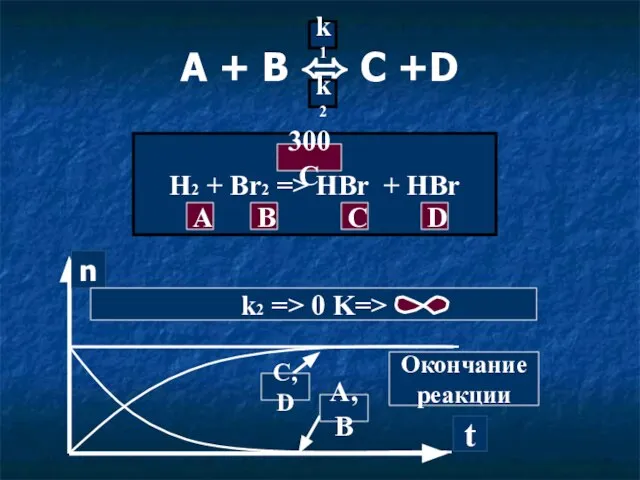
- 9. A + B ⬄ C +D k1 k2 H2 + Br2 => HBr + HBr A
- 10. K = k1:k2 = =[C]равн*[D]равн:[A]равн*[B]равн 300C H2 + I2 ⬄ HI + HI A B C
- 11. Условия смещения химического равновесия - принцип Ле - Шателье «Бегство от насилия»
- 12. Если на систему, находящуюся в равновесии, производится какое-либо внешнее воздействие, то оно благоприятствует протеканию такой реакции,
- 13. A + B ⬄ C + Q t+ t-
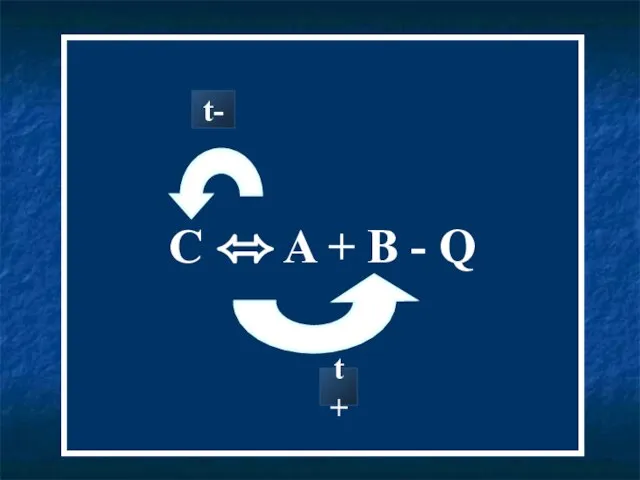
- 14. C ⬄ A + B - Q t- t+
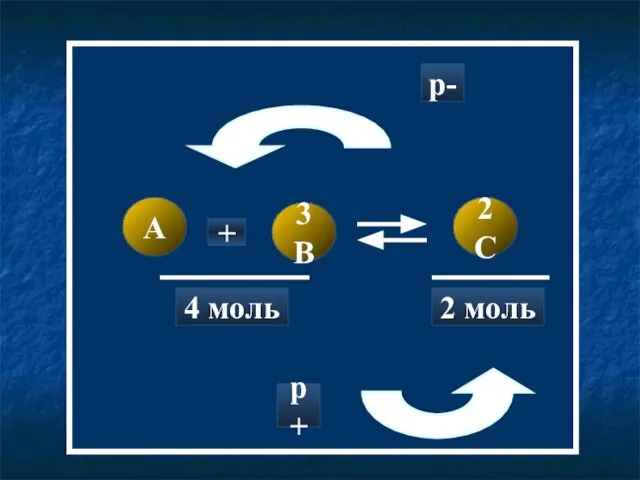
- 15. A 3B 2C + 4 моль 2 моль p- p+
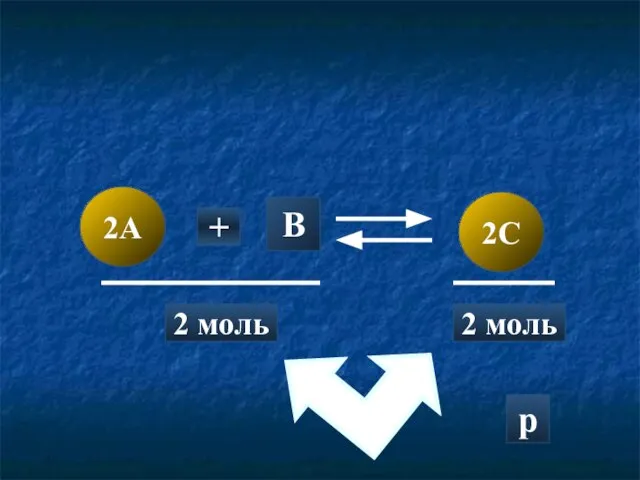
- 16. 2A 2C + B 2 моль 2 моль p
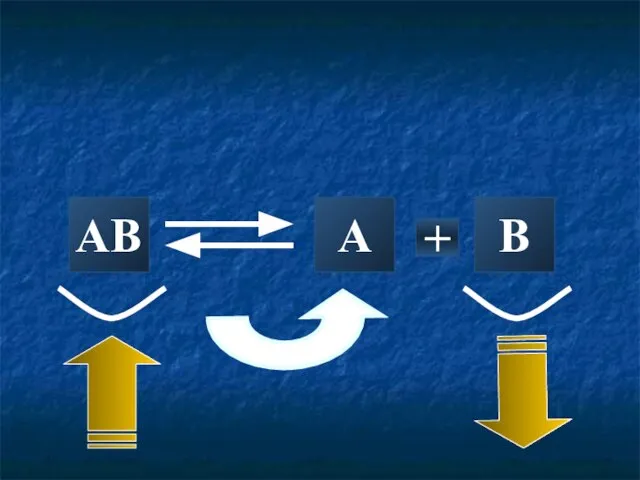
- 17. AB A + B
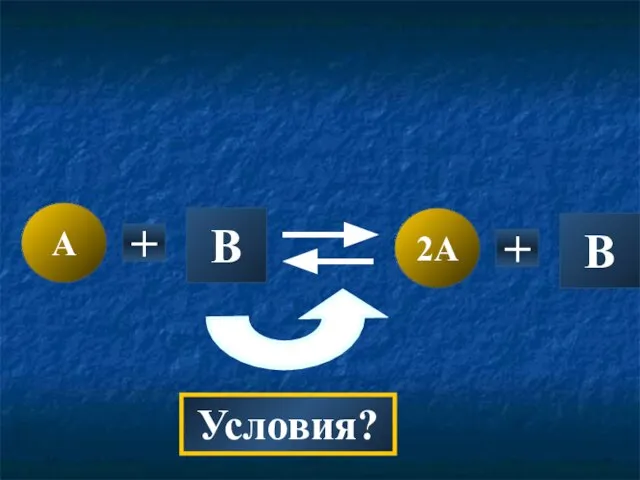
- 18. A 2A + B B + Условия?
- 20. Скачать презентацию





![K = k1:k2 = =[C]равн*[D]равн:[A]равн*[B]равн 300C H2 + I2 ⬄ HI +](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/373075/slide-9.jpg)



 Презентация на тему 9 famous dogs
Презентация на тему 9 famous dogs  Физиология и фармакология рецепторов
Физиология и фармакология рецепторов Особенности проведения тестов на проникновение в организациях банковской сферы
Особенности проведения тестов на проникновение в организациях банковской сферы Презентация на тему Право и правопорядок
Презентация на тему Право и правопорядок Стоматологияда тіс протездерін дайындау технологиясының рольі, мақсаты және міндеті
Стоматологияда тіс протездерін дайындау технологиясының рольі, мақсаты және міндеті Фабрика звезд
Фабрика звезд ХІТ-ПАРАД МОБІЛЬНОГО ШАХРАЙСТВА. - презентация
ХІТ-ПАРАД МОБІЛЬНОГО ШАХРАЙСТВА. - презентация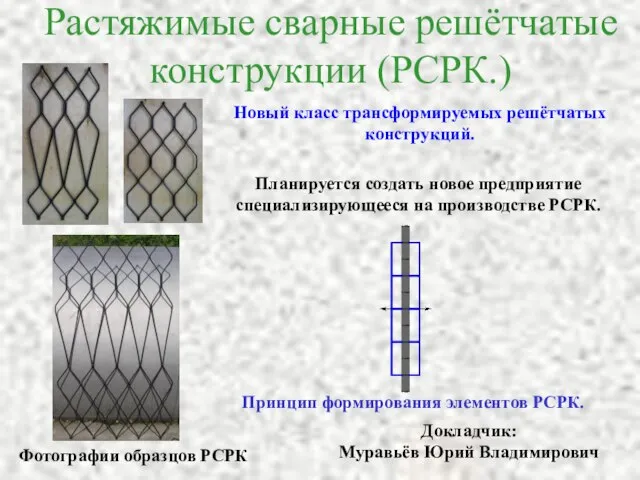 Растяжимые сварные решётчатые конструкции (РCРК.)
Растяжимые сварные решётчатые конструкции (РCРК.) МЕТОД ПРОЕКТОВ В ОБУЧЕНИИ ШКОЛЬНИКОВ БИОЛОГИИ
МЕТОД ПРОЕКТОВ В ОБУЧЕНИИ ШКОЛЬНИКОВ БИОЛОГИИ Население России
Население России Попеременный двухшажный ход
Попеременный двухшажный ход Благовещение. Иконография
Благовещение. Иконография Грани материнства и отцовства. Для православных родителей
Грани материнства и отцовства. Для православных родителей Компьютер и здоровье человека
Компьютер и здоровье человека Петербург – военная столица
Петербург – военная столица Страна тюльпания
Страна тюльпания МОУ ДОД ДУМ
МОУ ДОД ДУМ Lida Milk Plant
Lida Milk Plant Best places to study
Best places to study банк
банк 2011-2012 уч.год
2011-2012 уч.год Презентация на тему: НАФТА
Презентация на тему: НАФТА И я хочу подарить тебе 13 истин!!!
И я хочу подарить тебе 13 истин!!! Иллюзии Копперфильда
Иллюзии Копперфильда Вихревое электрическое поле. Ток смещения
Вихревое электрическое поле. Ток смещения Система образовательных порталов. Анализ телекоммуникационной инфраструктуры. Общие требования к аппаратным платформам, техниче
Система образовательных порталов. Анализ телекоммуникационной инфраструктуры. Общие требования к аппаратным платформам, техниче Кредитные продукты как объекты продаж с использованием маркетинговых технологий
Кредитные продукты как объекты продаж с использованием маркетинговых технологий Современный урок при переходе на вторые стандарты
Современный урок при переходе на вторые стандарты