Содержание
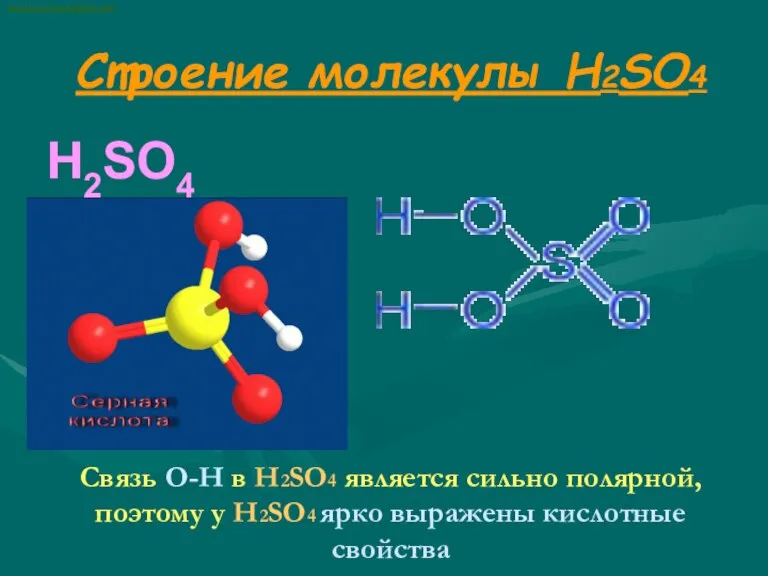
- 2. Строение молекулы H2SO4 H2SO4 Связь О-Н в H2SO4 является сильно полярной, поэтому у H2SO4 ярко выражены
- 3. Производство серной кислоты 1-я стадия. Печь для обжига колчедана. 4FeS2 + 11O2 => 2Fe2O3 + 8SO2
- 4. Физические свойства Тяжелая маслянистая жидкость ("купоросное масло"); p = 1,84 г/см3; Нелетучая, хорошо растворима в воде
- 5. Химические свойства H2SO4 - сильная двухосновная кислота H2SO4 ⬄ H+ + HSO4- ⬄2H+ + SO42- 1)
- 6. 3) с основаниями: H2SO4 + 2NaOH => Na2SO4 + 2H2O H+ + OH- => H2O H2SO4
- 7. ВАСИЛИЙ КАДЕВИЧ 2008 5) концентрированная H2+6SO4 – сильный окислитель; при взаимодействии с металлами (кроме Au, Pt)
- 8. 6) концентрированная H2S+6O4 реагирует при нагревании с некоторыми неметаллами за счет своих сильных окислительных свойств, превращаясь
- 9. 6) Гигроскопичность серной кислоты Концентрированная серная кислота жадно набирает воду отовсюду, образуя гидраты, и способна для
- 10. Концентрированная серная кислота энергично обугливает сахарозу
- 12. Помните! При приготовлении раствора кислоту вливать малыми порциями в воду, а не наоборот!
- 13. В природе встречается 180 минералов сульфатов, и на их долю приходится ~0,5 % массы земной коры.
- 14. Серная кислота в природе Кислые озёра
- 15. Существуют предположения, что кислотное озеро возникло сравнительно недавно в результате извержения, произошедшего незаметно для людей. Тот,
- 16. Серная кислота – очень активная жидкость, особенно концентрированная, которая реагирует со многими неорганическими веществами, также она
- 17. ВАСИЛИЙ КАДЕВИЧ 2008 Применение H2SO4 В производстве пластмассы В производстве синтетического волокна В средствах защиты растений
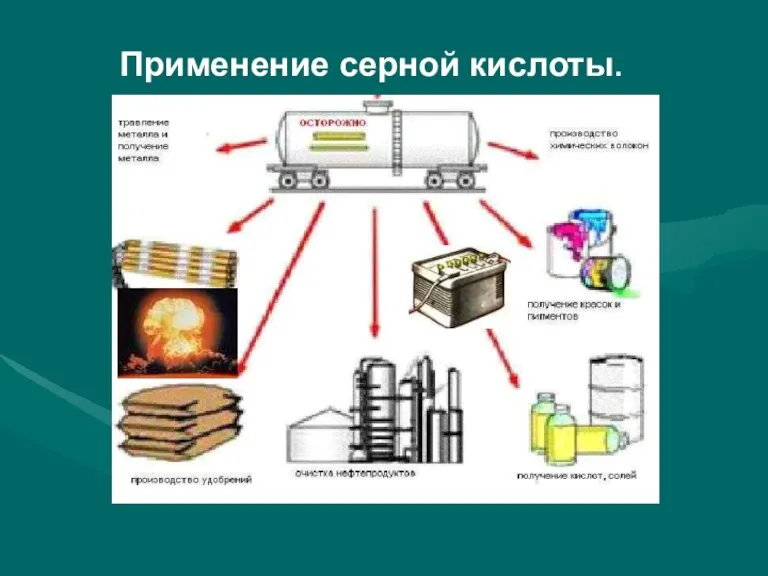
- 18. Применение серной кислоты.
- 19. Сульфат меди
- 20. Сульфат натрия.
- 21. Сульфат натрия.
- 22. СОЛИ СЕРНОЙ КИСЛОТЫ CaSO4• 2H2O - гипс CaSO4• 0,5H2O - алебастр CuSO4• 5H2O – медный купорос
- 23. Домашнее задание Составьте инструкцию по правилам обращения с серной кислотой • для лаборанта кабинета химии; •
- 24. Лабораторный опыт № 7 Исследование химических свойств раствора серной кислоты ВНИМАНИЕ ! При работе с кислотой
- 25. В пробирках в виде растворов представлены вещества: NaCl, NaBr, NaI, NaF, H2SO4, Na2CO3, Na2SO4, NaOH Предложите
- 26. Если эти утверждения верны на Ваш взгляд, то напротив них поставьте знак «+», а если нет,
- 28. Скачать презентацию























 Исследование в области естественных наук
Исследование в области естественных наук Домашнее задание: По прямой движется материальная точка, скорость её движения в момент времени t задаётся формулой =gt.Найти закон
Домашнее задание: По прямой движется материальная точка, скорость её движения в момент времени t задаётся формулой =gt.Найти закон  Государственные символы. Флаг РБ
Государственные символы. Флаг РБ Почему это так называется? Жилища на Руси. Проект по Родному языку
Почему это так называется? Жилища на Руси. Проект по Родному языку Солнечная система, ее состав
Солнечная система, ее состав Всемирная компьютерная сеть Интернет
Всемирная компьютерная сеть Интернет Sample letters
Sample letters  Прямая
Прямая Product Placement в клипах
Product Placement в клипах Собаки нужны людям.Потрясающая острота органов чувств и высокоразвитое социальное поведение позволили им стать незаменимыми пом
Собаки нужны людям.Потрясающая острота органов чувств и высокоразвитое социальное поведение позволили им стать незаменимыми пом Проблема компенсации в специальной психологии
Проблема компенсации в специальной психологии На догоспитальном этапе целесообразно разделить все нарушения ритма
На догоспитальном этапе целесообразно разделить все нарушения ритма Сражения Великой Отечественной войны 1941—1942 гг
Сражения Великой Отечественной войны 1941—1942 гг РЕТРО FM – уникальный продукт
РЕТРО FM – уникальный продукт Презентация на тему Объёмы геометрических тел
Презентация на тему Объёмы геометрических тел  Romeo and Juliet
Romeo and Juliet Презентация офисного зданияг. Москва, Трубниковский переулок, д. 22, стр. 2.
Презентация офисного зданияг. Москва, Трубниковский переулок, д. 22, стр. 2. Management public
Management public http://kamusic.ru/search/шум%20моря /
http://kamusic.ru/search/шум%20моря / Экспертиза ценности документа
Экспертиза ценности документа НАЙДИ
НАЙДИ Современный урок – урок актуальный для настоящего времени
Современный урок – урок актуальный для настоящего времени Это у нас, это гордость Вятки
Это у нас, это гордость Вятки От истоков до наших дней … И в будущее?
От истоков до наших дней … И в будущее? Презентация на тему Алматинский государственный природный заповедник
Презентация на тему Алматинский государственный природный заповедник  The world of my hobbies
The world of my hobbies Гражданское общество и государство: как добиться своего? Ликбез по теории ненасильственного сопротивления
Гражданское общество и государство: как добиться своего? Ликбез по теории ненасильственного сопротивления Презентация на тему Космодромы Байконур Плесецк Восточный
Презентация на тему Космодромы Байконур Плесецк Восточный