Содержание
- 2. Коррозия - проблема XXI века! Коррозия – рыжая крыса, Грызет металлический лом. В. Шефнер
- 3. Наша гипотеза: можно ли замедлить процесс коррозии, изучив скорость ее протекания в различных средах и на
- 4. Цель: изучить в различных средах протекание коррозии за определенный промежуток времени. Задачи: Найти информацию о коррозии
- 5. Теоретический этап исследования Коррозия – это процесс самопроизвольного разрушения металла под действием окружающей среды.
- 6. Что же вызывает коррозию??? Вода; Кислород; Оксиды углерода и серы, содержащиеся в воздухе; Водные растворы солей.
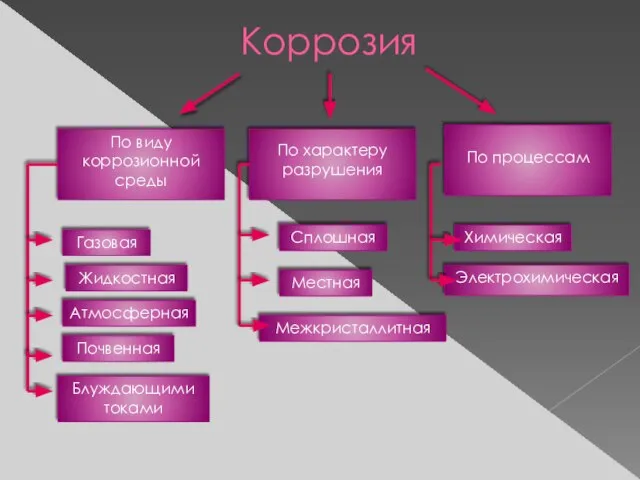
- 7. По виду коррозионной среды По характеру разрушения По процессам Газовая Жидкостная Атмосферная Почвенная Сплошная Местная Химическая
- 8. Химическая коррозия Компоненты окружающей среды окисляют непосредственно металл. Протекающие при химической коррозии окислительно - восстановительные реакции
- 9. Электрохимическая коррозия Коррозия протекающая в токопроводящей среде. Помимо химической реакции, в системе возникает электрический ток. Процесс
- 10. Скорость коррозии Факторы, влияющие на нее: наличием на поверхности фазовых и адсорбционных пленок влаги; загрязненностью воздуха
- 11. Практический этап исследования Вот и мы решили проверить, за сколько времени пройдёт процесс коррозии, и как
- 12. Постановка опыта Взяли 5 стаканов с водой и в каждый положили железный гвоздь. 1-й стакан контрольный;
- 13. Начало исследования. Через каждые 5 дней мы проверяли и записывали результаты. За это время стаканы и
- 14. Фото итог
- 15. Итак: Мы убедились на опыте, что на скорость протекания коррозии железа можно повлиять. Раствор щелочи ингибирует
- 16. Способы защиты от коррозии Нанесение защитных покрытий. Использование нержавеющих сталей. Введение в рабочую среду ингибиторов коррозии.
- 17. В заключении, хотим отметить, коррозия – главная проблема человечества связанная с металлами, она несёт очень большие
- 18. Спасибо за внимание!!! Проект подготовили ученики 9 класса МБОУ СОШ п.Дружба: Азаренко Елена Бурикова Кристина Барабанова
- 20. Скачать презентацию
















 Христианский православный храм
Христианский православный храм «Если каждый человекна кусочке своей землисделал бы всё, что он может,как прекрасна была бы земля наша!» А.П.Чехов.
«Если каждый человекна кусочке своей землисделал бы всё, что он может,как прекрасна была бы земля наша!» А.П.Чехов. Собрание по практике. Аттестационный лист
Собрание по практике. Аттестационный лист Осень в творчестве А.С.Пушкина
Осень в творчестве А.С.Пушкина Презентация на тему Население Бурятии
Презентация на тему Население Бурятии  Алёхин Александр Викторович(учитель физкультуры)
Алёхин Александр Викторович(учитель физкультуры) ACUTE CHOLECYSTITIS
ACUTE CHOLECYSTITIS  Рококо как стиль
Рококо как стиль Организационное поведение и управление персоналом
Организационное поведение и управление персоналом Станция «Детская библиотека»
Станция «Детская библиотека» Команда Набат, г. Бурмакино
Команда Набат, г. Бурмакино Думать глобально - действовать локально! Школа социального проектирования
Думать глобально - действовать локально! Школа социального проектирования Презентация Молодежной партии республики 1840.
Презентация Молодежной партии республики 1840. Card 0c аудиозаписи 1, 4) (1)
Card 0c аудиозаписи 1, 4) (1) AustroISOL, AustroPUR. Розробка, виробництво попередньо ізольованих труб
AustroISOL, AustroPUR. Розробка, виробництво попередньо ізольованих труб Transportation
Transportation «РАЗВИТИЕ МЕЖКУЛЬТУРНОЙ КОММУНИКАЦИИ УЧАЩИХСЯ ПОЛИЭТНИЧЕСКИХ КЛАССОВ В ПРОЦЕССЕ ШКОЛЬНОГО ФИЛОЛОГИЧЕСКОГО ОБРАЗОВАНИЯ»
«РАЗВИТИЕ МЕЖКУЛЬТУРНОЙ КОММУНИКАЦИИ УЧАЩИХСЯ ПОЛИЭТНИЧЕСКИХ КЛАССОВ В ПРОЦЕССЕ ШКОЛЬНОГО ФИЛОЛОГИЧЕСКОГО ОБРАЗОВАНИЯ» Изображение и реальность. И. Шишкин
Изображение и реальность. И. Шишкин Перспективная кадровая потребность по ключевым секторам экономики Тверской области
Перспективная кадровая потребность по ключевым секторам экономики Тверской области Презентация на тему Быт и нравы Древней Руси (6 класс)
Презентация на тему Быт и нравы Древней Руси (6 класс) Презентация на тему Объект и диагностический инструментарий мониторинга результативности освоения детьми ООП дошкольного образ
Презентация на тему Объект и диагностический инструментарий мониторинга результативности освоения детьми ООП дошкольного образ Кемлянская средняя школа
Кемлянская средняя школа Вопросы сокращения выбросов метана и глобальная климатическая повестка дня
Вопросы сокращения выбросов метана и глобальная климатическая повестка дня Использование ИКТ в работе с дошкольниками
Использование ИКТ в работе с дошкольниками Модерн в Казани
Модерн в Казани Особенности аварий на АЭС
Особенности аварий на АЭС Хацоцрот - еврейский музыкальный инструмент. Изготовление
Хацоцрот - еврейский музыкальный инструмент. Изготовление «Анализ подпрограммы «Обеспечение жильем молодых семей» ФЦП «Жилище» на 2011-2015 гг.» и Республиканской программы на 2011-2015 гг. У.Киль
«Анализ подпрограммы «Обеспечение жильем молодых семей» ФЦП «Жилище» на 2011-2015 гг.» и Республиканской программы на 2011-2015 гг. У.Киль