Содержание
- 2. 19.02.1859 г. – 02.10.1927 г. Сванте Аррениус Шведский ученый, лауреат Нобелевской премии мира по химии в
- 3. Основные положения ТЭД 1. При растворении в воде электролиты диссоциируют (распадаются) на положи-тельные и отрицательные ионы.
- 4. Обозначается (альфа) Измеряется в % (долях) - число частиц, распавшихся на ионы (диссоциированных) - общее число
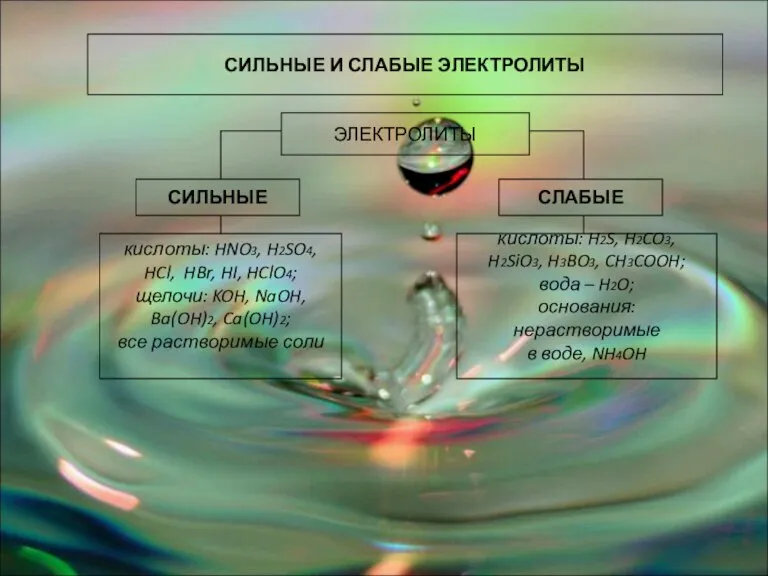
- 5. СИЛЬНЫЕ И СЛАБЫЕ ЭЛЕКТРОЛИТЫ ЭЛЕКТРОЛИТЫ СИЛЬНЫЕ СЛАБЫЕ кислоты: HNO3, H2SO4, HCl, HBr, HI, HClO4; щелочи: KOH,
- 6. Проверка знаний: Электролитическая диссоциация в растворах – это процесс распада электролита на __________ . Вопрос 1
- 7. Электролиз Электролиз — процесс, протекающий на электродах при прохождении электри-ческого тока через раствор либо расплав электролита.
- 8. Электролиз является одним из способов промышленного получения алюми-ния, водорода, хлора, хлорорганических соединений, диоксида марганца и др.
- 9. Законы Фарадея (22.09. 1791 — 25.08.1867)—англий-ский физик, химик, основоположник учения об электромагнитном поле.
- 10. Луиджи Гальвани (9.09.1737 — 4.12.1798) — итальянский врач и физик, один из основателей электрофизиологии и учения
- 11. Гальванический элемент — химический источник электрического тока, наз-ванный в честь Луиджи Гальвани. Принцип действия гальванического элемента
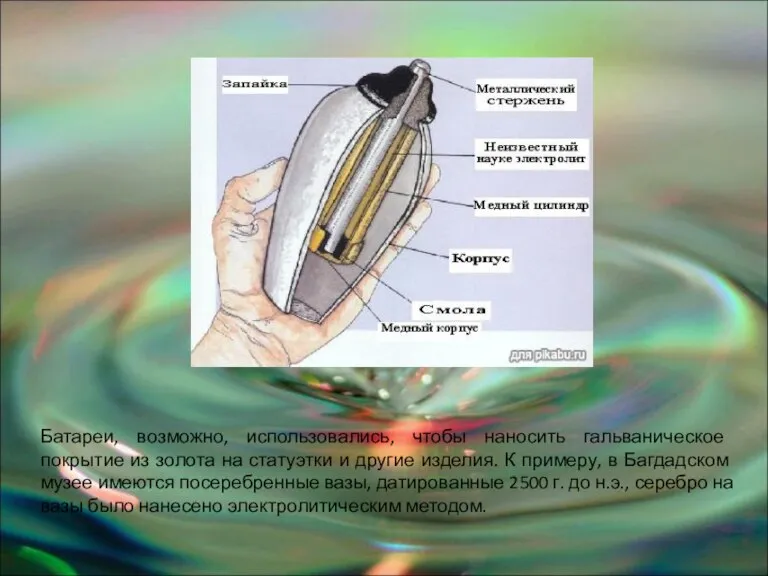
- 12. Багдадские батарейки Багдадские батарейки - ряд артефактов, найденных на территории Месопотамии, которые датируются первыми столетиями нашей
- 13. Батареи, возможно, использовались, чтобы наносить гальваническое покрытие из золота на статуэтки и другие изделия. К примеру,
- 14. Профессор Дж. Б. Перчински из Уни-верситета Север-ной Каролины соз-дал точную копию «батарейки» и на-полнил её пятипро-центным
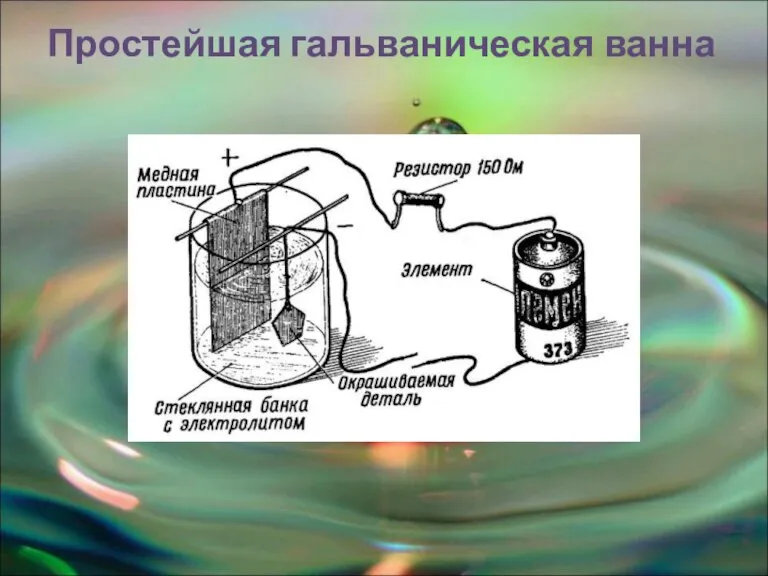
- 15. Простейшая гальваническая ванна
- 16. Гальваника
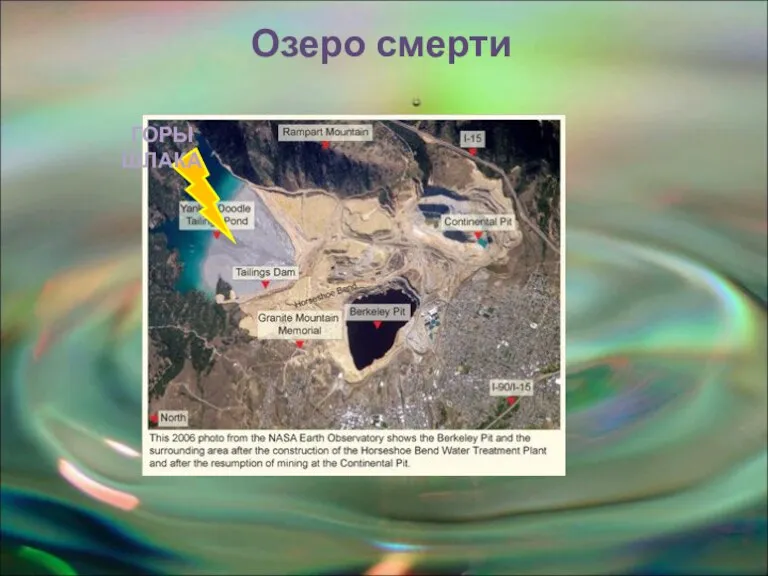
- 17. . ГОРЫ ШЛАКА Озеро смерти
- 18. Медь, кислоты, цинк, мышьяк - самая ядо-витая часть таблицы Менделеева сосредо-точена в одном месте. И это
- 19. При соприкосновении воды с срезами скальных пород в заброшенной шахте про-изошла цепь химических реакций, и при
- 21. Скачать презентацию














 Украина
Украина  Buckingham Palace
Buckingham Palace Бизнес-планированиеЗанятие 4
Бизнес-планированиеЗанятие 4 Интеллектуальная электроэнергетика
Интеллектуальная электроэнергетика Поработайте над содержанием презентации:
Поработайте над содержанием презентации: Санкт-Петербургский технический колледж управления и коммерции СПб ТКУиК
Санкт-Петербургский технический колледж управления и коммерции СПб ТКУиК Культура Византии
Культура Византии Презентация на тему Обоняние и вкус
Презентация на тему Обоняние и вкус История создания романа Ф.М. Достоевского «Преступление и наказание»
История создания романа Ф.М. Достоевского «Преступление и наказание» Повторение пунктуации сложного предложения. Знаки препинания в БСП
Повторение пунктуации сложного предложения. Знаки препинания в БСП Представление
Представление Вступительный экзамен в СНК “Эскулап”
Вступительный экзамен в СНК “Эскулап” Цветок — Нарцисс
Цветок — Нарцисс Охрана здоровья и безопасностьИТОГИ 2008 годаОАО «АрселорМиттал Кривой Рог», Украина
Охрана здоровья и безопасностьИТОГИ 2008 годаОАО «АрселорМиттал Кривой Рог», Украина Фотоматериалы с мастер – класса по теме «Урок-соревнование, как тип урока с использованием игровых технологий при проведении тема
Фотоматериалы с мастер – класса по теме «Урок-соревнование, как тип урока с использованием игровых технологий при проведении тема 1254663
1254663 Теория и история религий
Теория и история религий 4. СОУЭ 2020
4. СОУЭ 2020 Загадки и чудеса Рафаэля
Загадки и чудеса Рафаэля Системы счисления
Системы счисления Второй год обучения. Весенний семестр.Тема: «Организация витрины и входа в магазин»
Второй год обучения. Весенний семестр.Тема: «Организация витрины и входа в магазин» Порядок осуществления эмиссии и обращения государственных и муниципальных ценных бумаг
Порядок осуществления эмиссии и обращения государственных и муниципальных ценных бумаг Семейный ужин
Семейный ужин Выносливость и её развитие
Выносливость и её развитие Общие должностные и специальные обязанности военнослужащих
Общие должностные и специальные обязанности военнослужащих Дворовый спорт в Заречье
Дворовый спорт в Заречье Раневые инфекции
Раневые инфекции Эволюция телефонной связи
Эволюция телефонной связи