Слайд 4Топливные элементы – междисциплинарная проблема
Электрохимия
Мембранный транспорт
Катализ
Материаловедение
Инжениринг и проблемы энергетики

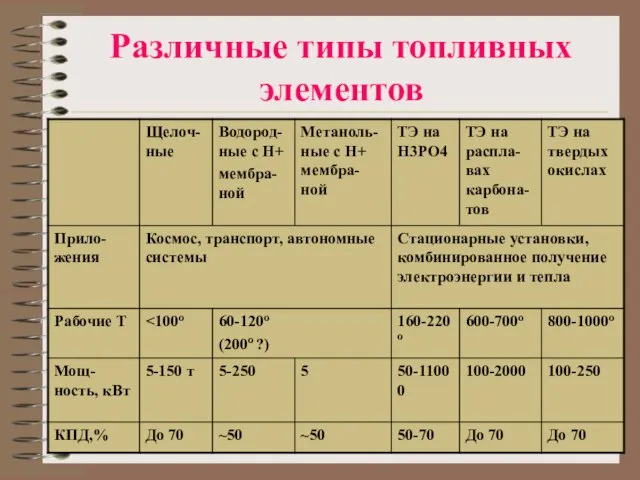
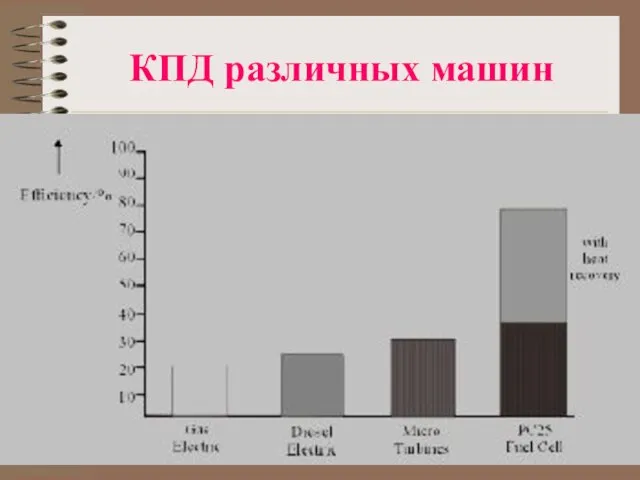
Слайд 7Различные типы топливных элементов
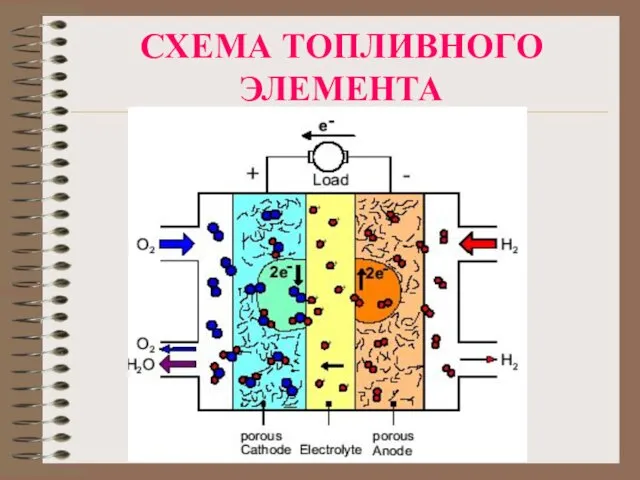
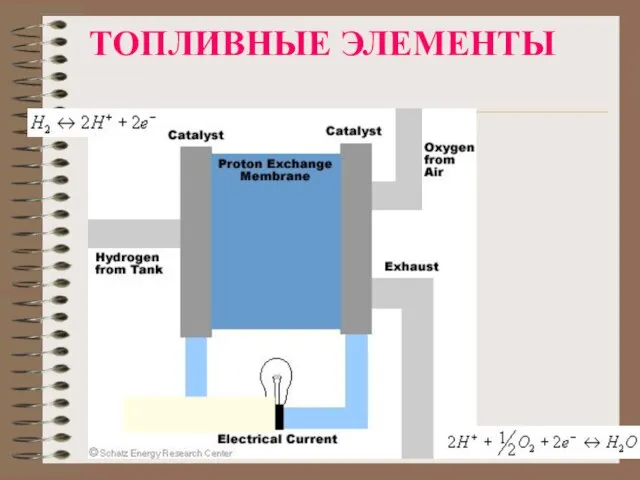
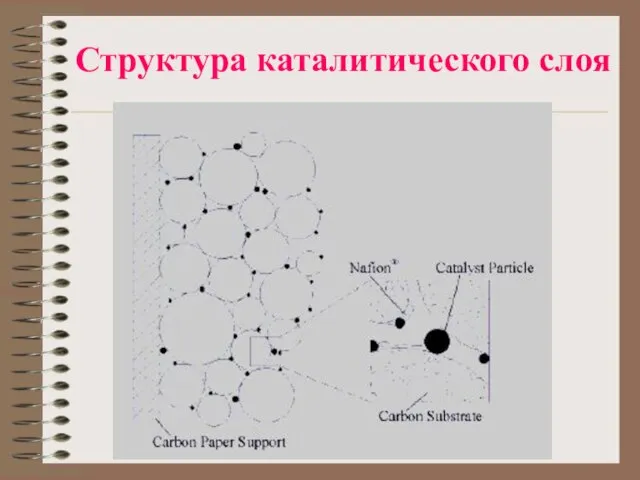
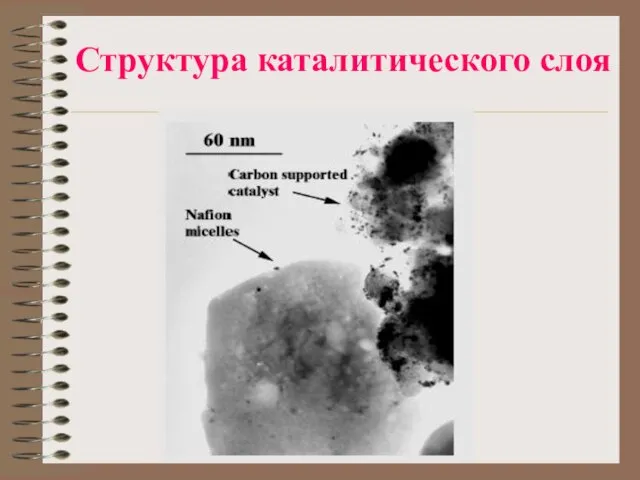
Слайд 9Водородные ТЭ с Н+ проводящей мембраной

Слайд 10Метанольные ТЭ с Н+ проводящей мембраной

Слайд 14Требования к мембранам
Низкая стоимость (<10$/кВт)
Высокая протонная проводимость
Хорошие барьерные свойства (Н2,О2, МеОН)
Термическая

и химическая стабильность: >120-150oC, >10000 час
Механическая стабильность
Электроизолирующие свойства
Слайд 16Мембрана сулфонилимида (более проводящая чем Nafion)

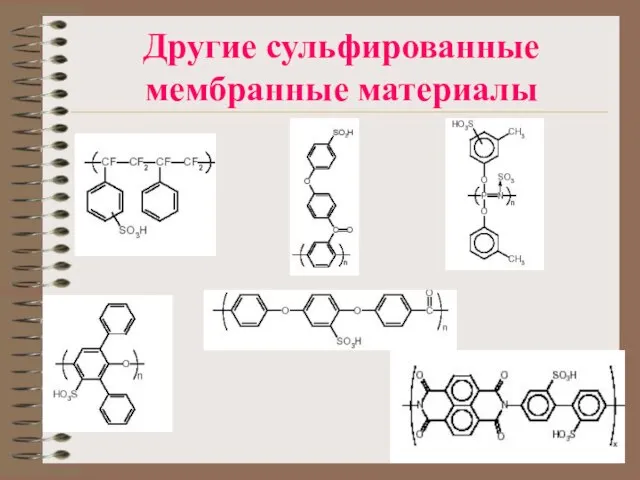
Слайд 18Другие сульфированные мембранные материалы
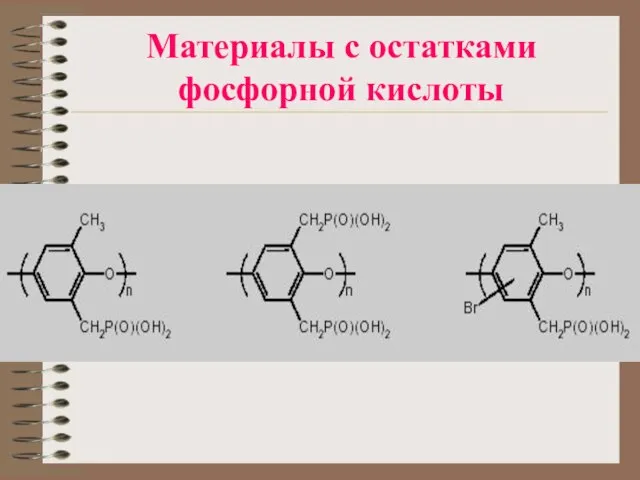
Слайд 19Материалы с остатками фосфорной кислоты
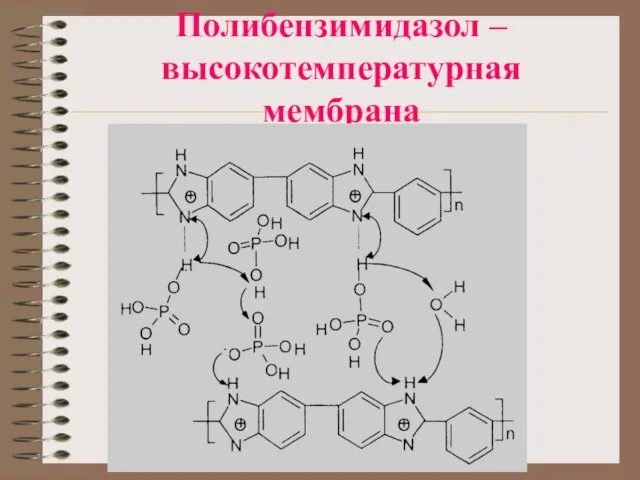
Слайд 20Полибензимидазол – высокотемпературная мембрана
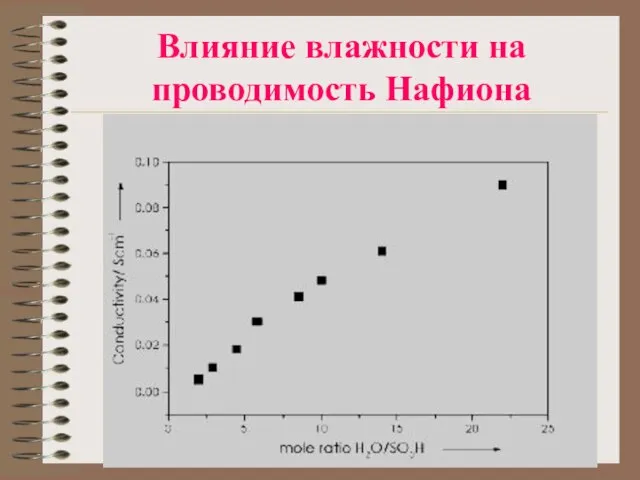
Слайд 23Влияние влажности на проводимость Нафиона
Слайд 26Водные проблемы
(water management)
Состояние воды в мембране:
сольватация –SO3H групп
сольватация Н+
«объемная» воды
Дегидратация:
“асимметрия” образования воды;
температурный

режим (<100oC);
возможное влияние на мех. стабильность
Увлажнение:
роль кроссовера;
“заливание” пор в электроде.
Слайд 28Методы получения водорода
(ископаемые топлива)
Паровая конверсия природного газа:
CH4 + H2O CO +

3H2
CO + H2O = CO2 + H2
Каталитический риформинг
C6H14 C6H6 + 4H2
Пиролиз
CnHm C2H4 + H2
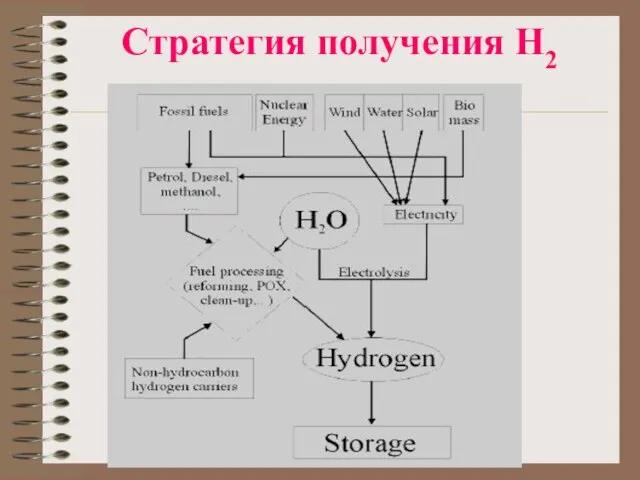
Слайд 29Альтернативные методы получения водорода
Электролиз
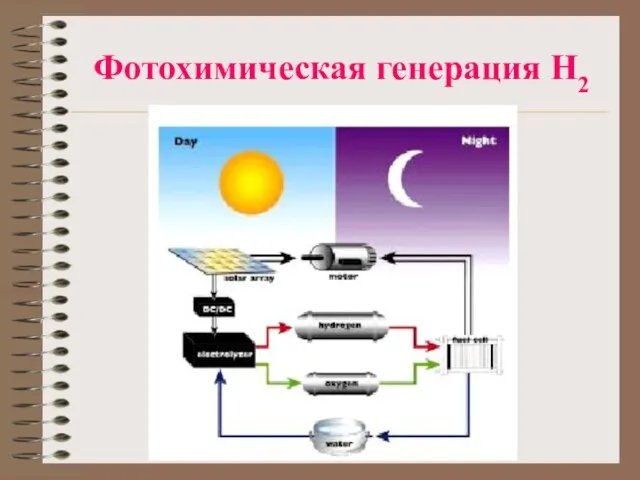
Фотолиз воды
Высокотемпературные ядерные (Не) реактора

Слайд 30Термохимический цикл в Не ядерном реакторе
Источник энергии – Не (1000оС)
2H2О + SO2

+ J2 H2SO4 + 2HJ (при 900о)
2HJ J2 + H2 (при 450оС)
H2SO4 + SO2 + H2O + 1/2O2 (при 850oC)
Слайд 32Методы очистки водорода
Мембраны:
Pd
полимерные мембраны
Химические:
дожигание: СО + 1/2O2 CO2
реакция водяного пара: CO

+ H2O = CO2 + H2
метанирование: СO + 3H2 CH4 + H2O
Адсорбционные
Слайд 33Хранение водорода
Газовые баллоны (0,5 кг Н2)
Жидкий водород (-253оС, теплопотери)
Гидрирды металлов, нано-трубки и

т.п.
Химические источники Н2:
СН3ОН, СН4, НС, биомасса.
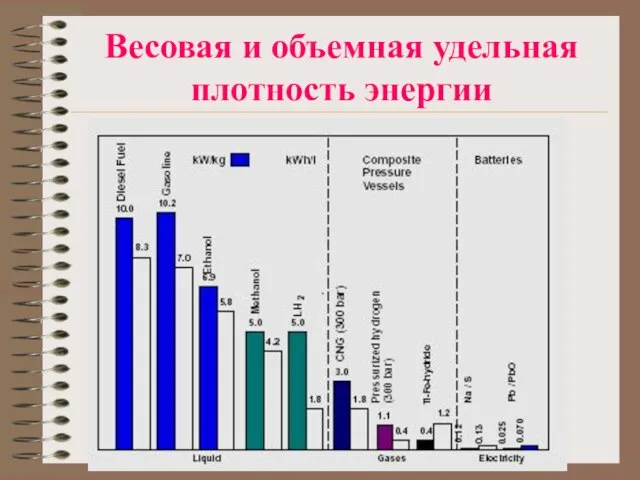
Слайд 34Весовая и объемная удельная плотность энергии























 Презентация на тему Политика и власть
Презентация на тему Политика и власть  6. СВН 2020
6. СВН 2020 The structure of the body
The structure of the body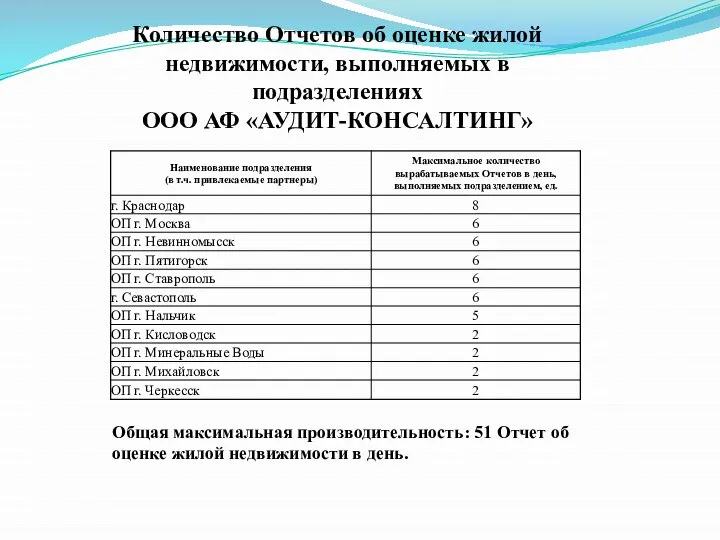 Количество Отчетов об оценке жилой недвижимости, выполняемых в подразделениях ООО АФ АУДИТ-КОНСАЛТИНГ
Количество Отчетов об оценке жилой недвижимости, выполняемых в подразделениях ООО АФ АУДИТ-КОНСАЛТИНГ УПРАВЛЕНЧЕСКИЙКОНСАЛТИНГ
УПРАВЛЕНЧЕСКИЙКОНСАЛТИНГ Презентация на тему орган зрения
Презентация на тему орган зрения Metodiki_yur_AKZS
Metodiki_yur_AKZS Пушкинская карта
Пушкинская карта Мой милый маг, моя Мария, - Мечтам мерцающий маяк. Мятежны марева морские, Мой милый маг, моя Мария, Молчаньем манит мутный мрак … Мне
Мой милый маг, моя Мария, - Мечтам мерцающий маяк. Мятежны марева морские, Мой милый маг, моя Мария, Молчаньем манит мутный мрак … Мне 3 года младший дошкольник
3 года младший дошкольник Правовая защита экологии в Беларуси
Правовая защита экологии в Беларуси Хирургическое_лечение_преждевременной_эякуляции
Хирургическое_лечение_преждевременной_эякуляции Столетие бедствий
Столетие бедствий Памятка по прямым выплатам ФСС
Памятка по прямым выплатам ФСС «Конституция –основной законгосударства»
«Конституция –основной законгосударства» Замечания заказчика
Замечания заказчика Презентация на тему Реализация ФГОС в работе школьной библиотеки. Воспитание культурного и гражданского самосознания учащихся.
Презентация на тему Реализация ФГОС в работе школьной библиотеки. Воспитание культурного и гражданского самосознания учащихся. Характерные особенности тактической подготовки баскетболистов при игре в защите
Характерные особенности тактической подготовки баскетболистов при игре в защите Презентация на тему Великий круговорот жизни 3 класс
Презентация на тему Великий круговорот жизни 3 класс (005)Pulser Test Form
(005)Pulser Test Form Культурные и сорные растения поля
Культурные и сорные растения поля Устное народное творчество Урала.
Устное народное творчество Урала. Презентация на тему Евглена Зеленая
Презентация на тему Евглена Зеленая  Протолитическая теория кислот и оснований
Протолитическая теория кислот и оснований Землетрясения Подготовила презентацию студентка 1ого курса ЭФ Группы Э112Б Олефир Карина
Землетрясения Подготовила презентацию студентка 1ого курса ЭФ Группы Э112Б Олефир Карина Apģērbs. Apģērba materiāli
Apģērbs. Apģērba materiāli Евгений Гришковец
Евгений Гришковец Вахта памяти в канун 74-й годовщины великой победы
Вахта памяти в канун 74-й годовщины великой победы