Слайд 3Даниель Резерфорд (Рутерфорд)
Получил образование в Эдинбургском университете, где и получил степень

доктора в 1772 году за работу под названием «De aëre mephitica», в которой описывал новый газ, около того же времени открытый независимо Д. Пристли и получивший название азота.
Слайд 4Джозеф Пристли
В 1772 г. Пристли, действуя разбавленной азотной кислотой на медь,
впервые получил окись азота — «селитряный воздух» — и нашёл, что окись азота при соприкосновении с воздухом буреет вследствие образования двуокиси азота. Пользуясь для собирания газов ртутной ванной, Пристли в 1772—74 гг. впервые получил хлороводород — «соляно-кислый воздух» и аммиак — «щелочной воздух».
Слайд 5Антуа́н Лора́н Лавуазье́
Установив свой новый взгляд на процессы горения и окисления,

Лавуазье вместе с тем правильно понял состав воздуха. Путём анализа и синтеза он показал, что воздух есть смесь двух газов: один из них — есть газ, преимущественно поддерживающий горение, «здоровый (salubre) воздух, чистый воздух, жизненный воздух, кислород», как последовательно называл его сам Лавуазье, другой газ — нездоровый воздух (moffette) или азот.
Слайд 6Формы существования Азота
АЗОТ
АТОМ В
N0 ПРОСТОЕ СОСТАВЕ
ВЕЩЕСТВО СЛОЖНЫХ
N20 ВЕЩЕСТВ
N-3.........
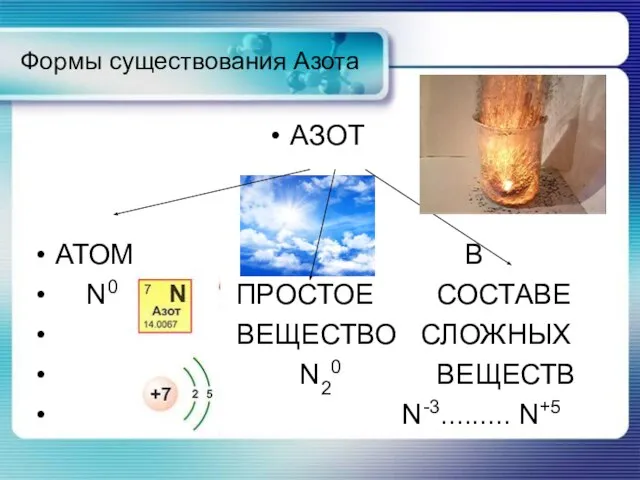
N+5
Слайд 7План урока
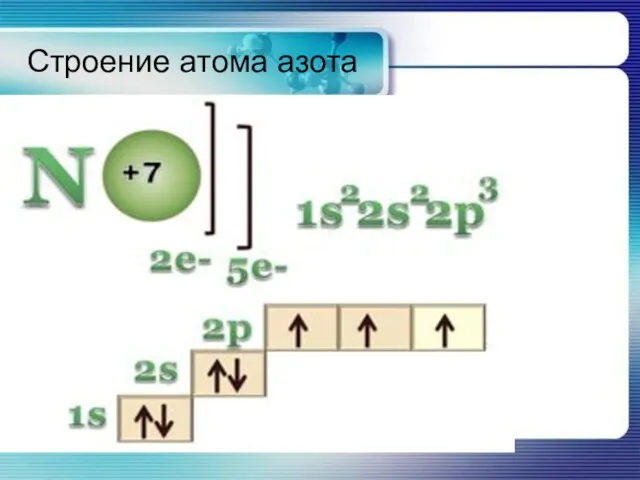
1. Строение атома азота.
2. Строение молекулы азота.
3. Физические свойства азота.
4.Химические свойства
азота.
5. Соединения азота.
6. Применение азота.
Слайд 9Возможные степени окисления азота

Слайд 10Покажите вещества, содержащие азот, в порядке увеличения степени окисления азота. Назовите вещества

Слайд 11Покажите вещества, содержащие азот, в порядке увеличения степени окисления азота. Назовите вещества

Слайд 12Покажите вещества, содержащие азот, в порядке увеличения степени окисления азота. Назовите вещества

Слайд 13Покажите вещества, содержащие азот, в порядке увеличения степени окисления азота. Назовите вещества

Слайд 14Покажите вещества, содержащие азот, в порядке увеличения степени окисления азота. Назовите вещества

Слайд 15Покажите вещества, содержащие азот, в порядке увеличения степени окисления азота. Назовите вещества

Слайд 16Покажите вещества, содержащие азот, в порядке увеличения степени окисления азота. Назовите вещества

Слайд 17Покажите вещества, содержащие азот, в порядке увеличения степени окисления азота. Назовите вещества

Слайд 20 Химические свойства
б) восстановительные свойства

Слайд 21Задача
30 г. Х кДж
N2 + O2 = 2NO - Q
60
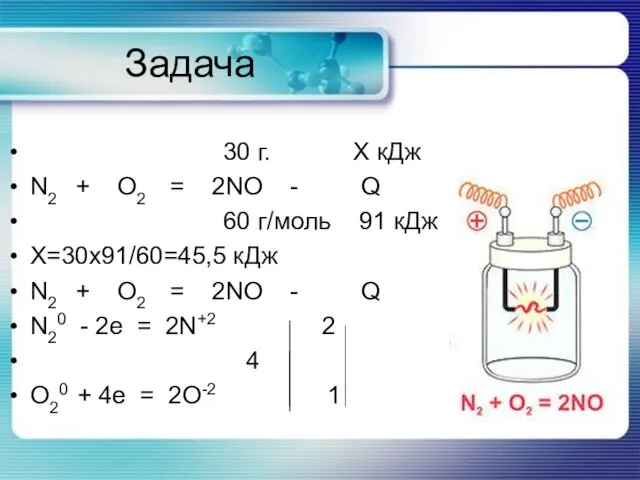
г/моль 91 кДж
Х=30х91/60=45,5 кДж
N2 + O2 = 2NO - Q
N20 - 2e = 2N+2 2
4
O20 + 4e = 2O-2 1
Слайд 22Химические свойства
а) окислительные свойства

Слайд 23Анри Луи Ле Шателье
В 1884 г. Ле Шателье сформулировал принцип динамического равновесия,

ныне носящий его имя (независимо от Ле Шателье этот принцип сформулировал в 1887 г. К. Ф. Браун). Согласно этому принципу, система, находящаяся в состоянии устойчивого химического равновесия, при внешнем воздействии (изменении температуры, давления, концентрации реагирующих веществ и т. д.) стремится вернуться в состояние равновесия, компенсируя оказанное воздействие
Слайд 24Смещение химического равновесия
N2+3H2 2NH3+ Q
1V +3V 2V
T -Q
P V
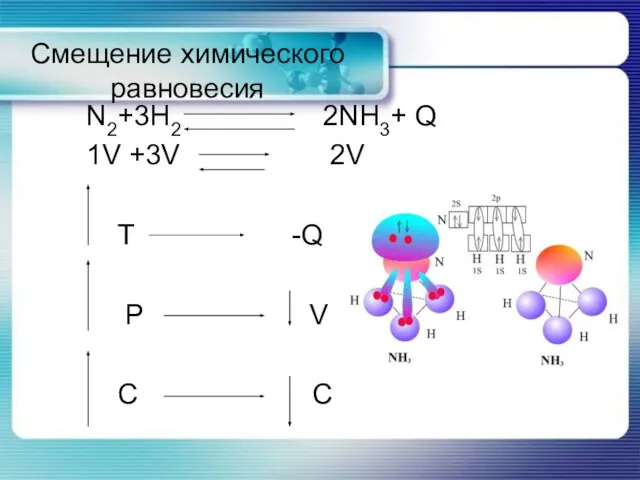
C C
Слайд 25Получение азота
а) в промышленности
б) в лаборатории

Слайд 27Жак-Ив Кусто́
Французский исследователь жизни моря исследовал в процессе тренировочных погружений состояние

азотного наркоза
Слайд 28Итоги урока:
ВЫСКАЖИТЕ АРГУМЕНТЫ В ПОЛЬЗУ КАЖДОЙ ВЕРСИИ:
АЗОТ- «БЕЗЖИЗНЕННЫЙ»?
АЗОТ-ГЛАВНЫЙ ЭЛЕМЕНТ ЖИЗНИ НА ЗЕМЛЕ?

Слайд 29Домашнее задание
Доработать конспект, используя материал учебника;
Решить задачу из информативной карты;
Составить уравнения реакций

взаимодействия азота с металлами магнием. алюминием;. Расставив коэффициенты методом электронного баланса.




























 Технология саморазвития личности (ТСРЛ)А.А. Ухтомского- Г.К. Селевков призме ФГОС второго поколения
Технология саморазвития личности (ТСРЛ)А.А. Ухтомского- Г.К. Селевков призме ФГОС второго поколения Московский областной гуманитарный институт
Московский областной гуманитарный институт Анализ государственной программы«Развитие здравоохранения в Российской Федерации»
Анализ государственной программы«Развитие здравоохранения в Российской Федерации» Навигатор дополнительного образования. Памятка как зарегистрироваться и получить именной сертификат
Навигатор дополнительного образования. Памятка как зарегистрироваться и получить именной сертификат Окружные ресурсные центры (ОРЦ) реализации и мониторинга региональных программ совершенствования питания в образовательных учре
Окружные ресурсные центры (ОРЦ) реализации и мониторинга региональных программ совершенствования питания в образовательных учре Отбытие поезда, проект фильма
Отбытие поезда, проект фильма Жозефина Ильинична Шиф
Жозефина Ильинична Шиф Иррациональные числа
Иррациональные числа История развития геометрии
История развития геометрии Презентация на тему Биологические и антропогенные факторы
Презентация на тему Биологические и антропогенные факторы  Календарь ролевых полевых игр по Дж.Р.Р. Толкиену
Календарь ролевых полевых игр по Дж.Р.Р. Толкиену Сложение и вычитание десятичных дробей.
Сложение и вычитание десятичных дробей. Развитие пространственного мышления на уроках географии
Развитие пространственного мышления на уроках географии Презентація
Презентація Мы за здоровый образ жизни!
Мы за здоровый образ жизни! Гармония в себе. Фотоальбом
Гармония в себе. Фотоальбом П Р О Е К Т Н А Я Р А Б О Т А «Почему у кошки светятся глаза?» ученицы 2 класса «Б» Дружининой Анастасии Научный руководитель: Сафро
П Р О Е К Т Н А Я Р А Б О Т А «Почему у кошки светятся глаза?» ученицы 2 класса «Б» Дружининой Анастасии Научный руководитель: Сафро Образовательный кредит СберБанка с государственной поддержкой
Образовательный кредит СберБанка с государственной поддержкой Социальное неравенство
Социальное неравенство Предложение по размещению рекламы в фитнес-клубах
Предложение по размещению рекламы в фитнес-клубах Школьное самоуправление: «Игра в демократию» или участие в школьной политике?
Школьное самоуправление: «Игра в демократию» или участие в школьной политике? Подростковый возраст и его особенности
Подростковый возраст и его особенности Преддипломная практика. Психологическая помощь в стрессовых ситуациях у педагогических работников
Преддипломная практика. Психологическая помощь в стрессовых ситуациях у педагогических работников Россия на мировом рынке технологий
Россия на мировом рынке технологий Итальянское Возрождение 6 класс
Итальянское Возрождение 6 класс Ēdināšanas uzņēmuma aprīkojums
Ēdināšanas uzņēmuma aprīkojums Частица как служебная часть речи
Частица как служебная часть речи Первопроходцы космоса
Первопроходцы космоса