Содержание
- 2. Биогенные элементы -элементы, необходимые организму для построения и жизнедеятельности клеток и органов
- 3. Классификация биогенных химических элементов
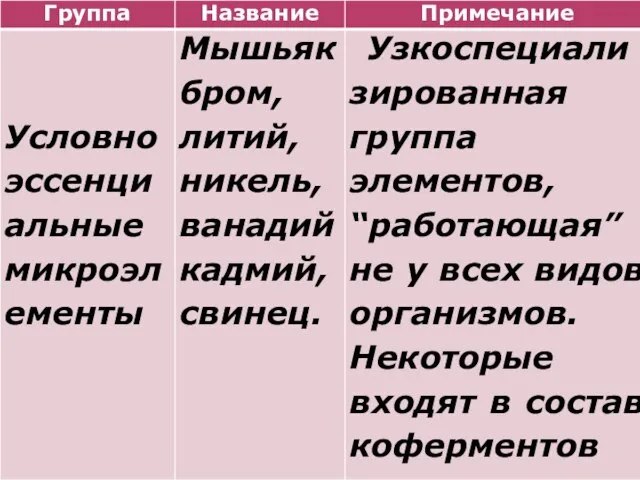
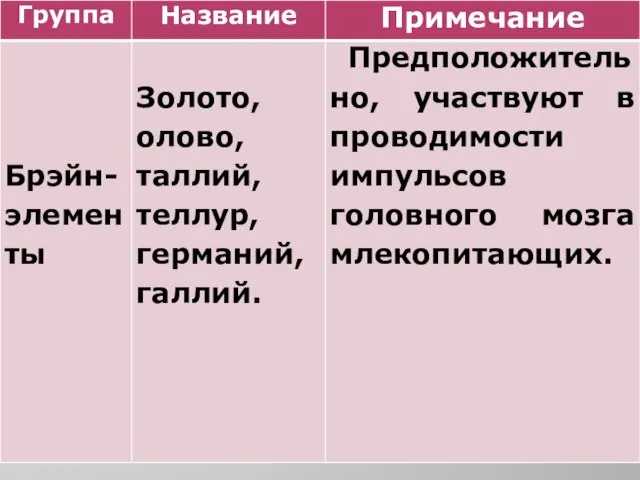
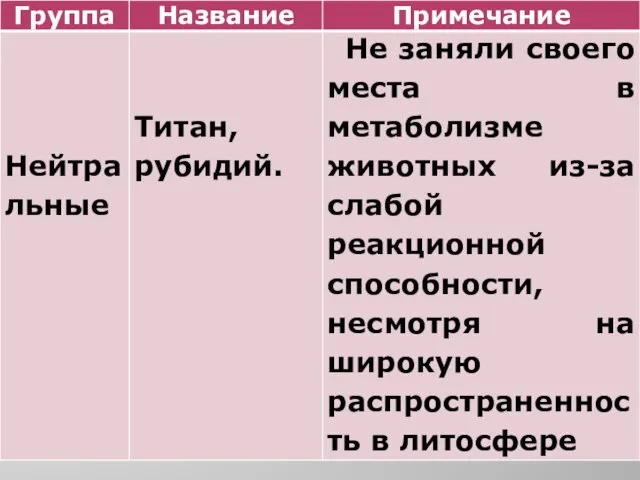
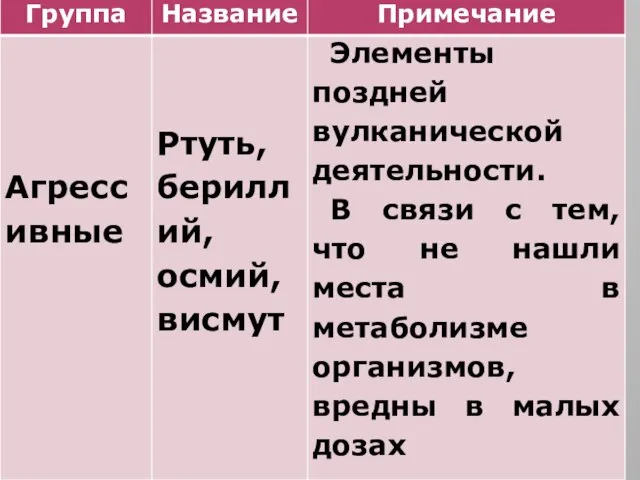
- 9. Классификация абиогенных химических элементов
- 13. Элементы в природе и организме Академик В. Вернадский писал: «Для понимания сложнейших жизненных процессов их надо
- 14. На основании анализа горных пород установлено, что в биосферу (лито-, гидро- и атмосферу) входят около 90
- 15. Структурные образования живой клетки включают в себя всего 6 биогенных элементов: С, Н, О, N, P,
- 16. По В. Вернадскому, средний химический состав человека включает примерно 80 элементов, из них макроэлементы: О, С,
- 17. Больше всего в организме легких элементов. Возрастание атомной массы в ПСЭ увеличивает токсичность элементов и снижает
- 18. В. Ковальский создал раздел биологии- геохимическую экологию, изучающую взаимоотношения организма с окружающей средой. Геохимическая экология изучает
- 19. Однако часть организмов (5 – 20 %) в этих условиях заболевают. Например, жители горных районов часто
- 20. Отдельные элементы, которые характеризуются небольшим содержанием, концентрируются в определенных частях организма. Так, значительно содержание Сu -
- 21. Биологическая роль химических элементов в организме Биологическая роль элементов в организме человека чрезвычайно разнообразна. Главная функция
- 22. Микроэлементы, входят в состав ферментов, гормонов, витаминов, биологически активных веществ в качестве комплексообразователей (активаторов), участвуют в
- 23. Содержание некоторых элементов в организме человека меняется с возрастом. Так, содержание Cd в почках и Мо
- 24. Кроме шести основных макроэлементов (С, Н, О, N, P, S) из которых состоят углеводы, жиры, белки
- 25. Недостаток и избыток элементов в организме одинаково вреден. Ряд элементов (Ag, Hg, Pb, Cd и др.)
- 26. s-элементы s-Элементы - это элементы, у атомов которых электронами заселяются s-подуровни внешнего уровня. Сокращенная электронная формула
- 27. Свойства s-элементов Легко отдают валентные s-электроны, проявляя сильные восстановительные свойства. Типичные металлы, обладают блеском, высокой электрической
- 28. Как правило, образуют соединения с ионным типом связи, исключение составляет водород, для которого наиболее характерна ковалентная
- 29. Водород в виде соединений (белки, жиры, углеводы и др.) входят в состав всех организмов. Он отвечает
- 30. Вода - составная часть организма. У взрослых содержание её в организме составляет 60%, у детей эта
- 31. Вода поддерживает состояние кислотно-основного равновесия, а также осмотическое, гемодинамическое и термическое равновесие в организме. Вода используется
- 32. Бериллий постоянно находится в растениях и организме животных. Он является ультрамикроэлементом, содержание в организме ~ 10-7
- 33. Кальций относится к макроэлементам, содержание в организме 1,4%. Основная масса находится в костной и зубной тканях.
- 34. Барий Ва - микроэлемент, содержание в организме 10-5 %. Концентрируется, в основном, в сетчатке глаза. Биологическая
- 35. р-элементы р-Элементы - это элементы, у атомов которых происходит заполнение электронами р - подуровня внешнего уровня.
- 36. Свойства р-элементов В группах радиусы атомов и однотипных ионов, в общем, увеличиваются. Энергия ионизации при переходе
- 37. Свойства р-элементов В периодах слева направо атомные и ионные радиусы р - элементов по мере увеличения
- 38. IIIА - группа Бор относится к примесным микроэлементам, его массовая доля в организме человека составляет 10-5
- 39. Избыток В вреден для организма человека. В угнетает ферменты амилазы, протеиназы, уменьшает активность адреналина. Является необходимым
- 40. Алюминий А1 относится к примесным элементам (10-5 %). А1 концентрируется главным образом в сыворотке крови, легких,
- 41. Галлий Ga — примесный микроэлемент. Биологическая роль не установлена. Таллий Тl — весьма токсичный элемент.
- 42. IVA группа Углерод С. По содержанию в организме человека (21,15%) С относится к макроэлементам. Он входит
- 43. Кремний Si. По содержанию в организме человека Si относится к примесным микроэлементам. Больше всего Si в
- 44. В стоматологической практике применяют карборунд SiC для шлифовки пломб и пластмассовых протезов. SiO2 входит в состав
- 45. Германий Ge относится к микроэлементам, содержание в организме человека — 10-5 — 10-6 %. Биологическая роль
- 46. Олово. Sn по содержанию в организме человека (10-4%) относятся к микроэлементам. Сведения о биологической роли противоречивы.
- 47. Свинец. Рb и его соединения, особенно органические, весьма токсичны, Соединения Рb влияют на синтез белка, энергетический
- 48. VA – группа Азот N по содержанию в организме человека (3,1%) относится к макроэлементам. Этот элемент
- 49. Фосфор Р содержится в организме человека 0,95%. Р относится к макроэлементам. Это органоген и играет исключительно
- 50. Мышьяк As по содержанию в организме человека составляет 10-6 % и относится к микроэлементам. Он концентрируется
- 51. Сурьма Sb и висмут Bi. По содержанию в организме Sb и Bi (10-5 %) относятся к
- 52. VIA-группа Кислород O. По содержанию в организме человека (62%) О относится к макроэлементам. Он незаменим и
- 53. Большинство окислительно-восстановительных реакций в организме протекает при участии О и его активных форм. Фагоцитарные (защитные) функции
- 54. Озон О3 как очень сильный окислитель используют для дезинфекции помещений, обеззараживания воздуха, очистки питьевой воды. Сера
- 55. Образующаяся в организме эндогенная H2SO4 участвует в обезвреживании ядовитых соединений - фенола, крезола, индола, вырабатываемых в
- 56. Селен Se. По содержанию в организме ( 10-5 – 10-7 %) Se относится к микроэлементам. Se
- 57. Теллур Te и полоний Po. Те обнаружен в живых организмах. Норма его содержания в тканях и
- 58. VIIA - группа По содержанию в организме человека С1 (0,15%) относится к макроэлементам, остальные элементы этой
- 59. Фтор F. Масса F в организме человека составляет около 7 мг (~10-5 %). Соединения фтора концентрируются
- 60. Фторид-ион легко замещает гидроксид-ион в гидроксиапатите, образуя защитный эмалиевый слой более твердого фторапатита: Са10(РО4)6(ОН)2 + 2F-
- 61. Кариес зубов начинается на поврежденном участке эмали с появлением пятна. Под действием кислот, вырабатываемых бактериями, происходит
- 62. Обогащение питьевой воды F, то есть фторирование воды с целью доведения содержания в ней F до
- 63. Применение NaF основано на образовании фторапатита: 2NaF + Ca10(PO4)6(OH)2 = 2NaOH + Са10 (РО4)6F2 . При
- 64. Хлор Cl. В организме человека содержится примерно 0,15%. Хлорид-ионы играют важную биологическую роль. Они активируют некоторые
- 65. Хлорид-ион имеет оптимальный радиус для проникновения через мембрану клеток. Именно этим объясняется его совместное участие с
- 66. Бром Br. Масса брома в организме человека составляет около 10-5 %. Он локализуется преимущественно в железах
- 67. При введении в организм бромид-ионов наиболее чувствительной оказывается центральная нервная система. Бромид-ионы накапливаются в различных отделах
- 68. Бромид-ионы могут замещать ионы Сl- и I- в организме. Примером такого взаимозамещения является замещение йода бромом
- 69. Бромид-ионы легко всасываются в желудочно-кишечном тракте. Токсичность бромид-ионов невысока. Однако вследствие медленного выведения из организма (30-60
- 70. Йод I относится к числу незаменимых биогенных элементов. Его соединения играют важную роль в процессах обмена
- 71. Пониженная активность щитовидной железы (гипотиреоз) может быть связана с уменьшением её способности накапливать йодид-ионы, а также
- 72. d-элементы d-Элементы - это элементы, у атомов которых происходит заселение электронами d-подуровня второго снаружи уровня. К
- 73. Свойства d-элементов В периодах с увеличением заряда ядра возрастание радиуса атомов происходит медленно, непропорционально числу электронов,
- 74. Свойства d-элементов В результате экранирования этим слоем с увеличением номера элемента атомный радиус, энергия ионизации, а,
- 75. Свойства d-элементов Все атомы d-блока, за исключением группы I Б и II Б, имеют незавершенный d-подуровень.
- 76. Свойства d-элементов В растворах d-элементы с высшей степенью окисления представлены анионами, как правило, кислородсодержащими. При этом
- 77. Свойства d-элементов В периоде с увеличением заряда ядра уменьшается устойчивость соединений с высшей степенью окисления элементов.
- 78. 1Б группа Медь Cu является необходимым элементом растительных и животных организмов. В организме человека содержится около
- 79. Серебро Ag — микроэлемент растительных и животных организмов. В организме человека содержится -7,3 ммоль Ag. Концентрируется
- 80. Бионеорганические комплексы Ag с белками — протеинаты, представляют собой коллоидные растворы. Коллоидные препараты Ag не вызывают
- 81. Из соединений Ag наиболее известны протаргол (белковый комплекс Ag) и колларгол (коллоидное Ag). В небольшом количестве
- 82. II Б группа Цинк Zn, кадмий Cd, ртуть Hg - микроэлементы живых организмов. Zn содержится в
- 83. Cd и Hg обнаруживаются в печени и почках как примесные микроэлементы. Cd в виде белкового комплекса
- 84. Хром Cr, молибден Mo, вольфрам W являются микроэлементами живых организмов. Хром относится к биогенным элементам, содержащимся
- 85. Вольфрам как микроэлемент мало изучен, и как все тяжелые металлы не играет большой роли в живых
- 86. VII Б группа Марганец Мn, технеций Те, рений Re - элементы - аналоги, образующие VII Б-группу.
- 87. Марганец - один из десяти металлов жизни, является важным биогенным элементом. В органах и тканях взрослого
- 88. VIII Б группа Группу VIII Б составляют девять d-элементов: Fе, Co, Ni, Ru, Rh, Pd, Os,
- 89. Семейство железа Fe, Co, Ni, хотя и отличаются числом внешних электронов, тем не менее имеют близкие
- 90. И только небольшое увеличение электроотрицательности свидетельствует о том, что от Fe к Ni имеет место уменьшение
- 91. Железа Fe в организме человека содержится ~5 г. Большая часть его сосредоточена в гемоглобине крови (~
- 92. Одним из наиболее важных внутрикомплексных соединений является гемоглобин. Сложный по составу белок, содержащий и небелковую группу
- 93. Кобальт Со в роли микроэлемента выполняет разнообразные функции. В организме он представлен в виде витамина В12.
- 94. Семейство платины К семейству Pt относят шесть d-элементов VIII Б -группы. В природе они рассеяны и
- 95. В ПСЭ платиновые металлы расположены в V и VI периодах. У всех платиновых металлов при заполнении
- 96. Платиновые металлы VI периода вследствие лантаноидного сжатия имеют практически одинаковые радиусы, которые очень мало отличаются от
- 97. Относительно небольшие радиусы атомов и большая стабильность d-подуровня определяют низкую химическую активность платиновых металлов. В электрохимическом
- 99. Скачать презентацию




























































































 Спрос и предложение товаров
Спрос и предложение товаров 5. Гражданское общество
5. Гражданское общество Выполнение плана январь 2021
Выполнение плана январь 2021 Что такое информация. Виды информации
Что такое информация. Виды информации Информация о товарах. 8 класс
Информация о товарах. 8 класс Михайловский замок
Михайловский замок Из чаши мудрости испей
Из чаши мудрости испей Стихи о цветах
Стихи о цветах Первая мировая война
Первая мировая война Разработка электронного тренажера по интерактивной сборке ПК
Разработка электронного тренажера по интерактивной сборке ПК Школьный управляющий совет: смысл и структура Педагогический совет ГОУ СОШ 516 22.03.2011.
Школьный управляющий совет: смысл и структура Педагогический совет ГОУ СОШ 516 22.03.2011. О повышении энергоэффективности в Республике Беларусь
О повышении энергоэффективности в Республике Беларусь к успеху»
к успеху» Managementul strategic
Managementul strategic  Презентация на тему Компьютерные вирусы и антивирусные программы
Презентация на тему Компьютерные вирусы и антивирусные программы  Презентация на тему Растения степей
Презентация на тему Растения степей Создание резюме и его продвижение на сервисах по подбору сотрудников
Создание резюме и его продвижение на сервисах по подбору сотрудников Творческие работы
Творческие работы ЭОР
ЭОР Москва центр борьбы с ордынским игом
Москва центр борьбы с ордынским игом Билим Н.С._защита диплома
Билим Н.С._защита диплома Сказка
Сказка Бег на средние и длинные дистанции
Бег на средние и длинные дистанции 1 урок реал7 класс (1)
1 урок реал7 класс (1) Могу ли я отстоять свое мнение?
Могу ли я отстоять свое мнение? Органы управления. Правовые аспекты организации системы управления и определение компетенции органов управления
Органы управления. Правовые аспекты организации системы управления и определение компетенции органов управления Математика. Задачи
Математика. Задачи Духовное краеведение Подмосковья
Духовное краеведение Подмосковья