Слайд 2КОНКУРЕНТНОЕ И НЕКОНКУРЕНТНОЕ ИНГИБИРОВАНИЕ ФЕРМЕНТОВ
Схема неконкурентного ингибирования активности фермента
Схема конкурентного ингибирования активности
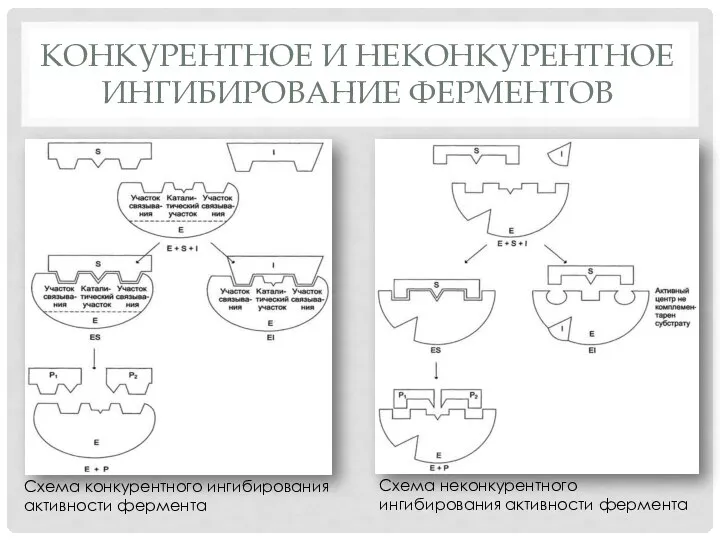
фермента
Слайд 3КОНКУРЕНТНОЕ ИНГИБИРОВАНИЕ
В этом случае ингибитор связывается в активном центре фермента и конкурирует
за него с субстратом. Таким образом, конкурентный ингибитор не связывается с фермент-субстратным комплексом (ES).
Конкурентный ингибитор обычно структурно схож с субстратом, однако фермент не способен катализировать реакцию в присутствии ингибитора из-за отсутствия у последнего необходимых функциональных групп.
Слайд 4КОНКУРЕНТНОЕ ИНГИБИРОВАНИЕ
Реакция, катализируемая сукцинатдегидрогеназой, и ее конкурентное ингибирование.
Конкурентные ингибиторы напоминают в структурном

отношении сукцинат- они содержат две определенным образом расположенные в пространстве отрицательно заряженные группы, которые соответствуют конформации активного центра.
Слайд 5НЕКОНКУРЕНТНОЕ ИНГИБИРОВАНИЕ
В случае неконкурентного ингибирования ингибитор связывается с ферментом не в активном

центре.
Неконкурентные ингибиторы связываются обратимо как с ферментом, так и с фермент-субстратным комплексом.
Ингибитор вызывает такие конформационные изменения, которые не позволяют ферменту превращать субстрат в продукт, но не влияют на сродство фермента к субстрату.




 Комнатные растения
Комнатные растения Вагітність і гігієна вагітної жінки. Пологи. Годування дитини грудьми
Вагітність і гігієна вагітної жінки. Пологи. Годування дитини грудьми Наследование признаков сцепленное с полом. Нарушения формирования пола
Наследование признаков сцепленное с полом. Нарушения формирования пола Роль жиров в жизни человека
Роль жиров в жизни человека Презентация на тему Деление клетки Митоз
Презентация на тему Деление клетки Митоз  ЭКО Флоронс
ЭКО Флоронс Паспорта комнатных растений
Паспорта комнатных растений Презентация на тему Функция эритроцитов. Понятие об эритроне
Презентация на тему Функция эритроцитов. Понятие об эритроне  Голонасінні
Голонасінні Nerw sistemasy
Nerw sistemasy Процессы в живой природе
Процессы в живой природе Систематика растений, ее значение для ботаники. Водоросли, их разнообразие и значение в природе
Систематика растений, ее значение для ботаники. Водоросли, их разнообразие и значение в природе Строение органов дыхания
Строение органов дыхания Белки
Белки Микроэволюция. Популяция. Выявление изменчивости у особей одного вида
Микроэволюция. Популяция. Выявление изменчивости у особей одного вида Регуляция кровообращения
Регуляция кровообращения Физиология растений
Физиология растений Combaterea Buruienilor Perene în Culturile Legumicole
Combaterea Buruienilor Perene în Culturile Legumicole Лизосомы. Типы лизосом
Лизосомы. Типы лизосом Переходные формы в природе
Переходные формы в природе Витамин С
Витамин С Состав воздуха. Газообмен в лёгких и тканях
Состав воздуха. Газообмен в лёгких и тканях Модификационная изменчивость
Модификационная изменчивость Строение тела
Строение тела Бобр - крупный грызун
Бобр - крупный грызун Панда
Панда Презентация на тему Многообразие и происхождение культурных растений (6 класс)
Презентация на тему Многообразие и происхождение культурных растений (6 класс)  Анатомическое строение артикуляционного аппарата
Анатомическое строение артикуляционного аппарата