Содержание
- 2. Антибиотики – специфические продукты жизнедеятельности микроорганизмов, обладающие высокой физиологической активностью к определенным группам микроорганизмов и злокачественным
- 3. Процесс получения антибиотика включает в себя четыре основные стадии получение соответствующего штамма — продуцента антибиотика, пригодного
- 4. Первая задача при поиске продуцентов антибиотиков — выделение их из природных источников. Вместе с тем для
- 5. К числу наиболее существенных факторов, оказывающих влияние на проявление антибиотических свойств микроорганизмов, относятся состав среды, ее
- 6. При промышленном получении ряда антибиотиков в качестве источников углерода нередко применяют картофельный крахмал, кукурузную муку или
- 7. Источниками минерального питания служат фосфор, сера и другие макро- и микроэлементы. Большинство микроорганизмов легко используют в
- 8. Влияние рН среды. Многие бактериальные организмы, синтезирующие антибиотики, лучше развиваются при рН около 7,0, хотя некоторые,
- 10. Скачать презентацию
Слайд 2Антибиотики – специфические продукты жизнедеятельности микроорганизмов, обладающие высокой физиологической активностью к определенным
Антибиотики – специфические продукты жизнедеятельности микроорганизмов, обладающие высокой физиологической активностью к определенным

Специфичность характеризуется: 1. Высокой биологической активностью по отношению к чувствительным микроорганизмам, т.е. даже в очень низких концентрациях проявляют высокий физиологический эффект. Например, пенициллин в концентрации 0,000001 г/мл оказывает выраженное бактерицидное действие. 2. Избирательность действия, например, бензилпенициллин действует только на грамположительные кокки и не оказывает биологического действия на грамотрицательные.
Слайд 3Процесс получения антибиотика включает в себя четыре основные стадии получение соответствующего штамма
Процесс получения антибиотика включает в себя четыре основные стадии получение соответствующего штамма

Слайд 4Первая задача при поиске продуцентов антибиотиков — выделение их из природных источников.
Первая задача при поиске продуцентов антибиотиков — выделение их из природных источников.
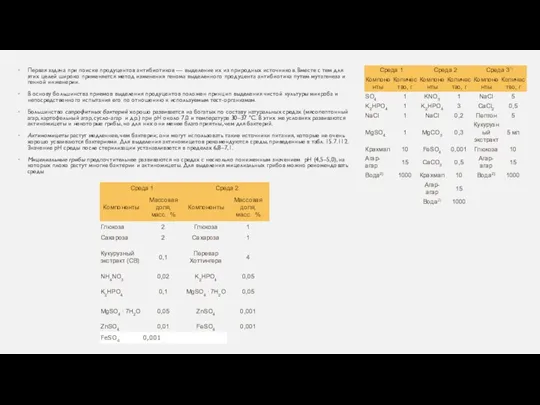
В основу большинства приемов выделения продуцентов положен принцип выделения чистой культуры микроба и непосредственного испытания его по отношению к используемым тест-организмам.
Большинство сапрофитных бактерий хорошо развивается на богатых по составу натуральных средах (мясопептонный агар, картофельный агар, сусло-агар и др.) при рН около 7,0 и температуре 30–37 °С. В этих же условиях развиваются актиномицеты и некоторые грибы, но для них они менее благоприятны, чем для бактерий.
Актиномицеты растут медленнее, чем бактерии; они могут использовать такие источники питания, которые не очень хорошо усваиваются бактериями. Для выделения актиномицетов рекомендуются среды, приведенные в табл. 15.7.112. Значение рН среды после стерилизации устанавливается в пределах 6,8–7,1.
Мицелиальные грибы предпочтительнее развиваются на средах с несколько пониженным значением рН (4,5–5,0), на которых плохо растут многие бактерии и актиномицеты. Для выделения мицелиальных грибов можно рекомендовать среды
Слайд 5К числу наиболее существенных факторов, оказывающих влияние на проявление антибиотических свойств микроорганизмов,
К числу наиболее существенных факторов, оказывающих влияние на проявление антибиотических свойств микроорганизмов,

Среды для культивирования микроорганизмов. Натуральные (комплексные) среды, состоящие из природных соединений и имеющие неопределенный химический состав (части зеленых растений, животные ткани, солод, дрожжи, фрукты, овощи, навоз, почва и т. д.), содержат все компоненты, необходимые для роста и развития микроорганизмов большинства видов. Используются следующие среды:
мясопептонная среда, в состав которой одновременно с мясным экстрактом и пептоном входят хлорид натрия, фосфат калия, иногда глюкоза или сахароза; используется обычно в лабораторной практике;
картофельные среды с глюкозой и пептоном, часто используемые в лаборатории для культивирования многих видов актиномицетов и бактерий;
среды с кукурузным экстрактом, соевой мукой, бардой и другими веществами, в состав которых входят сульфат аммония, карбонат кальция, фосфаты, глюкоза, сахароза, лактоза или иные углеводы и ряд других соединений; среды успешно применяются в промышленности, т. к. являются дешевыми и обеспечивают хорошее развитие микроорганизмов с высоким выходом антибиотиков.
Поскольку натуральные среды не позволяют получать строгие количественные данные для изучения физиологических и биохимических особенностей организма, применяют синтетические среды, которые подбирают для отдельных продуцентов индивидуально. Синтетические среды могут быть как относительно простыми, так и сложными, для составления которых используют методы математического планирования эксперимента.
Источниками углерода могут быть органические кислоты, спирты, углеводы, сочетания различных углеродсодержащих соединений
Слайд 6При промышленном получении ряда антибиотиков в качестве источников углерода нередко применяют картофельный
При промышленном получении ряда антибиотиков в качестве источников углерода нередко применяют картофельный

Источники азота оказывают большое влияние на образование микроорганизмами антибиотических веществ. Обычно в средах для культивирования микроорганизмов источником азота служат соли азотной (реже азотистой) кислоты, аммонийные соли органических и неорганических кислот, аминокислоты, белки и продукты их гидролиза. Многие микроорганизмы успешно используют и окисленные формы азота, некоторые из них нуждаются именно в нитратном источнике азота (Streptomyces auranticus, S. subtropicus и некоторые другие). Ряд актиномицетов иногда усваивают лучше нитраты, чем аммонийные соли; они могут использовать даже нитриты, если их вносят в среду в небольших количествах (не более 50 мг NaNO2 / 1 л среды). При этом усвоение нитритов тесно связано с источником углерода; например в присутствии глицерина нитриты потребляются гораздо лучше, чем в присутствии глюкозы. Использование аммония и некоторых органических источников азота плесневыми грибами улучшается в присутствии небольших количеств (0,1–0,2 %) некоторых дикарбоновых (янтарной и фумаровой) кислот. В ряде случаев для накопления антибиотика необходимо присутствие и аммонийного, и нитратного источника азота (биосинтез пенициллина).
Обычно наиболее благоприятным для микроорганизмов является соотношение C : N = 20. Однако для образования антибиотика такое соотношение не всегда оптимально. Поэтому для каждого продуцента необходимо подбирать соответствующее соотношение углерода и азота.
Слайд 7Источниками минерального питания служат фосфор, сера и другие макро- и микроэлементы.
Большинство микроорганизмов легко
Источниками минерального питания служат фосфор, сера и другие макро- и микроэлементы.
Большинство микроорганизмов легко

Продуценты антибиотиков по отношению к концентрации фосфора в среде можно разделить на три группы:
высокочувствительные продуценты, для которых оптимальная концентрация фосфора в среде составляет менее 0,01 % (продуценты нистатина, тетрациклинов, флоримицина, ванкомицина);
продуценты средней чувствительности, для которых оптимальная концентрация фосфора составляет 0,010–0,015 % (продуценты стрептомицина, эритромицина, циклосерина, неомицина);
малочувствительные продуценты, для которых оптимальная концентрация фосфора составляет 0,018–0,020 % (продуценты новобиоцина, грамицидина, олеандомицина).
Сера входит в состав некоторых антибиотиков, образуемых грибами (пенициллин, цефалоспорин, глиотоксин и др.), бактериями (бацитрацины, субтилины, низины) и актиномицетами (эхиномицины, группа тиострептона). Обычно источником серы в среде служат сульфаты. Однако при биосинтезе пенициллина лучшим источником серы для продуцента служит тиосульфат натрия.
Кроме того, для биосинтеза антибиотиков необходимы и отдельные микроэлементы. Так, продуцент альбомицина S. subtropicus образует антибиотик при значительной концентрации железа в среде. Железо необходимо для образования хлорамфеникола и других антибиотиков.
Биосинтезу ряда антибиотических веществ (хлорамфеникола, стрептомицина, пенициллина и др.) способствуют ионы цинка.
Стимулирующее влияние на биосинтез гентамицина, курамицина А, фософономицина оказывают ионы кобальта.
Ионы галогенов входят в состав некоторых тетрациклиновых антибиотиков и хлорамфеникола.
Слайд 8Влияние рН среды. Многие бактериальные организмы, синтезирующие антибиотики, лучше развиваются при рН около
Влияние рН среды. Многие бактериальные организмы, синтезирующие антибиотики, лучше развиваются при рН около

Большинство актиномицетов хорошо развиваются при начальных значениях рН среды в пределах от 6,7 до 7,8; в большинстве случаев жизнеспособность актиномицетов при рН ниже 4,0–4,5 подавлена.
Температура. Для большинства бактериальных организмов температурный оптимум развития лежит в диапазоне 30–37 °С. Для продуцента грамицидина С (B. brevis) оптимальная температура для развития и биосинтеза равна 40 °С.
Актиномицеты, как правило, культивируются при температуре 26–30 °С, хотя некоторые виды стрептомицетов могут развиваться как при пониженных (от 0 до 18 °С), так и при повышенных (55–60 °С) температурах.
Для большинства мицелиальных грибов оптимальная температура составляет 25–28 °С.
Аэрация. Большинство изученных продуцентов антибиотиков являются аэробами. Для биосинтеза многих антибиотиков (пенициллин, стрептомицин и др.) максимальное их накопление происходит при степени аэрации, равной единице, при которой через определенный объем среды за 1 мин продувается такой же объем воздуха.
В процессе развития продуцента антибиотика в промышленных условиях потребность организма в кислороде меняется в зависимости от стадии развития, вязкости КЖ и других факторов. На определенных стадиях могут возникнуть ситуации, связанные с кислородным голоданием продуцента. В этих условиях следует принимать дополнительные меры, например, повышение концентрации окислителя добавлением пероксида водорода.
 Чай пить - долго жить
Чай пить - долго жить Покрытосеменные, или цветковые растения
Покрытосеменные, или цветковые растения Взаимодействие генов. Цитоплазматическая наследственность. Генетика пола
Взаимодействие генов. Цитоплазматическая наследственность. Генетика пола Занимательные вопросы о лошадях
Занимательные вопросы о лошадях Внутренние мужские половые органы
Внутренние мужские половые органы Некоторые опасные животные мира
Некоторые опасные животные мира Анатомия стебля. Лист
Анатомия стебля. Лист Дизайн СОШ в концепции устойчивого развития природоохранных территорий
Дизайн СОШ в концепции устойчивого развития природоохранных территорий Курсовая работа. Система обучения. Лестница деятельности. На примере изучения белков в ходе интегрированного урока
Курсовая работа. Система обучения. Лестница деятельности. На примере изучения белков в ходе интегрированного урока Мутационная изменчивость
Мутационная изменчивость Почему люди любят динозавров
Почему люди любят динозавров День Птиц
День Птиц Влияние радиоактивного излучения на живые организмы
Влияние радиоактивного излучения на живые организмы Галерея. История развития биологии
Галерея. История развития биологии Презентация на тему Сонная болезнь
Презентация на тему Сонная болезнь  Шестой день творения
Шестой день творения Фауна различных материков
Фауна различных материков 11_i_12_myshtsy_verkh_nizhn_konechnostei_774
11_i_12_myshtsy_verkh_nizhn_konechnostei_774 Формы естественного отбора
Формы естественного отбора Строение лишайника
Строение лишайника Воздушное пространство – это воздух, который окутывает нашу Землю
Воздушное пространство – это воздух, который окутывает нашу Землю Blue whales
Blue whales Занимательный час Эти необычные домашние животные
Занимательный час Эти необычные домашние животные Экзаменационные препараты
Экзаменационные препараты Презентация на тему Богомолы
Презентация на тему Богомолы  Зимующие птицы
Зимующие птицы Дыхательная система
Дыхательная система Железы внутренней секреций. Эндокринная система
Железы внутренней секреций. Эндокринная система