Содержание
- 2. Плазмиды С узким спектром хозяев Могут существовать только в очень ограниченном числе видов бактерий. Чаще всего
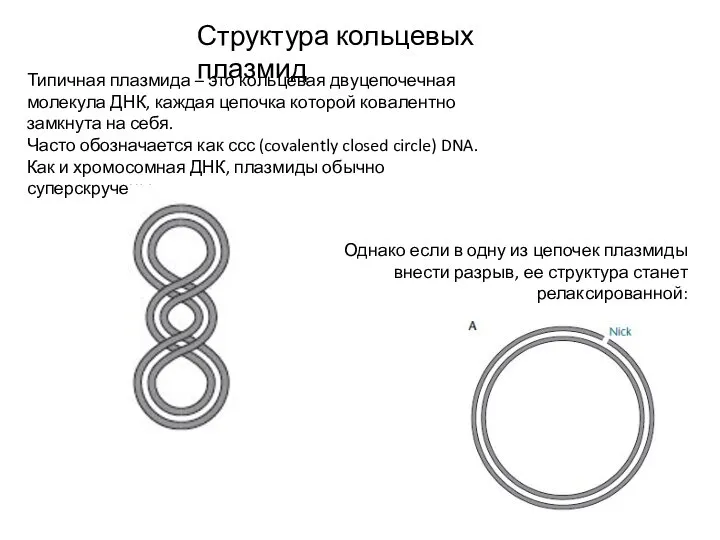
- 3. Структура кольцевых плазмид Типичная плазмида – это кольцевая двуцепочечная молекула ДНК, каждая цепочка которой ковалентно замкнута
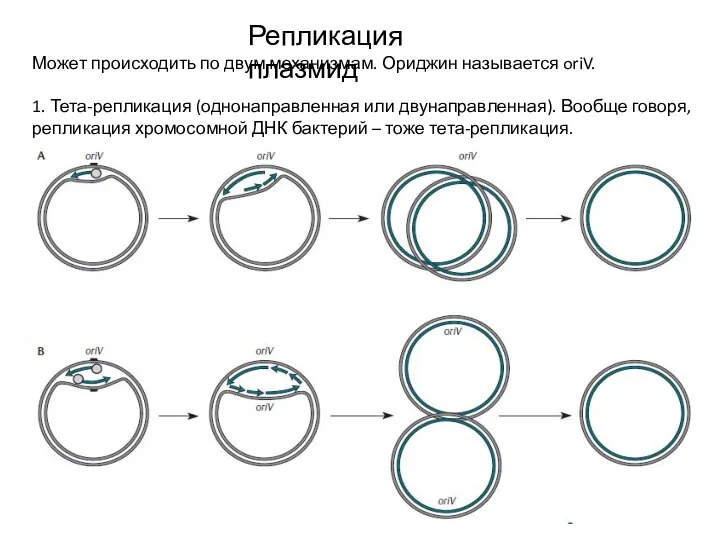
- 4. Репликация плазмид Может происходить по двум механизмам. Ориджин называется oriV. 1. Тета-репликация (однонаправленная или двунаправленная). Вообще
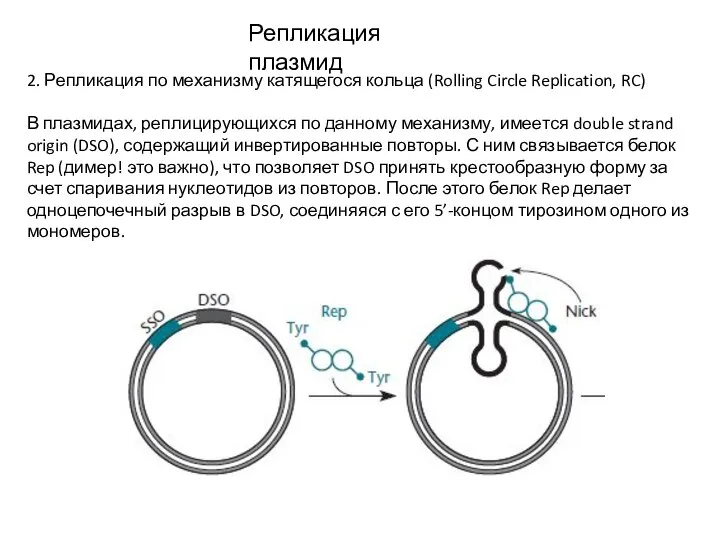
- 5. Репликация плазмид 2. Репликация по механизму катящегося кольца (Rolling Circle Replication, RC) В плазмидах, реплицирующихся по
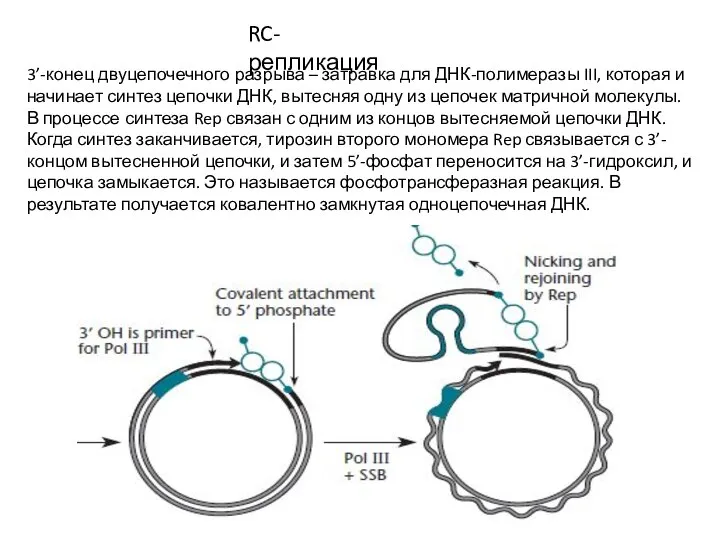
- 6. RC-репликация 3’-конец двуцепочечного разрыва – затравка для ДНК-полимеразы III, которая и начинает синтез цепочки ДНК, вытесняя
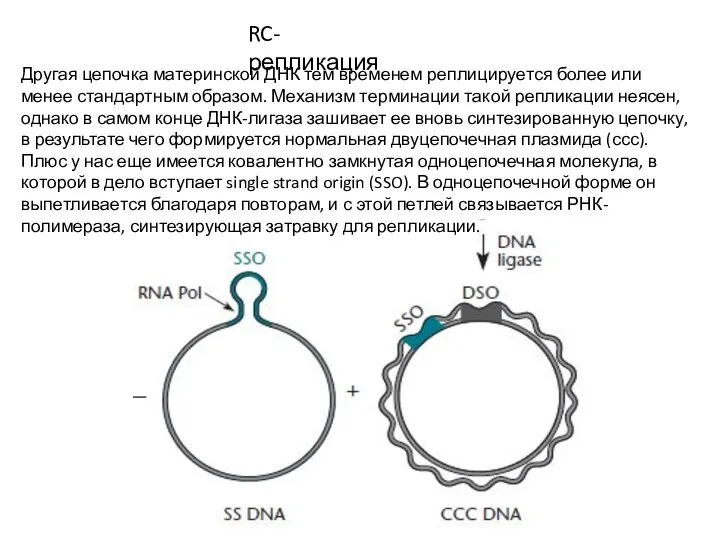
- 7. RC-репликация Другая цепочка материнской ДНК тем временем реплицируется более или менее стандартным образом. Механизм терминации такой
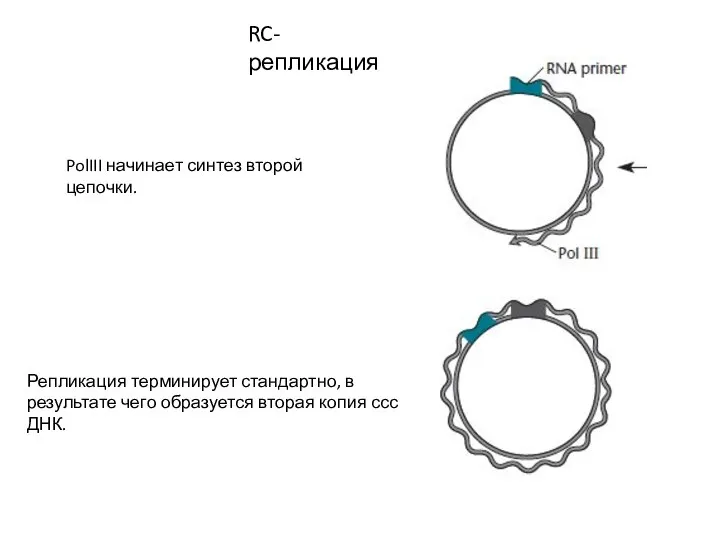
- 8. RC-репликация PolIII начинает синтез второй цепочки. Репликация терминирует стандартно, в результате чего образуется вторая копия ссс
- 9. Интересные подробности о репликации плазмид Белок Rep после своего участия в репликации «приходит в негодность» (это
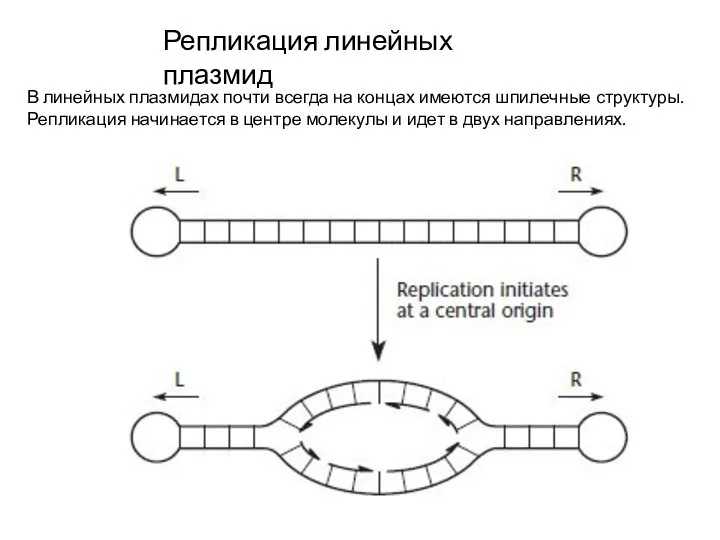
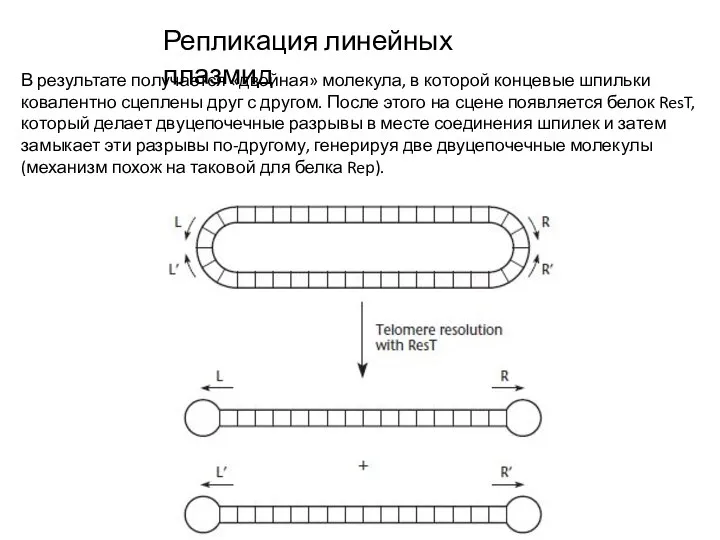
- 10. Репликация линейных плазмид В линейных плазмидах почти всегда на концах имеются шпилечные структуры. Репликация начинается в
- 11. Репликация линейных плазмид В результате получается «двойная» молекула, в которой концевые шпильки ковалентно сцеплены друг с
- 12. Несовместимость плазмид Несовместимость (inc, incompatibility) двух плазмид – их неспособность существовать в одной бактериальной клетке. Иногда
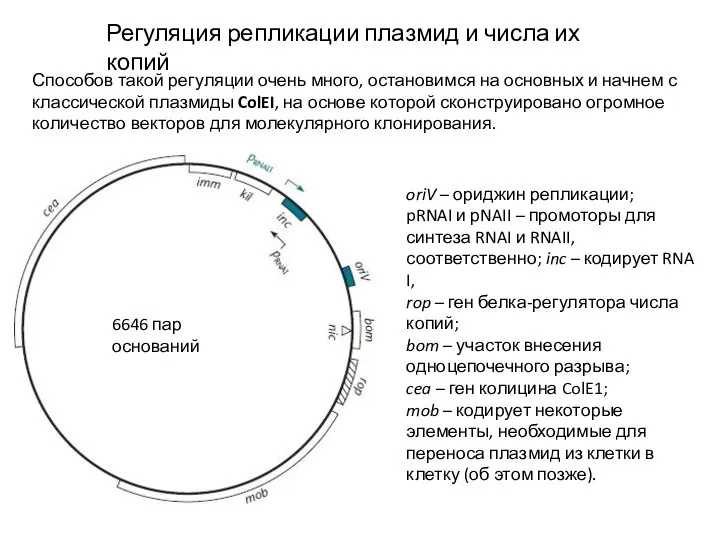
- 13. Регуляция репликации плазмид и числа их копий Способов такой регуляции очень много, остановимся на основных и
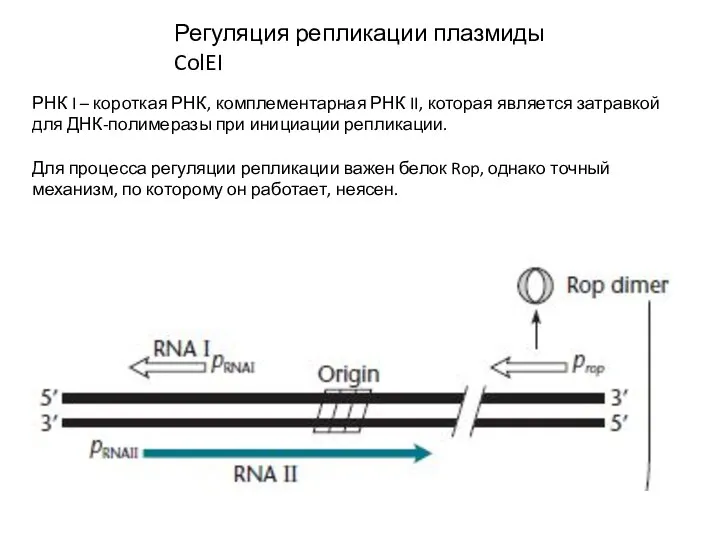
- 14. Регуляция репликации плазмиды ColEI РНК I – короткая РНК, комплементарная РНК II, которая является затравкой для
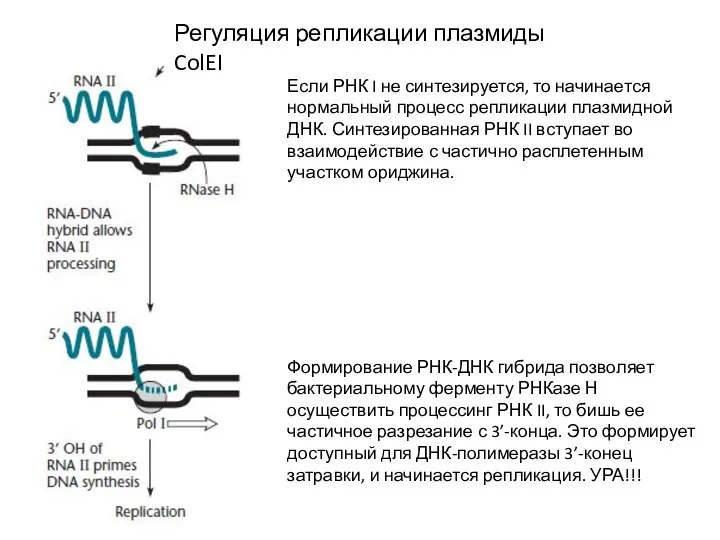
- 15. Регуляция репликации плазмиды ColEI Если РНК I не синтезируется, то начинается нормальный процесс репликации плазмидной ДНК.
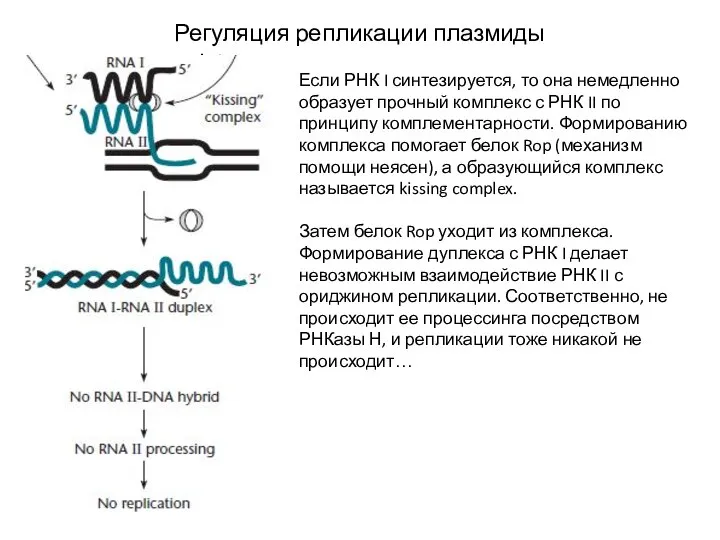
- 16. Регуляция репликации плазмиды ColEI Если РНК I синтезируется, то она немедленно образует прочный комплекс с РНК
- 17. Регуляция репликации плазмиды ColEI Чем больше в клетке копий РНК I, тем слабее репликация, а значит,
- 18. Регуляция репликации плазмиды R1 Регуляция также основана на действии короткой РНК, только она образует комплекс не
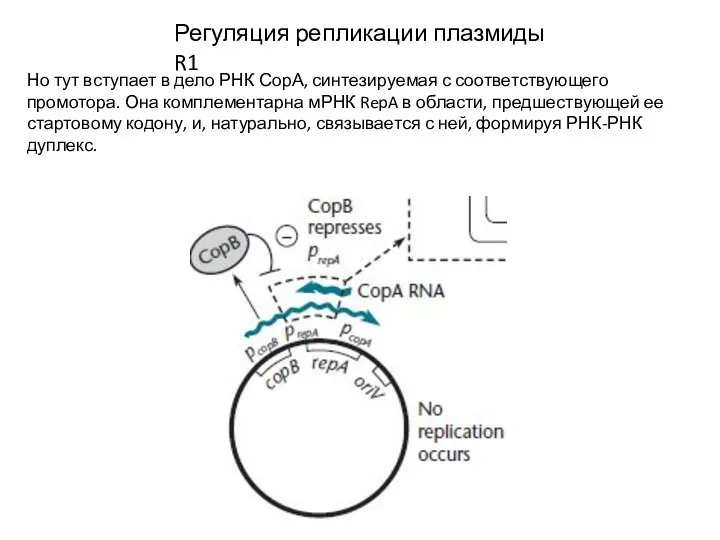
- 19. Регуляция репликации плазмиды R1 Но тут вступает в дело РНК СорА, синтезируемая с соответствующего промотора. Она
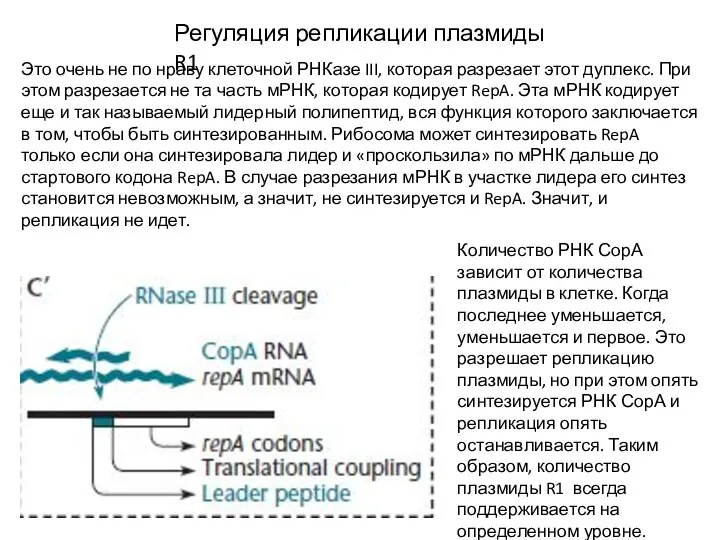
- 20. Регуляция репликации плазмиды R1 Это очень не по нраву клеточной РНКазе III, которая разрезает этот дуплекс.
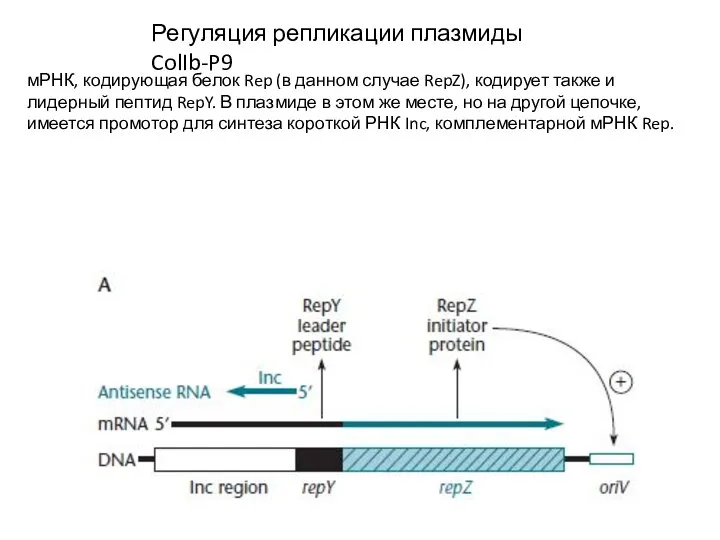
- 21. Регуляция репликации плазмиды ColIb-P9 мРНК, кодирующая белок Rep (в данном случае RepZ), кодирует также и лидерный
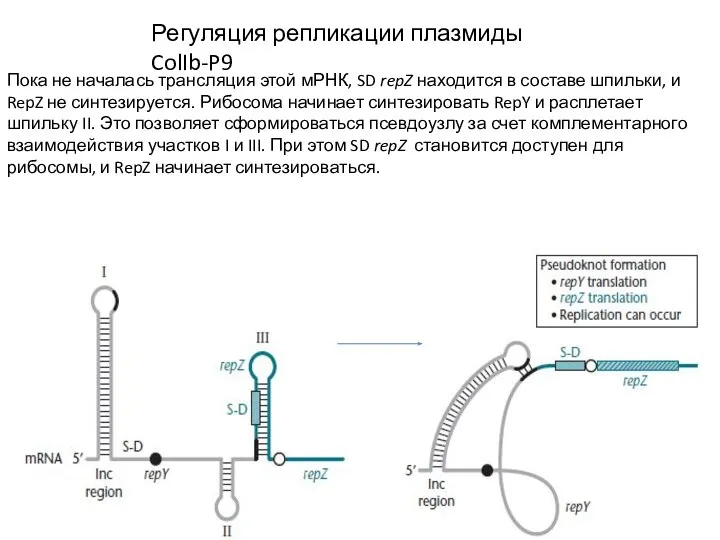
- 22. Регуляция репликации плазмиды ColIb-P9 Пока не началась трансляция этой мРНК, SD repZ находится в составе шпильки,
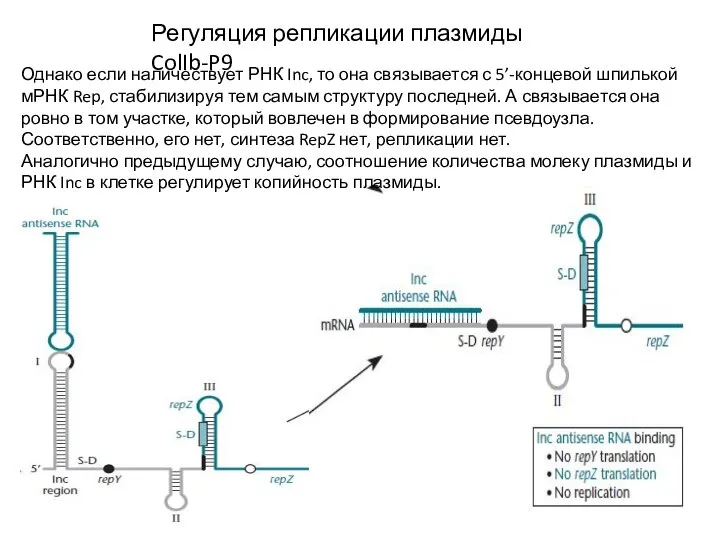
- 23. Регуляция репликации плазмиды ColIb-P9 Однако если наличествует РНК Inc, то она связывается с 5’-концевой шпилькой мРНК
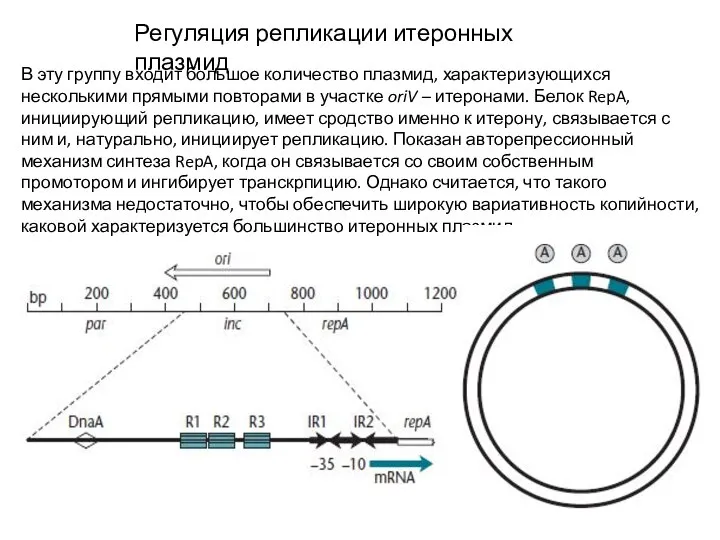
- 24. Регуляция репликации итеронных плазмид В эту группу входит большое количество плазмид, характеризующихся несколькими прямыми повторами в
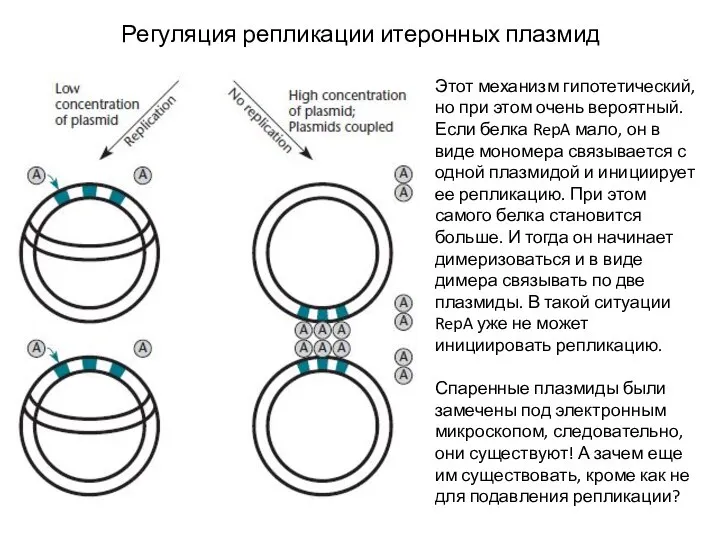
- 25. Регуляция репликации итеронных плазмид Этот механизм гипотетический, но при этом очень вероятный. Если белка RepA мало,
- 26. Потеря плазмиды Потеря плазмиды есть ситуация, в которой после клеточного деления в одну из дочерних клеток
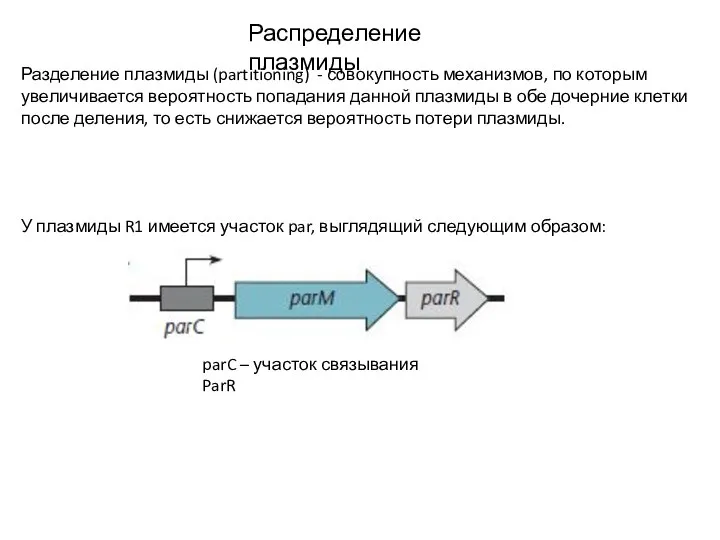
- 27. Распределение плазмиды Разделение плазмиды (partitioning) - совокупность механизмов, по которым увеличивается вероятность попадания данной плазмиды в
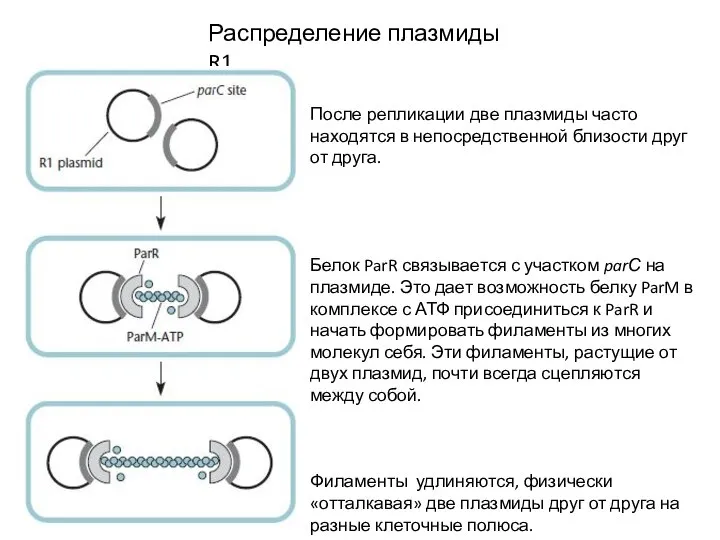
- 28. Распределение плазмиды R1 После репликации две плазмиды часто находятся в непосредственной близости друг от друга. Белок
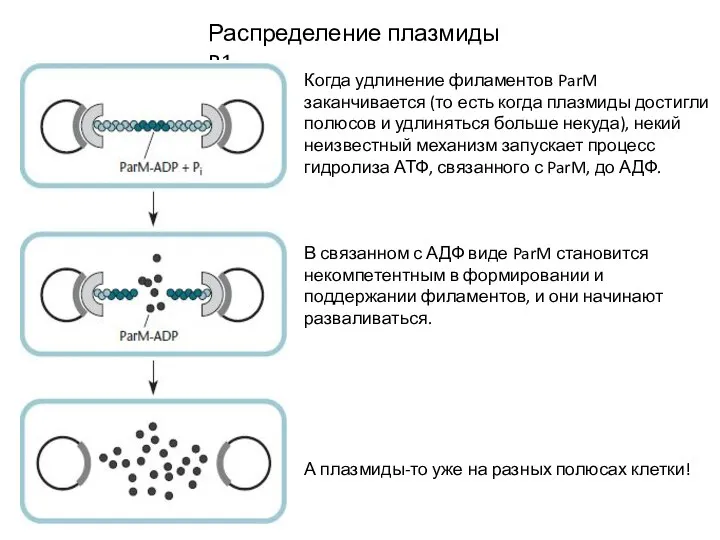
- 29. Распределение плазмиды R1 Когда удлинение филаментов ParM заканчивается (то есть когда плазмиды достигли полюсов и удлиняться
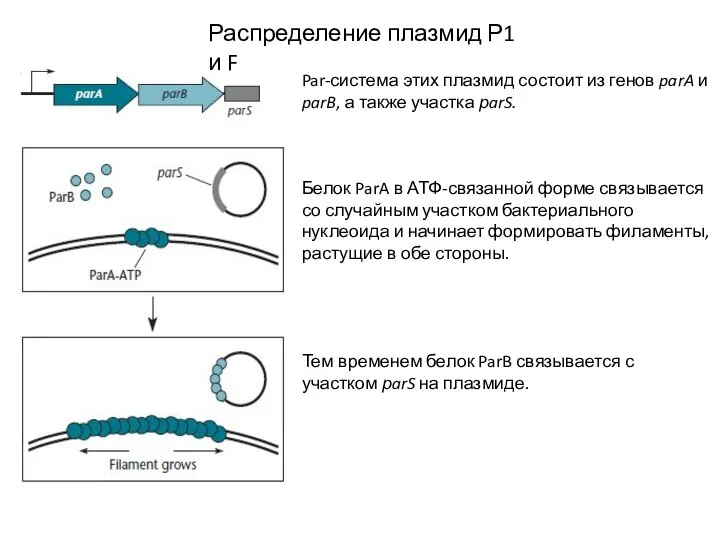
- 30. Распределение плазмид Р1 и F Par-система этих плазмид состоит из генов parA и parB, а также
- 32. Скачать презентацию





 Нервная система. Классификация
Нервная система. Классификация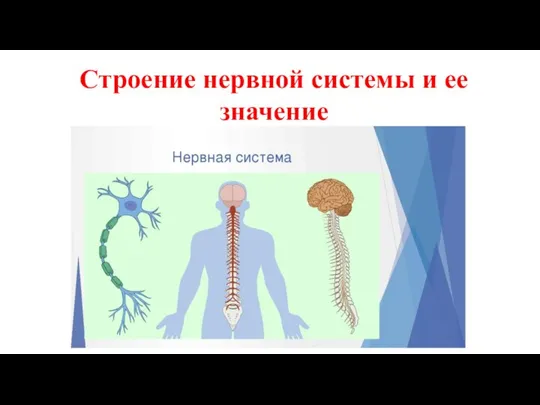 строение_НС
строение_НС Анаконда (фотографии)
Анаконда (фотографии) Деление клетки. Митоз
Деление клетки. Митоз Вегетативное размножение
Вегетативное размножение Ацинус
Ацинус Строение клетки
Строение клетки Органоиды клетки
Органоиды клетки Амфибии. Лягушка-бык
Амфибии. Лягушка-бык Презентация на тему Земноводные и пресмыкающиеся
Презентация на тему Земноводные и пресмыкающиеся  Исследование взаимосвязи соматотипа и чувствительности к подкреплению с Интернет-зависимостью и табакокурением
Исследование взаимосвязи соматотипа и чувствительности к подкреплению с Интернет-зависимостью и табакокурением Разнообразие природы родного края
Разнообразие природы родного края Основы цитологии. Субклеточный и клеточный уровни организации тела человека
Основы цитологии. Субклеточный и клеточный уровни организации тела человека Деление клеток
Деление клеток Региональное кровообращение
Региональное кровообращение Апикальные меристемы
Апикальные меристемы Половое размножение
Половое размножение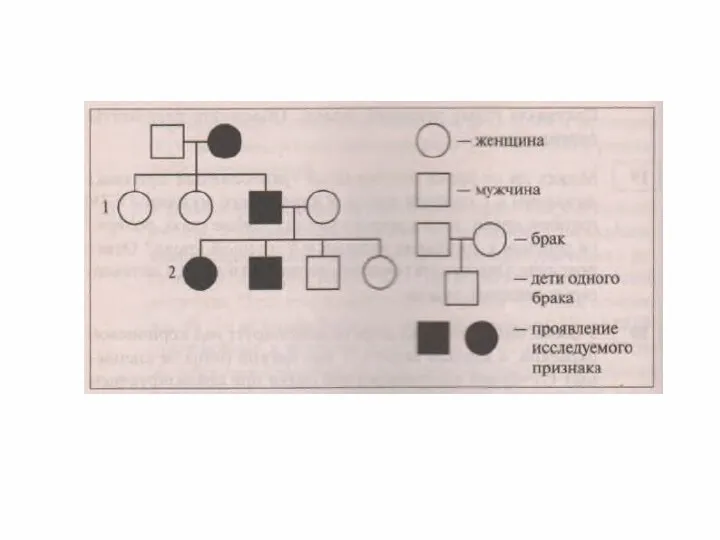 Задачи на составление родословных
Задачи на составление родословных Конкуренция в природе
Конкуренция в природе Презентация на тему Методы селекции растений (11 класс)
Презентация на тему Методы селекции растений (11 класс)  Вода, ее состав, свойства, значение
Вода, ее состав, свойства, значение Генетический код
Генетический код Онтогенетический уровень жизни
Онтогенетический уровень жизни Виды комнатных растений
Виды комнатных растений Слуховой анализатор
Слуховой анализатор Мутація у живих організмів
Мутація у живих організмів Своя игра В мире насекомых
Своя игра В мире насекомых Строение стебля
Строение стебля