Содержание
- 2. Впервые термин «углеводы» был предложен профессором Дерптского (ныне Тартуского) университета К.Г. Шмидтом в 1844 г В
- 3. Углеводы К классу углеводов относят органические соединения, содержащую альдегидную или кетонную группу и несколько спиртовых гидроксилов
- 4. Функции углеводов в организме Углеводы служат материалом, при окислении которого выделяется энергия, используемая в биохимических реакциях
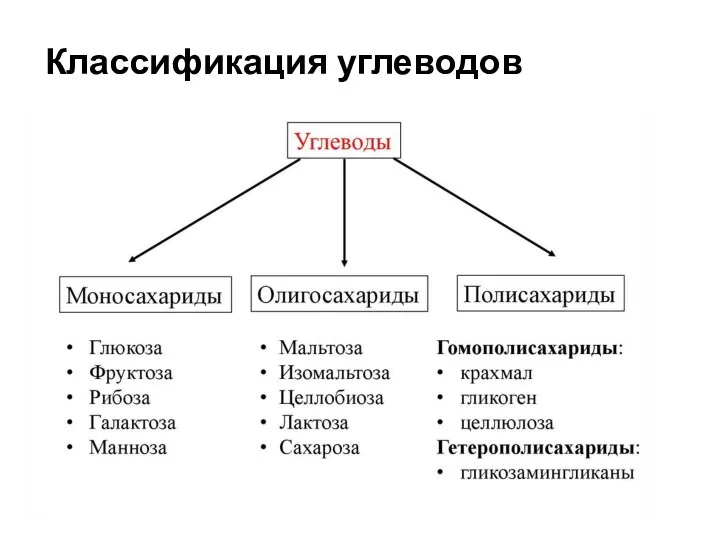
- 5. Классификация углеводов Низшие углеводы называются сахарами, соединения сложной структуры – сахаридами. По правилам номенклатуры название углеводов
- 6. Классификация углеводов
- 7. Моносахариды
- 8. Моносахариды Моносахариды можно рассматривать как производные многоатомных спиртов, содержащие карбонильную (альдегидную или кетонную) группу Если карбонильная
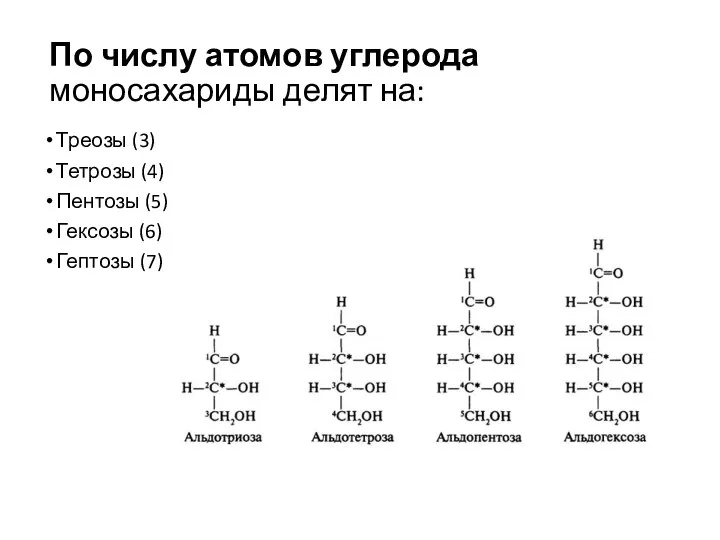
- 9. По числу атомов углерода моносахариды делят на: Треозы (3) Тетрозы (4) Пентозы (5) Гексозы (6) Гептозы
- 10. Изомерия моносахаридов Моносахариды обладают оптической активностью Из шести атомов углерода, составляющих углеродную цепь молекулы глюкозы, четыре
- 11. Э. Фишер предложил сравнивать расположение водорода и гидроксила при втором снизу углеродном атоме в молекуле моносахарида
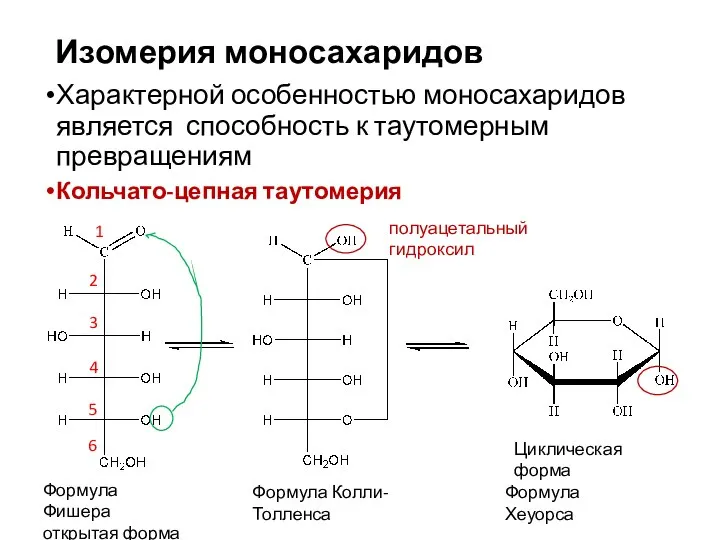
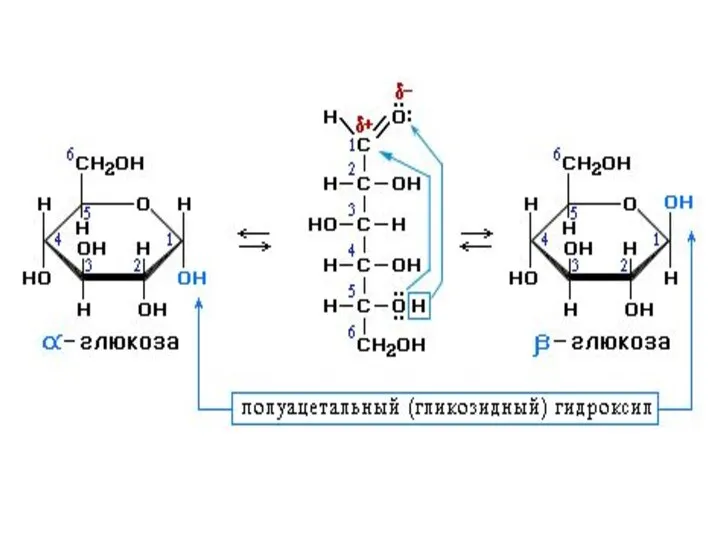
- 13. Изомерия моносахаридов Характерной особенностью моносахаридов является способность к таутомерным превращениям Кольчато-цепная таутомерия полуацетальный гидроксил Циклическая форма
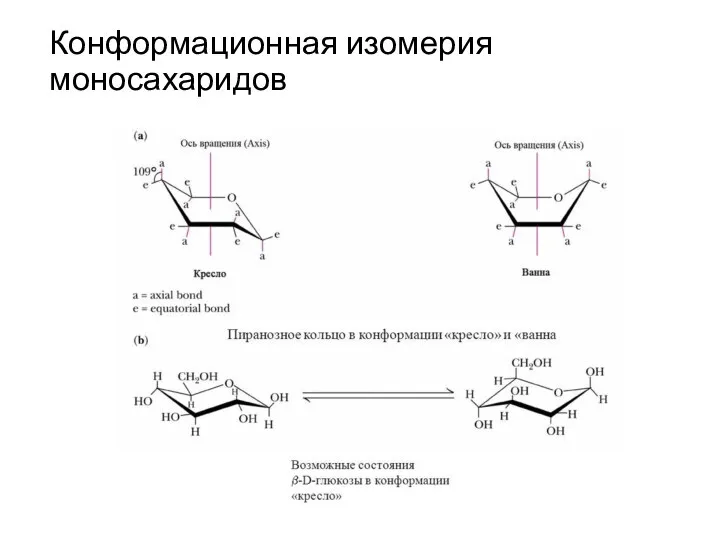
- 15. Конформационная изомерия моносахаридов
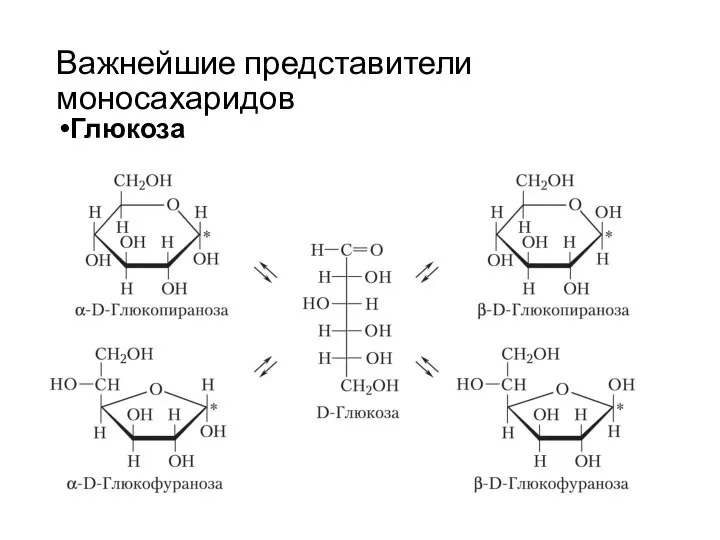
- 16. Важнейшие представители моносахаридов Глюкоза
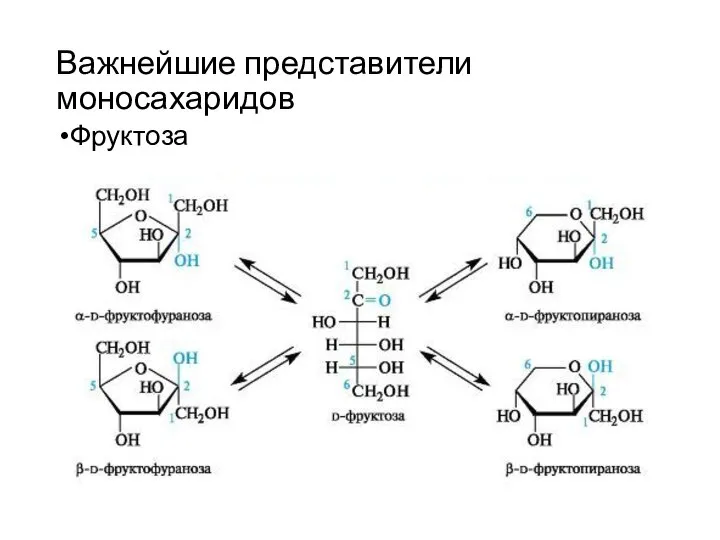
- 17. Важнейшие представители моносахаридов Фруктоза
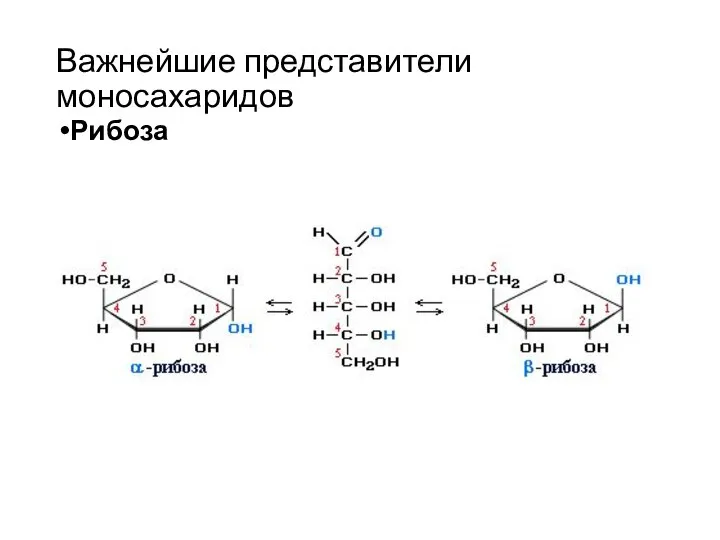
- 18. Важнейшие представители моносахаридов Рибоза
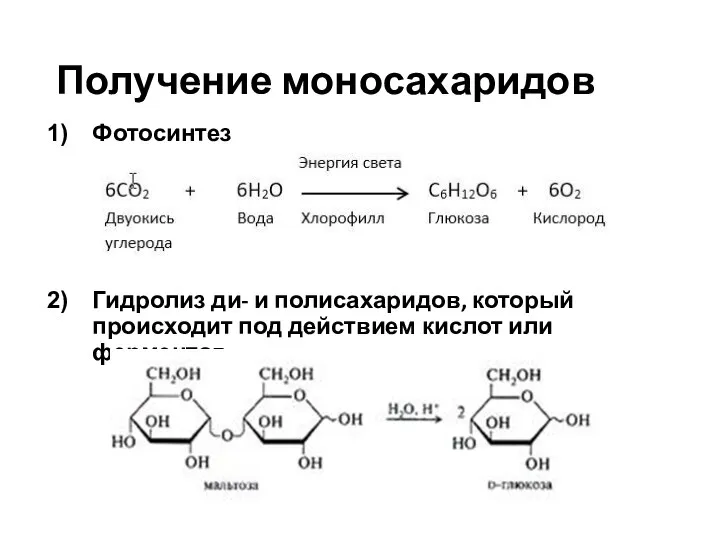
- 19. Получение моносахаридов Фотосинтез Гидролиз ди- и полисахаридов, который происходит под действием кислот или ферментов
- 20. 3) Альдольная конденсация формальдегида – первый синтез сахаров был произведен еще А.М. Бутлеровым, в качестве катализатора
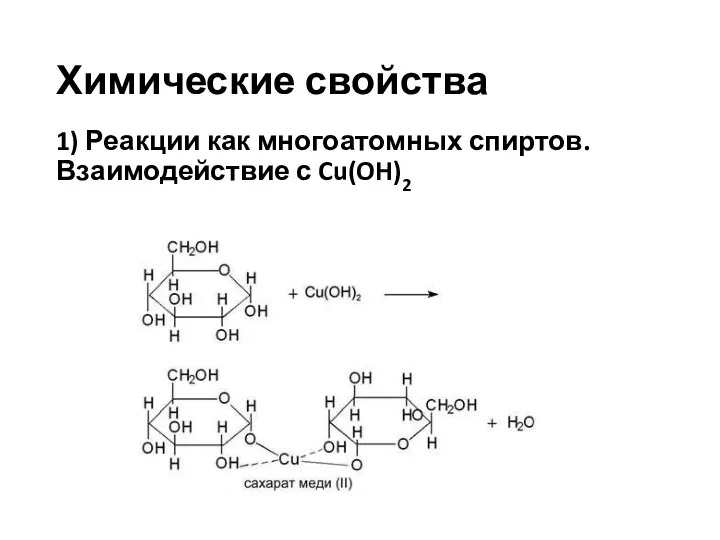
- 21. Химические свойства 1) Реакции как многоатомных спиртов. Взаимодействие с Cu(OH)2
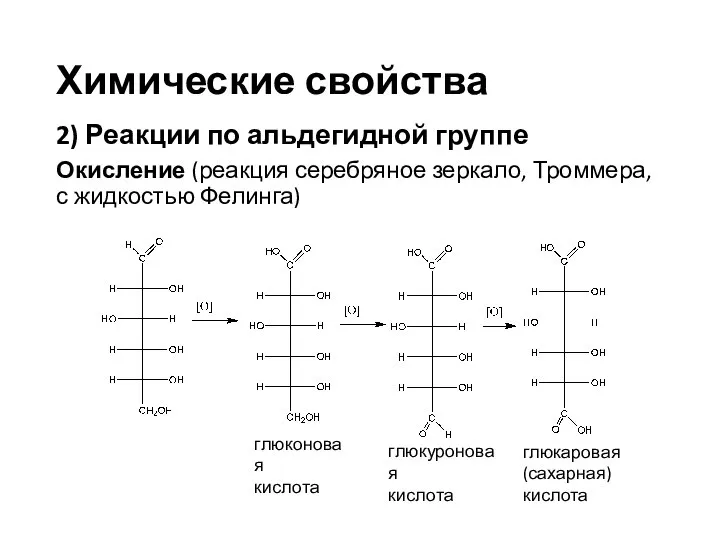
- 22. Химические свойства 2) Реакции по альдегидной группе Окисление (реакция серебряное зеркало, Троммера, с жидкостью Фелинга) глюкуроновая
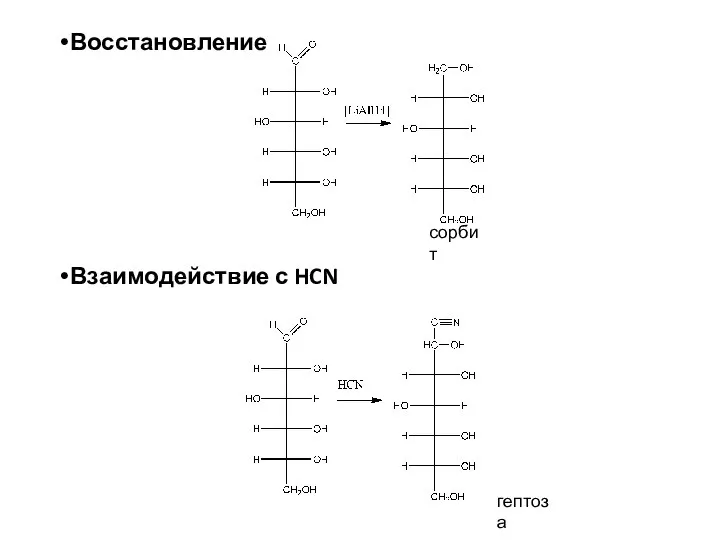
- 23. Восстановление Взаимодействие с HCN сорбит гептоза
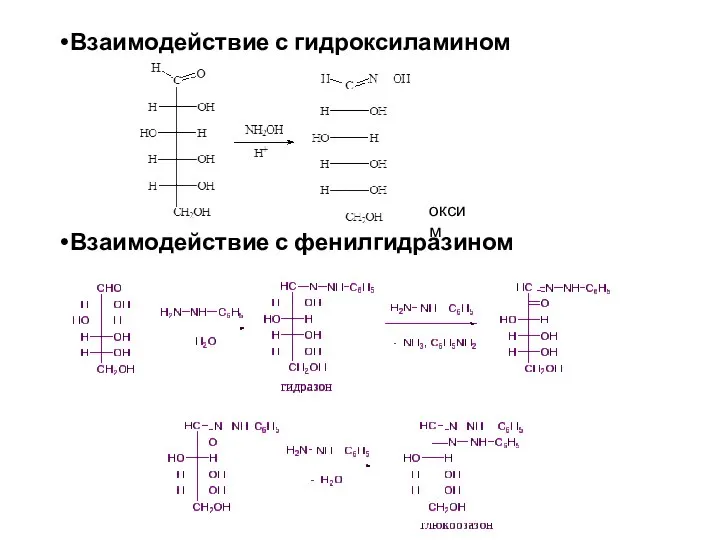
- 24. Взаимодействие с гидроксиламином Взаимодействие с фенилгидразином оксим
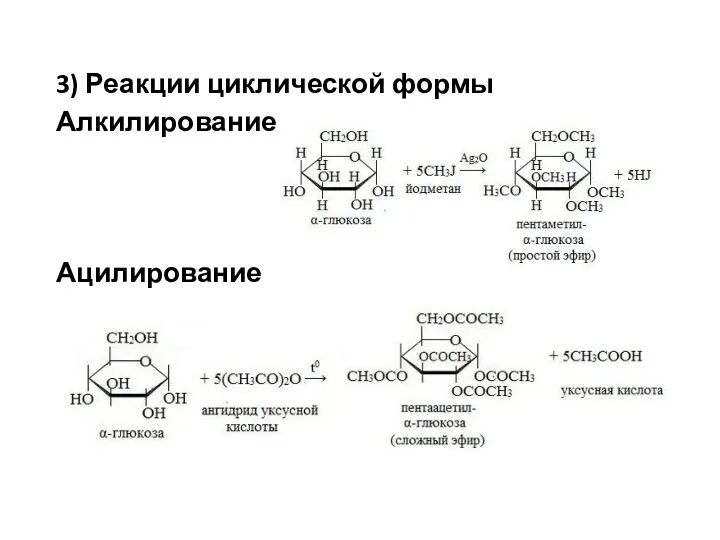
- 25. 3) Реакции циклической формы Алкилирование Ацилирование
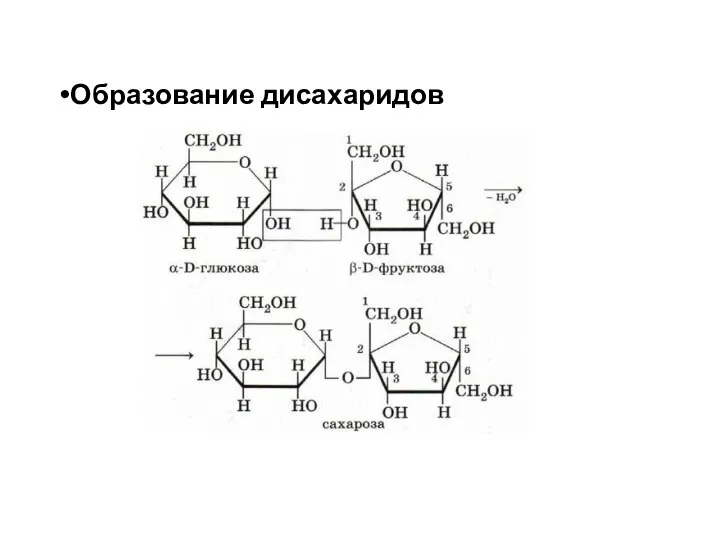
- 26. Образование дисахаридов
- 28. Скачать презентацию










 Болезни лошадей
Болезни лошадей Анатомия органа зрения
Анатомия органа зрения Практическое доказательство пагубного влияния продуктов табачного дыма, алкоголя, токсических веществ на живые организмы
Практическое доказательство пагубного влияния продуктов табачного дыма, алкоголя, токсических веществ на живые организмы Автономное существование человека в природе
Автономное существование человека в природе Мутагенные факторы среды
Мутагенные факторы среды Зоология. Введение
Зоология. Введение Экотоксикология популяций растений
Экотоксикология популяций растений Класс Пресмыкающиеся
Класс Пресмыкающиеся Собаки. Виды собак
Собаки. Виды собак Отдел покрытосеменные растения. Общая характеристика, многообразие покрытосеменных. Деление цветковых на классы и семейства. Д
Отдел покрытосеменные растения. Общая характеристика, многообразие покрытосеменных. Деление цветковых на классы и семейства. Д Презентация на тему Растительная клетка
Презентация на тему Растительная клетка  Основные понятия генетики
Основные понятия генетики 1_4_Tsep_tkanevogo_dykhania
1_4_Tsep_tkanevogo_dykhania Микроорганизмы. Водоросли. Простейшие. Приложение 3
Микроорганизмы. Водоросли. Простейшие. Приложение 3 Как заглянуть в митохондрию с помощью наночастиц
Как заглянуть в митохондрию с помощью наночастиц Высшая нервная деятельность
Высшая нервная деятельность Статеве розмноження рослин. Квітка. Лабораторне дослідження будови квітки. Інструктаж із БЖД
Статеве розмноження рослин. Квітка. Лабораторне дослідження будови квітки. Інструктаж із БЖД Бурый медведь
Бурый медведь Откуда животные?
Откуда животные? Выявление ароморфозов и идиоадаптаций у растений и животных. Лабораторная работа
Выявление ароморфозов и идиоадаптаций у растений и животных. Лабораторная работа Амурский тигр
Амурский тигр Обмен простых белков. Белки плазмы крови
Обмен простых белков. Белки плазмы крови Исследователи природы
Исследователи природы Экология и эволюция. Лекция 3
Экология и эволюция. Лекция 3 Подготовка к тестированию по биологии
Подготовка к тестированию по биологии Tetrapoda. Amphibia. Amniota. Переход от Sarcopterygia к Tetrapoda
Tetrapoda. Amphibia. Amniota. Переход от Sarcopterygia к Tetrapoda 9-13бесполое размножение
9-13бесполое размножение Невозможное путешествие. Путешествие к центру ядерного взрыва. Игра в ДНК
Невозможное путешествие. Путешествие к центру ядерного взрыва. Игра в ДНК