Слайд 2Закон сохранения энергии
Энергия в природе не возникает из ничего и не исчезает:

количество энергии неизменно, она только переходит из одной формы в другую.
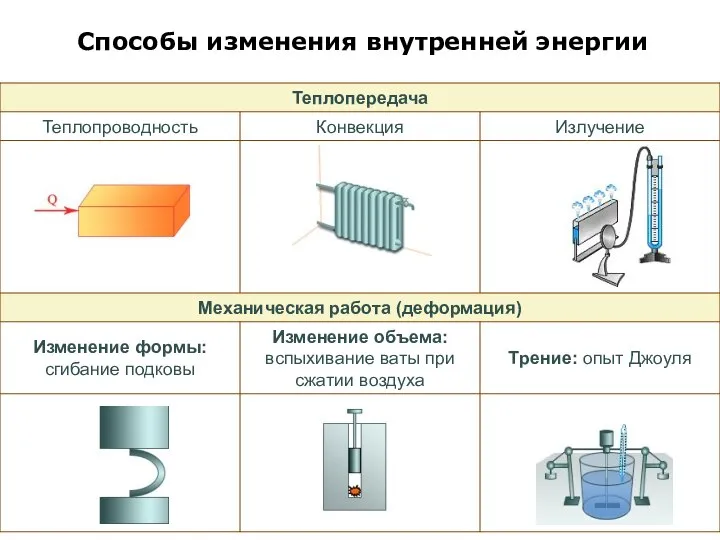
Слайд 3Способы изменения внутренней энергии
Слайд 4I закон термодинамики
внутренняя энергия определяется только состоянием системы, причем изменение внутренней энергии
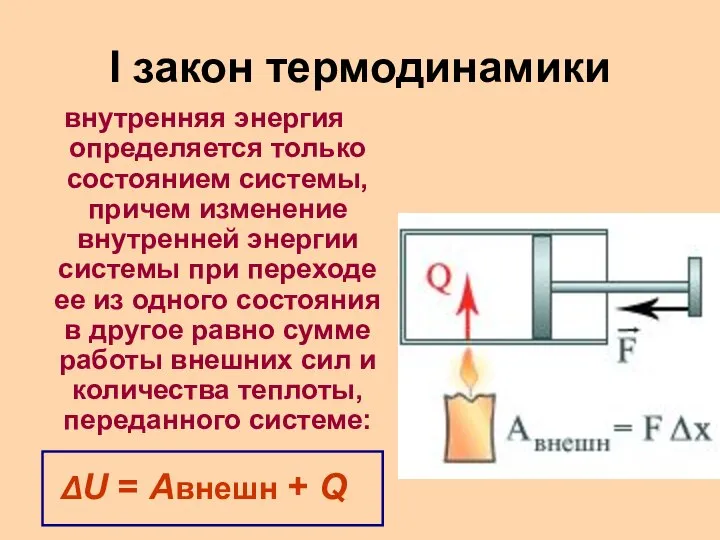
системы при переходе ее из одного состояния в другое равно сумме работы внешних сил и количества теплоты, переданного системе:
ΔU = Aвнешн + Q
Слайд 5Если при нагревании газ расширяется и при этом совершает работу A, то

первый закон термодинамики можно сформулировать по-другому:
Q = ΔU + AI
Количество теплоты, переданное газу, равно сумме изменения его внутренней энергии и работы, совершенной газом.
Так как работа газа и работа внешних сил вследствие 3-го закона Ньютона равны по модулю и имеют противоположный знак:
Aвнешн = –AI
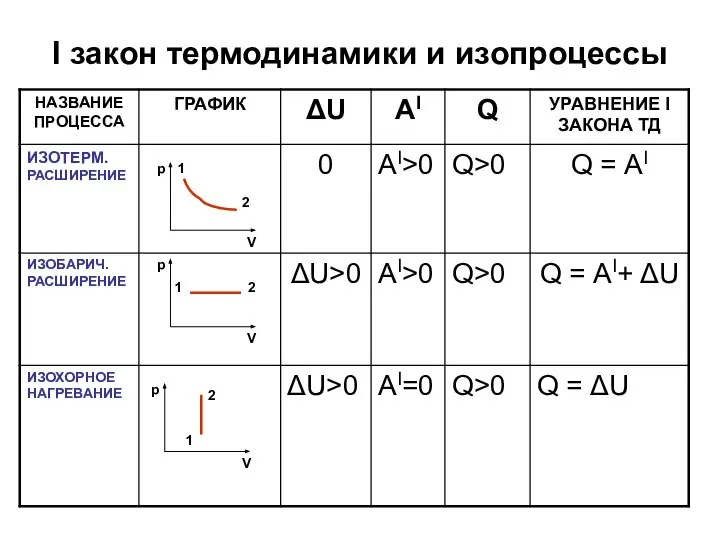
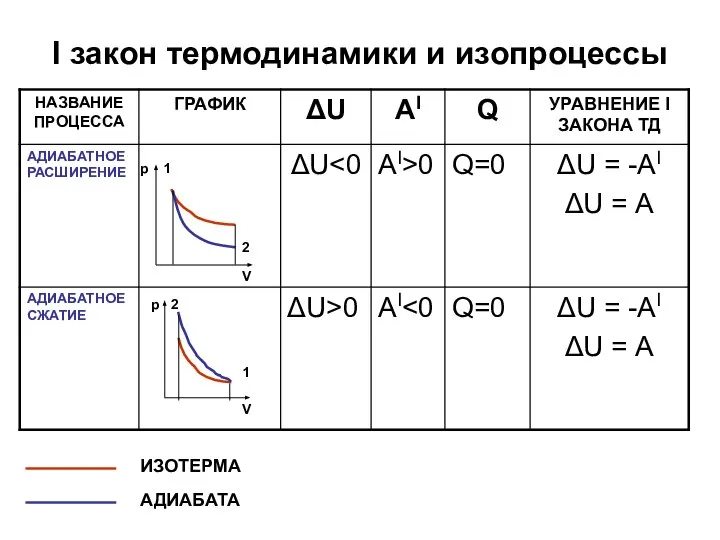
Слайд 6I закон термодинамики и изопроцессы
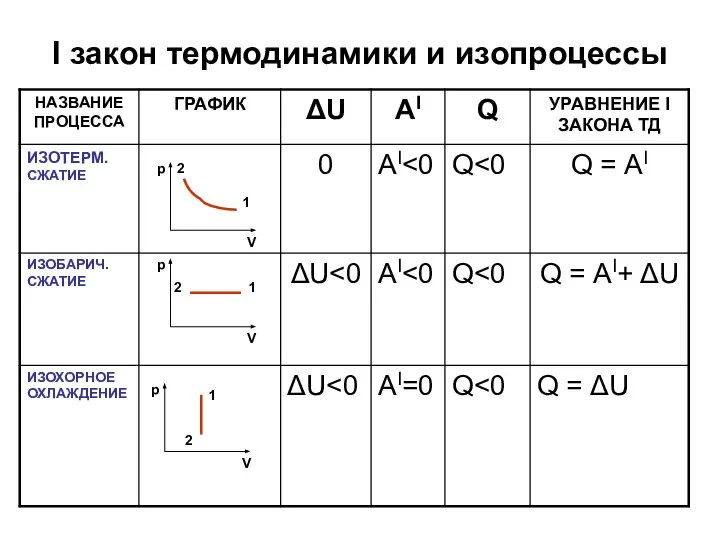
Слайд 7I закон термодинамики и изопроцессы
Слайд 8Адиабатный процесс
– это модель термодинамического процесса, происходящего в системе без теплообмена с
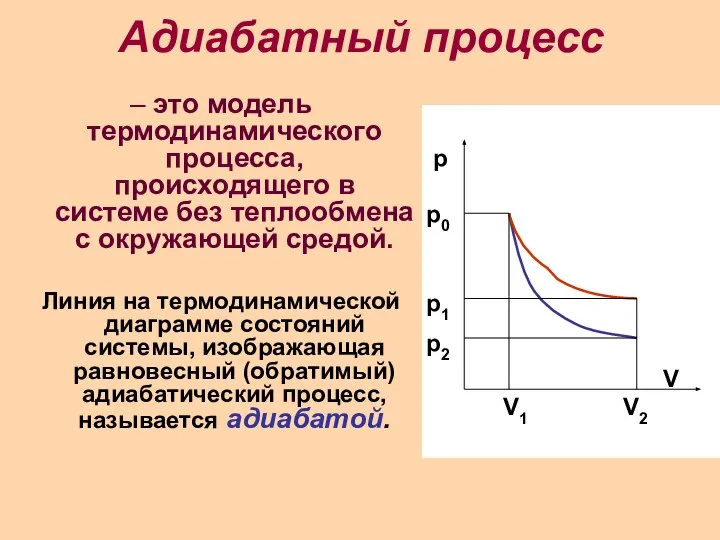
окружающей средой.
Линия на термодинамической диаграмме состояний системы, изображающая равновесный (обратимый) адиабатический процесс, называется адиабатой.
Слайд 9I закон термодинамики и изопроцессы
V
р
1
2
ИЗОТЕРМА
АДИАБАТА
V
р
2
1
Слайд 12Обратимый процесс
Это процесс, который может происходить как в прямом, так и в

обратном направлении
Обратимый процесс – это идеализация реального процесса.
Все макроскопические процессы проходят в определенном направлении
Слайд 13Необратимый процесс
Процесс, обратный которому самопроизвольно не происходит
Все макроскопические процессы являются необратимыми

Слайд 14Примеры
Кусок льда, внесенный в комнату, не отдает энергию окружающей среде и не

охлаждается
Маятник самостоятельно не наращивает амплитуду колебаний
Слайд 15Ни охлаждение льда в первом случае, ни увеличение амплитуды во втором не

противоречит ни закону сохранения энергии, ни законам механики. Оно противоречит лишь второму закону термодинамики
Слайд 16Второй закон термодинамики
В циклически действующем тепловом двигателе невозможно преобразовать все количество теплоты,

полученное от нагревателя, в механическую работу
Слайд 17Формулировка Р. Клаузиуса
Невозможно перевести тепло от более холодной системы к более горячей

при отсутствии одновременных изменений в обоих системах или окружающих телах
Слайд 18Формулировка У. Кельвина
Невозможно осуществить такой периодический процесс, единственным результатом которого было бы

совершение работы за счет теплоты взятой от одного источника
Слайд 19Статистическое истолкование второго закона термодинамики
Изолированная система самопроизвольно переходит из менее вероятного состояния

в более вероятное, или
Замкнутая система многих частиц самопроизвольно переходит из более упорядоченного состояния в менее упорядоченное

















 Электрические явления. Основные понятия
Электрические явления. Основные понятия Обобщающий урок по теме Электрический ток
Обобщающий урок по теме Электрический ток Статика
Статика Время и его измерение. Основы кинематики
Время и его измерение. Основы кинематики масс-1
масс-1 Оптическая дифракционная решетка
Оптическая дифракционная решетка Программируемые усилители
Программируемые усилители Параметрические цепи
Параметрические цепи Крыло конечного размаха
Крыло конечного размаха Презентация на тему Равнодействующие силы. Сила трения
Презентация на тему Равнодействующие силы. Сила трения  ОГЭ-2022 по физике. Задания, требования и изменения в сравнении с ОГЭ-2020
ОГЭ-2022 по физике. Задания, требования и изменения в сравнении с ОГЭ-2020 Құрамында талшықтары көп полимерлі композитті наноматериалдар
Құрамында талшықтары көп полимерлі композитті наноматериалдар Кинематика_ _Лекция 1_ (1)
Кинематика_ _Лекция 1_ (1) Чи довго пратимете
Чи довго пратимете Однофазные цепи
Однофазные цепи Относительность движения. Инерциальные системы отсчета. Первый закон Ньютона
Относительность движения. Инерциальные системы отсчета. Первый закон Ньютона Закон Ома для участка цепи
Закон Ома для участка цепи Свет как электромагнитная волна. Монохроматические цвета
Свет как электромагнитная волна. Монохроматические цвета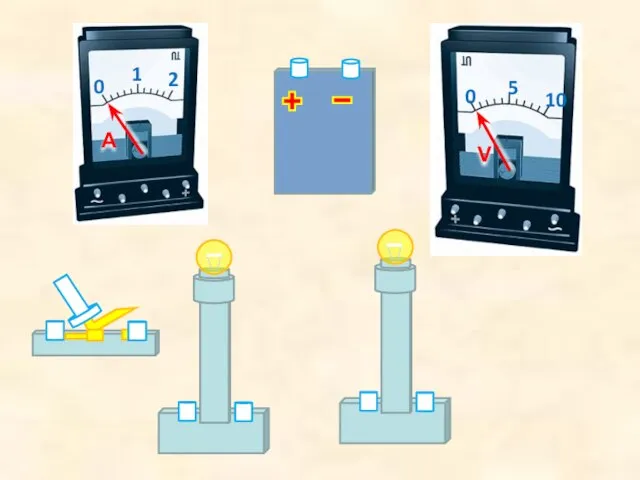 Презентация по физике "Последовательное соединенье проводников" -
Презентация по физике "Последовательное соединенье проводников" -  Ken Freese’s ’65 BJ-8 Piston Set DAMAGE. (29D motor)
Ken Freese’s ’65 BJ-8 Piston Set DAMAGE. (29D motor) Колебания и волны (ОГЭ). Решение задач 9 класс
Колебания и волны (ОГЭ). Решение задач 9 класс Открытие В.К. Рентгеном Х-лучей. Открытие А. Беккерелем явления радиоактивности
Открытие В.К. Рентгеном Х-лучей. Открытие А. Беккерелем явления радиоактивности Коэффициент полезного действия (КПД) тепловых двигателей
Коэффициент полезного действия (КПД) тепловых двигателей Лейденская банка. Опыт
Лейденская банка. Опыт Свойства дискретно-временного преобразования Фурье
Свойства дискретно-временного преобразования Фурье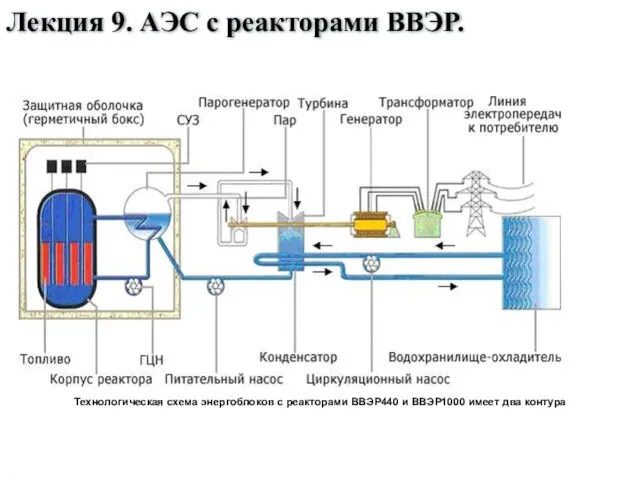 АЭС с реакторами ВВЭР. Лекция 9
АЭС с реакторами ВВЭР. Лекция 9 Автомобиль Lada Priora. Анализ дефекта Поломка шатуна
Автомобиль Lada Priora. Анализ дефекта Поломка шатуна Оптическая схема телескопа Ньютона. Занятие 20
Оптическая схема телескопа Ньютона. Занятие 20