Содержание
- 2. При синтезе необходимо обеспечить устойчивость системы с гигантской поверхностной энергией. Получение материала c требуемым размером кристаллов,
- 4. Переход в газовую фазу путем испарения, распыления, конденсации или химических реакций между компонентами газовой фазы. Также
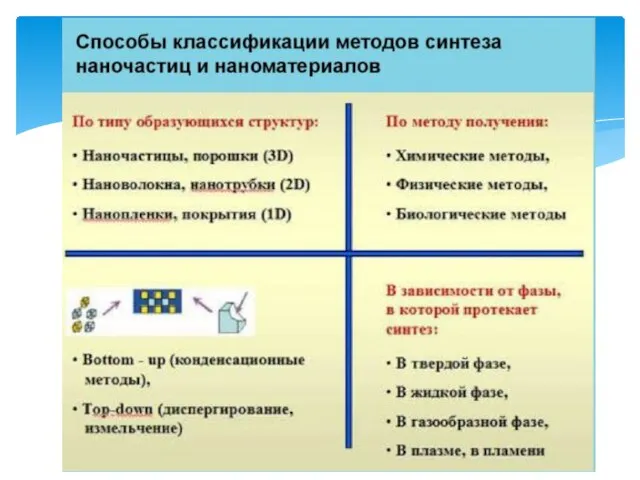
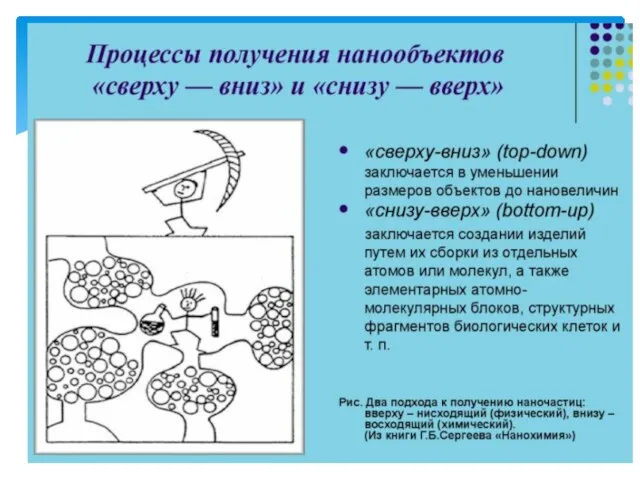
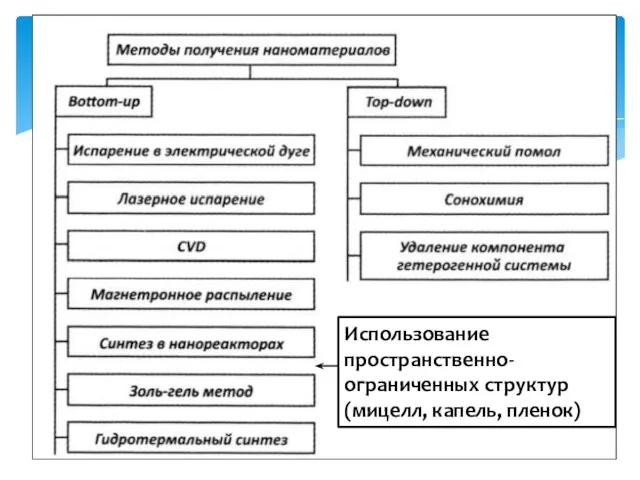
- 8. Методы получения
- 9. Процессы роста кристаллов где ∆GV 1-2 отнесено к единице объема новой фазы, r – радиус зародыша,
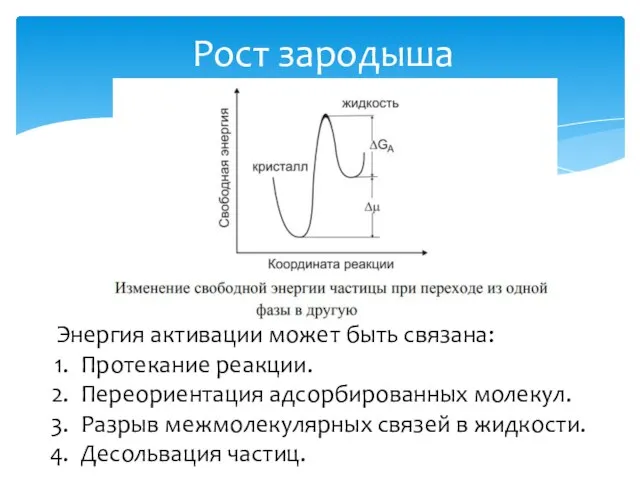
- 10. Рост зародыша Энергия активации может быть связана: Протекание реакции. Переориентация адсорбированных молекул. Разрыв межмолекулярных связей в
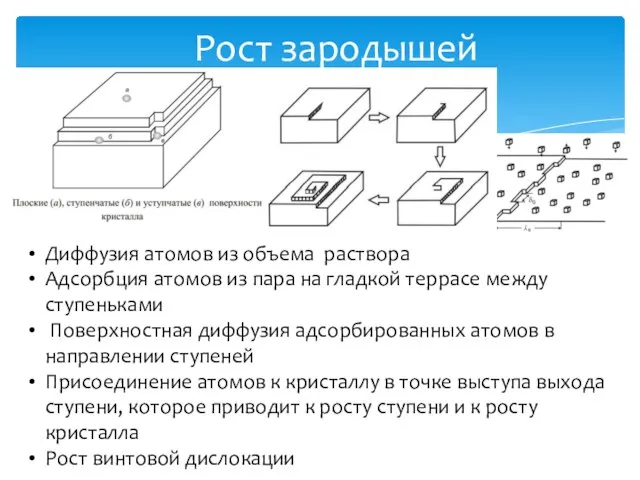
- 11. Рост зародышей Диффузия атомов из объема раствора Адсорбция атомов из пара на гладкой террасе между ступеньками
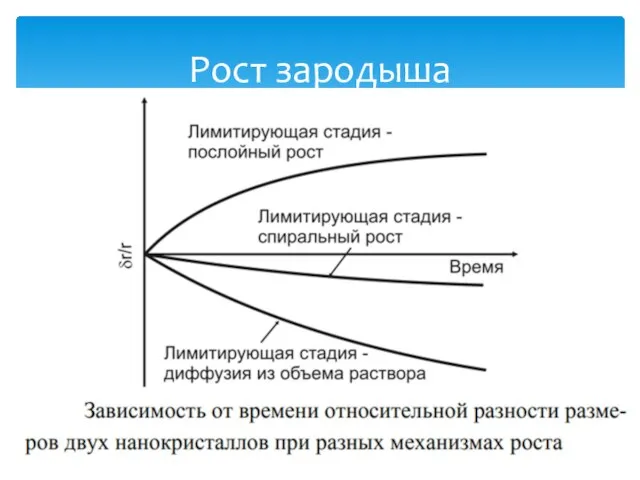
- 12. Рост зародыша
- 13. Когда зародыш мал, скорость роста лимитируется процессом послойного роста. В маленьком кристалле возникновение винтовой дислокации невозможно.
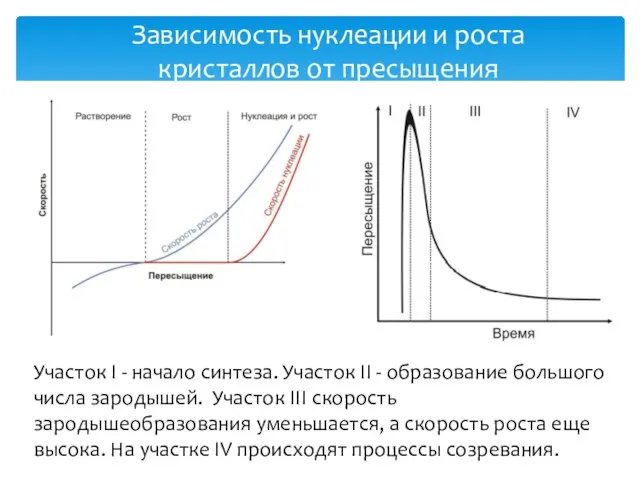
- 14. Зависимость нуклеации и роста кристаллов от пресыщения Участок I - начало синтеза. Участок II - образование
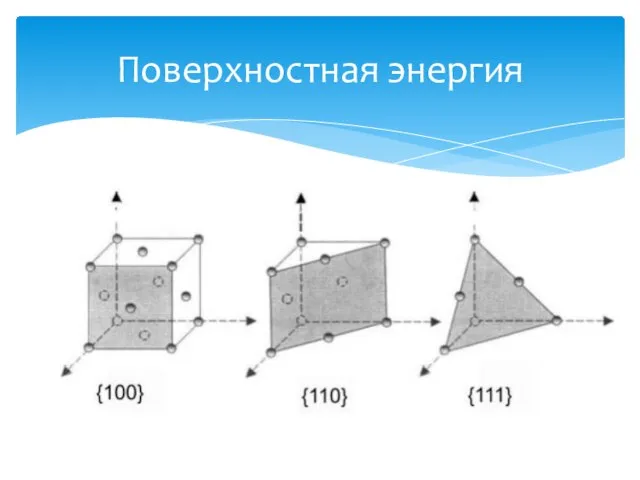
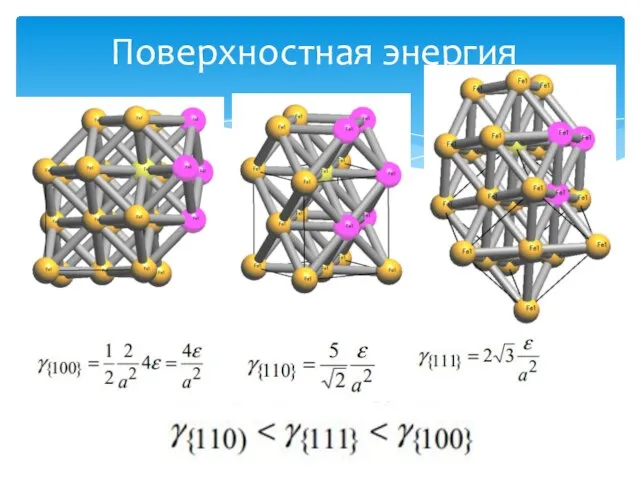
- 15. Поверхностная энергия
- 16. Поверхностная энергия
- 17. Поверхностная энергия
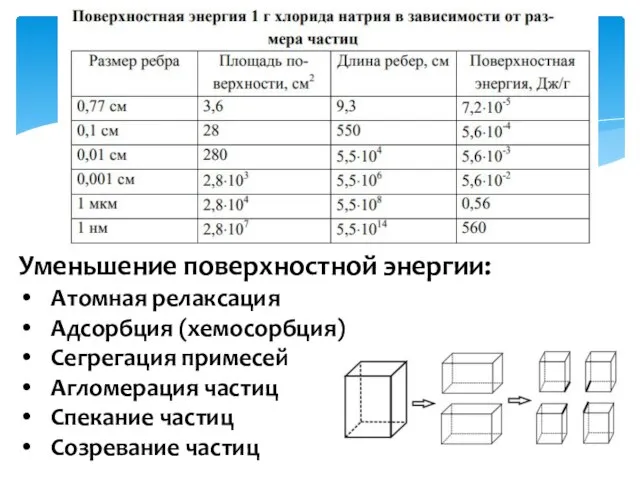
- 18. Уменьшение поверхностной энергии: Атомная релаксация Адсорбция (хемосорбция) Сегрегация примесей Агломерация частиц Спекание частиц Созревание частиц
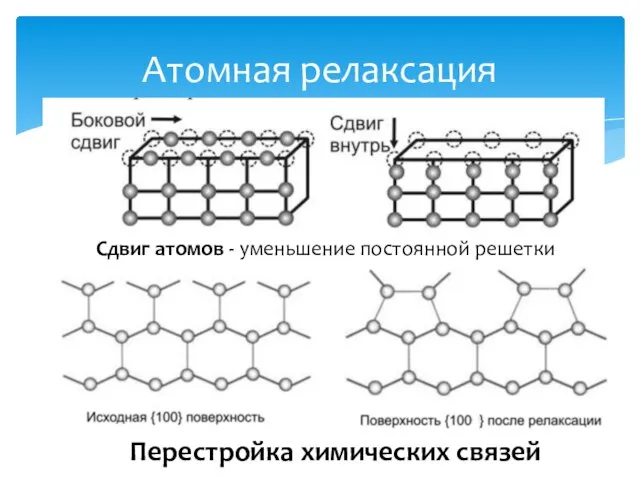
- 19. Атомная релаксация Сдвиг атомов - уменьшение постоянной решетки Перестройка химических связей
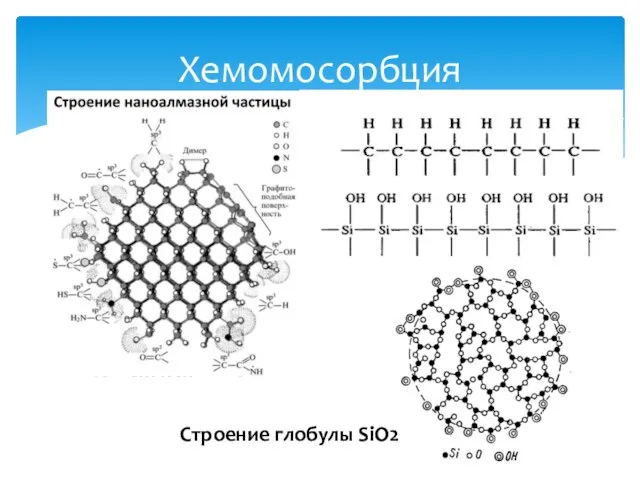
- 20. Хемомосорбция Строение глобулы SiO2
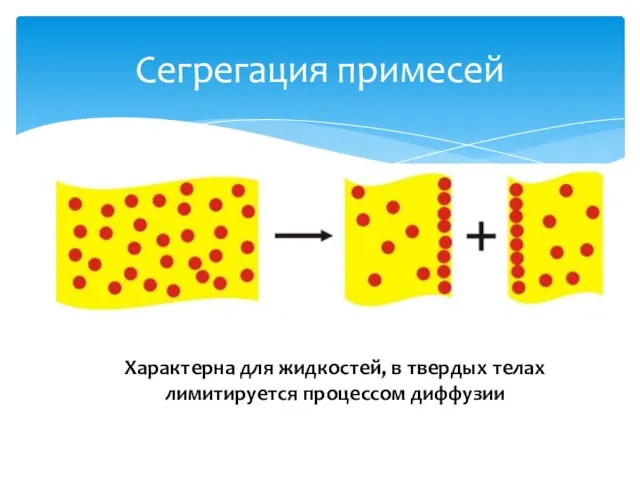
- 21. Сегрегация примесей Характерна для жидкостей, в твердых телах лимитируется процессом диффузии
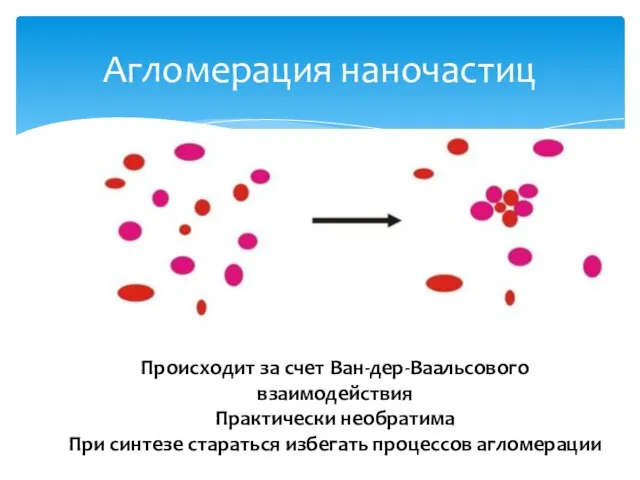
- 22. Агломерация наночастиц Происходит за счет Ван-дер-Ваальсового взаимодействия Практически необратима При синтезе стараться избегать процессов агломерации
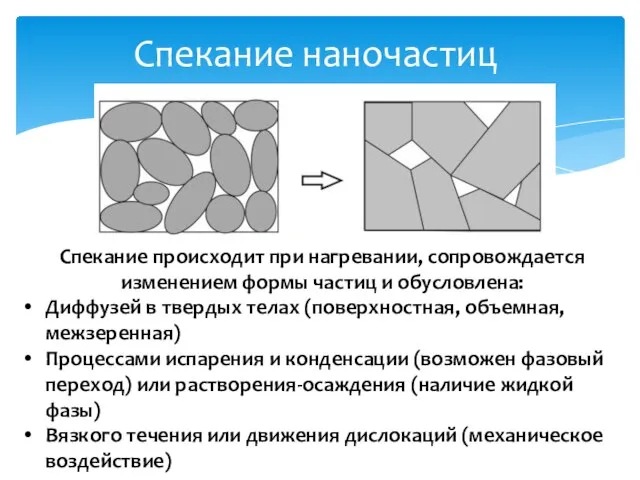
- 23. Спекание наночастиц Спекание происходит при нагревании, сопровождается изменением формы частиц и обусловлена: Диффузей в твердых телах
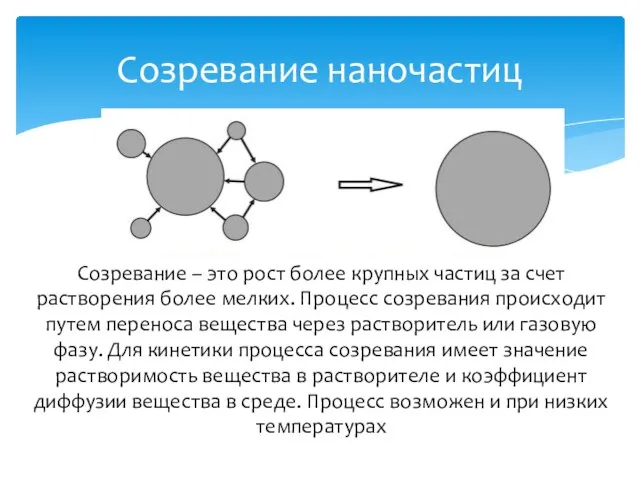
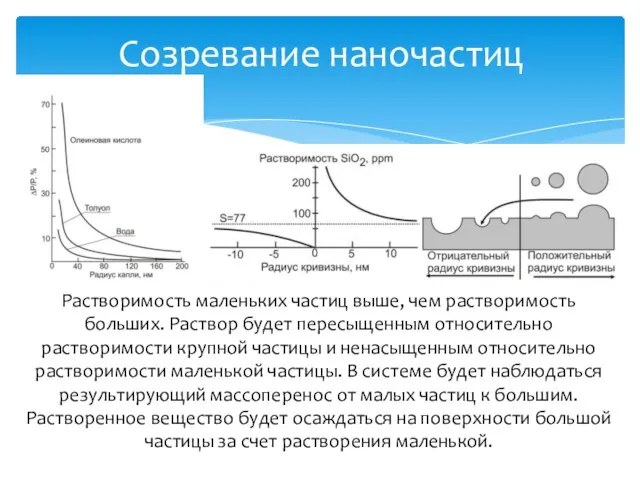
- 24. Созревание наночастиц Созревание – это рост более крупных частиц за счет растворения более мелких. Процесс созревания
- 25. Созревание наночастиц Растворимость маленьких частиц выше, чем растворимость больших. Раствор будет пересыщенным относительно растворимости крупной частицы
- 26. Роль процесса созревания наночастиц
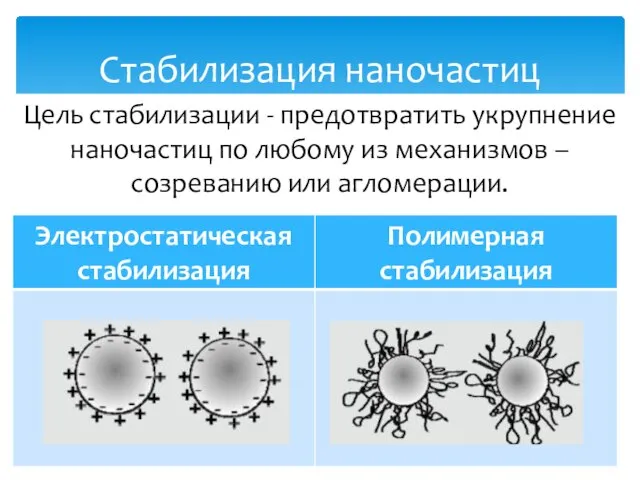
- 27. Стабилизация наночастиц Цель стабилизации - предотвратить укрупнение наночастиц по любому из механизмов – созреванию или агломерации.
- 28. Электростатическая стабилизация Электрический заряд, обусловлен: 1. Адсорбция и десорбция ионов 2. Диссоциация поверхностных групп 3. Изоморфное
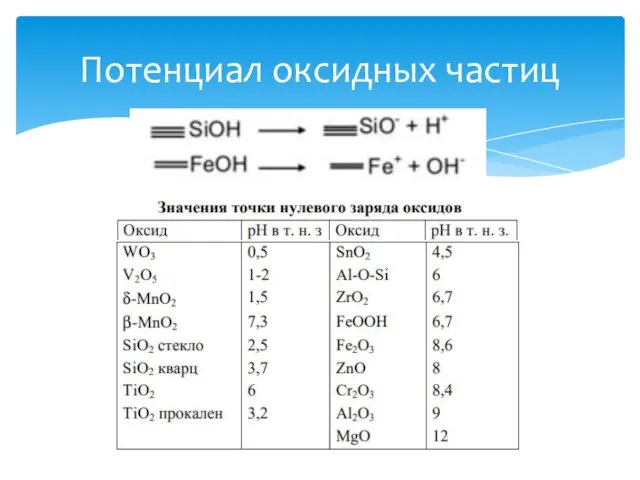
- 29. Потенциал оксидных частиц
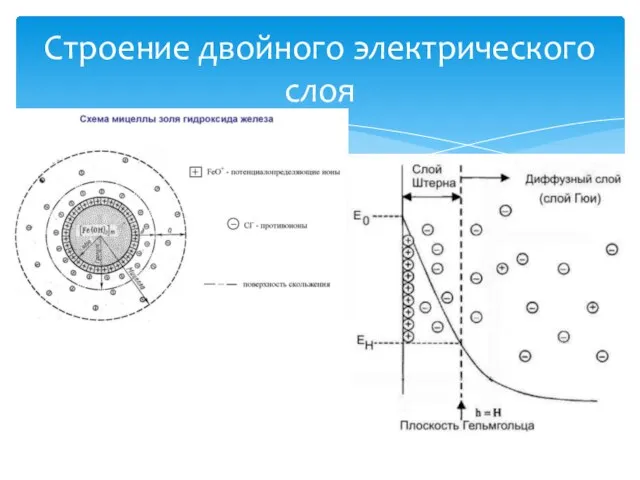
- 30. Строение двойного электрического слоя
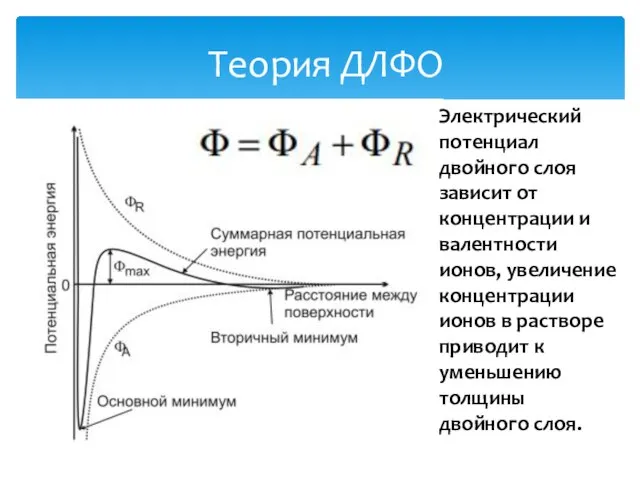
- 31. Теория ДЛФО Электрический потенциал двойного слоя зависит от концентрации и валентности ионов, увеличение концентрации ионов в
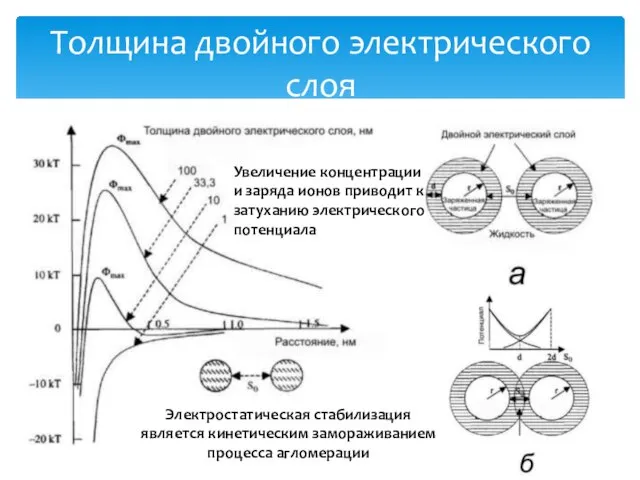
- 32. Толщина двойного электрического слоя Электростатическая стабилизация является кинетическим замораживанием процесса агломерации Увеличение концентрации и заряда ионов
- 33. Электростатическая стабилизация 2FeCl3 + 3Ba(OH)2 = 2FeOOH↓ + 3BaCl2 + 2H2O FeCl3 + 3NH4OH = FeOOH↓
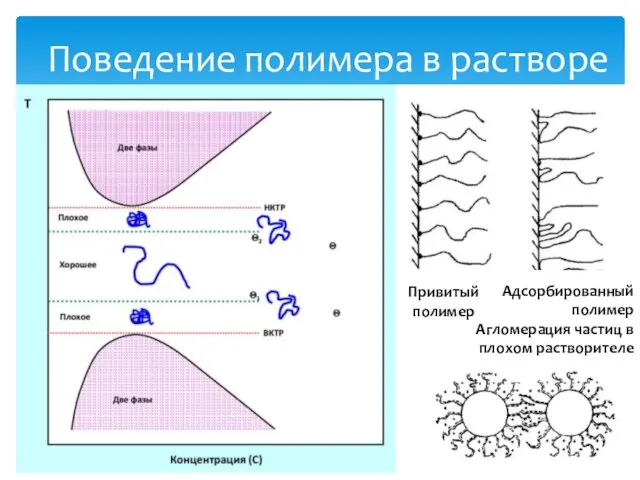
- 34. Поведение полимера в растворе Привитый полимер Адсорбированный полимер Агломерация частиц в плохом растворителе
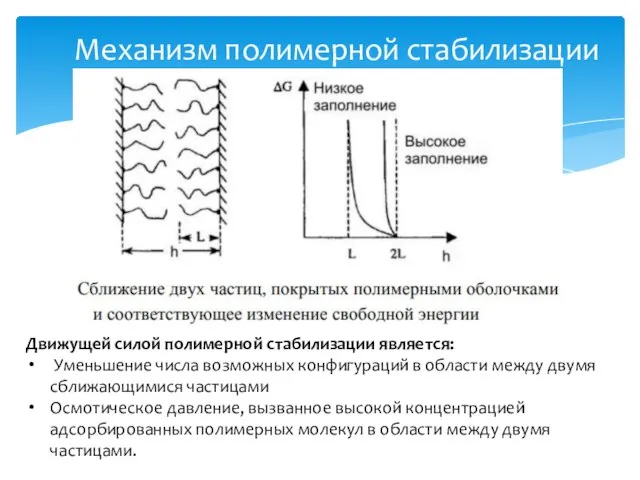
- 35. Механизм полимерной стабилизации Движущей силой полимерной стабилизации является: Уменьшение числа возможных конфигураций в области между двумя
- 37. Скачать презентацию










 Основные сведения о строении атома
Основные сведения о строении атома Сила тяжіння. Вага тіла. Невагомість
Сила тяжіння. Вага тіла. Невагомість Решение задач на вычисление значения сопротивления силы тока, напряжения в цепи переменного тока
Решение задач на вычисление значения сопротивления силы тока, напряжения в цепи переменного тока Серия автомобильных 2-стоечных подъемников грузоподъемностью 4 500 кг - RLP2-450
Серия автомобильных 2-стоечных подъемников грузоподъемностью 4 500 кг - RLP2-450 Динамика жидкости и твердого тела
Динамика жидкости и твердого тела Давление газов. Закон Паскаля
Давление газов. Закон Паскаля Конденсаторы. Схемы электрической цепи (Тест) (8 класс)
Конденсаторы. Схемы электрической цепи (Тест) (8 класс) Оборудование для ремонта бытовых электроприборов
Оборудование для ремонта бытовых электроприборов Гамма- излучение
Гамма- излучение Физическая викторина
Физическая викторина Ядерные реакции. Процесс столкновения микрочастицы с атомным ядром
Ядерные реакции. Процесс столкновения микрочастицы с атомным ядром Газовая хроматография
Газовая хроматография Электроемкость, конденсаторы
Электроемкость, конденсаторы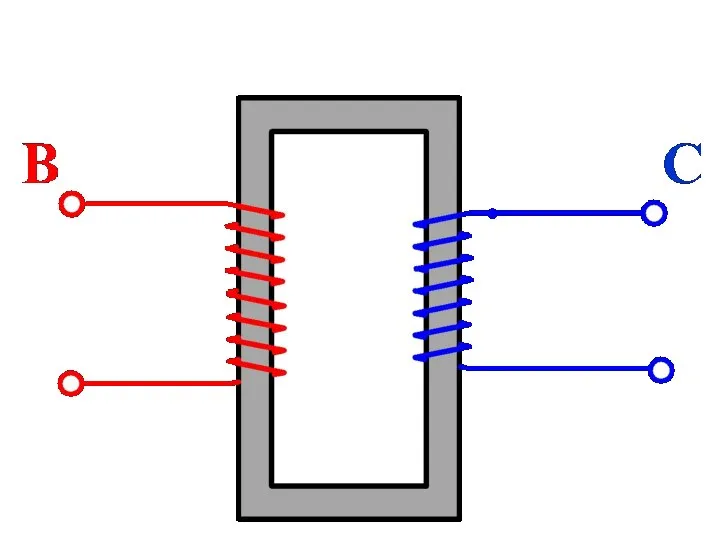 Автотрансформаторы
Автотрансформаторы Сила
Сила Построение структур, обобщенные параметры, классификация и расчет составов ДНПКМ. Лекция 5
Построение структур, обобщенные параметры, классификация и расчет составов ДНПКМ. Лекция 5 Динамика. Сила
Динамика. Сила Законы отражения света. Свойства изображения в плоском зеркале. Законы преломления
Законы отражения света. Свойства изображения в плоском зеркале. Законы преломления Реактивная сила
Реактивная сила Научно-исследовательская работа. Парадоксы физики
Научно-исследовательская работа. Парадоксы физики Потенциальная энергия. (Лекция 4)
Потенциальная энергия. (Лекция 4) Режимы движения жидкости. Лекция 3
Режимы движения жидкости. Лекция 3 Закон сохранения импульса
Закон сохранения импульса Стихотворение Ученье - свет, а не ученье - тьма
Стихотворение Ученье - свет, а не ученье - тьма Презентация на тему Взаимодействие тел
Презентация на тему Взаимодействие тел  Закон вращательного движения абсолютно твердого тела. Гироскоп
Закон вращательного движения абсолютно твердого тела. Гироскоп Презентация на тему Эрнест Резерфорд. Планетарная модель атома
Презентация на тему Эрнест Резерфорд. Планетарная модель атома  Сила. Сила тяжести
Сила. Сила тяжести