Слайд 3Всё началось с Гаммета
Луис Плак Гаммет (1894-1987) – крупнейший
американсткий химик. Выпускник

Гарвардского университета.
С 1923 по 1961г. преподавал в Колумбийском университете.
Л.Гаммет считается основателем физической органической
химии. Разработал специальный подход к описанию скоростей
кислотнокатализируемых реакций (функция кислотности
Гаммета), разработал методы оценки эффектов заместителей
(константы заместителей Гаммета), ввел уравнение,
связывающее эффекты заместителей с константами скоростей и
равновесия реакций (уравнение Гаммета).
Автор монографии
«Основы физической органической химии» (М.: Мир, 1972),
которую называют «библией для думающих химиков-
органиков».
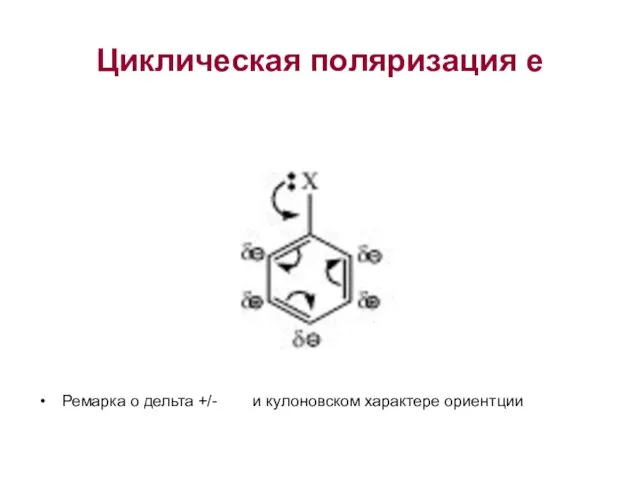
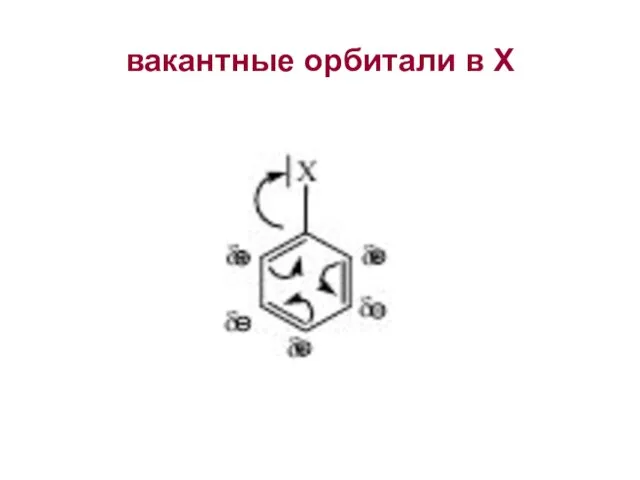
Слайд 4Циклическая поляризация е
Ремарка о дельта +/- и кулоновском характере ориентции
Слайд 6Иллюзии в оргхимии
Представления о циклической поляризации бензольного ядра заместителей различной природы позволяют

согласовать многие экспериментальные данные с электронной природой заместителей.
Тем не менее они являются не более чем иллюзией. Истинной причиной появления неравномерного распределения электронной плотности в бензольном ядре при введении в него заместителей является формирование новых молекулярных орбиталей, которое и влечет за собой изменение зарядов на атомах углерода.
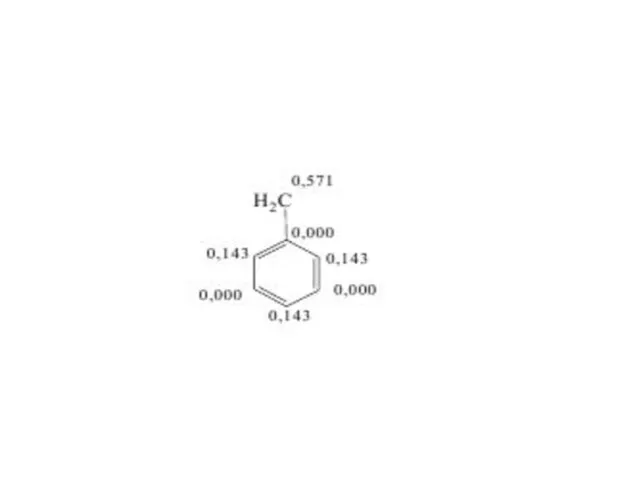
Слайд 9
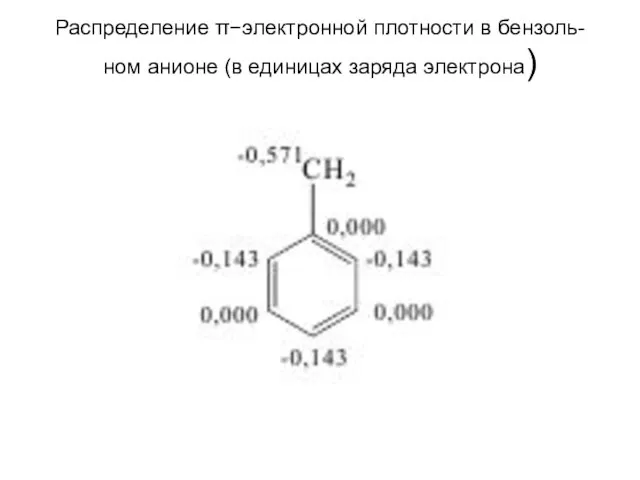
Распределение π−электронной плотности в бензоль-
ном анионе (в единицах заряда электрона)
Слайд 10Распределение электронной плотности (в единицах
заряда электрона) в молекуле анилина, полученное при
использовании: а
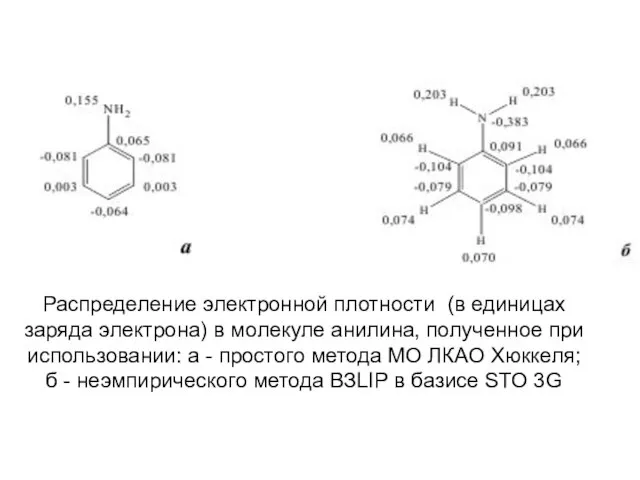
- простого метода МО ЛКАО Хюккеля;
б - неэмпирического метода ВЗLIP в базисе STO 3G
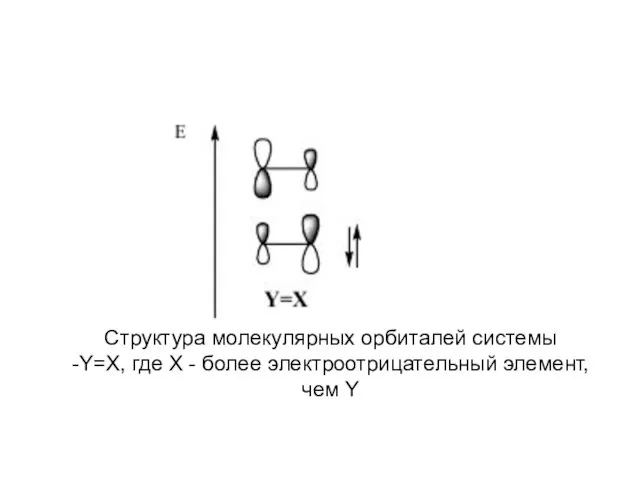
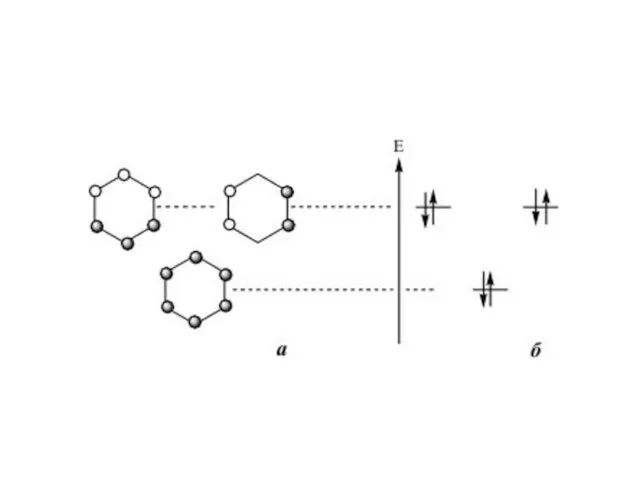
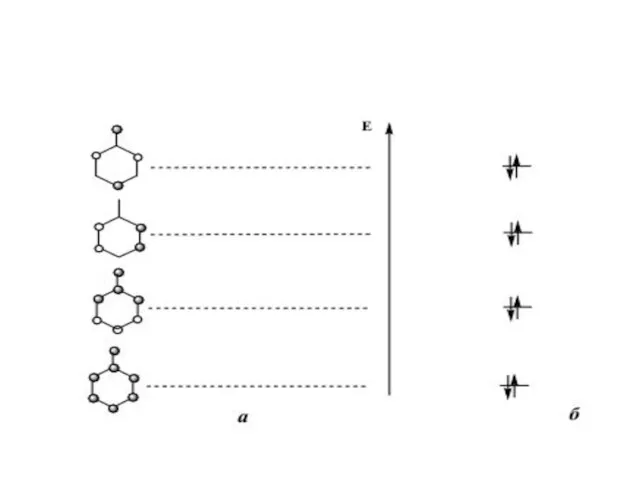
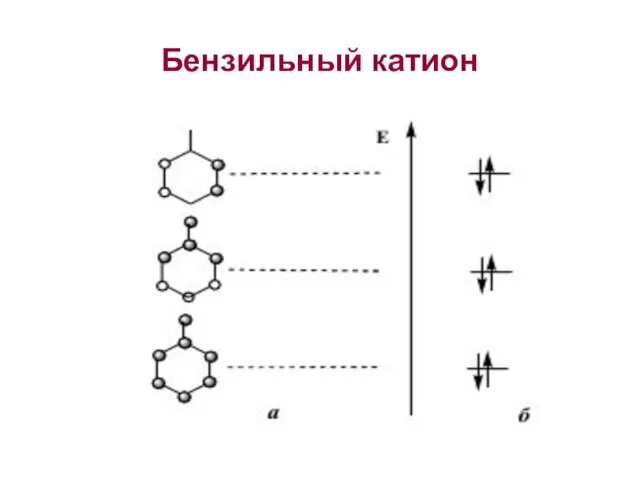
Слайд 13Структура молекулярных орбиталей системы
-Y=X, где Х - более электроотрицательный элемент,
чем Y







 Движение тела брошенного под углом к горизонту. Повторение, решение задач (10 класс)
Движение тела брошенного под углом к горизонту. Повторение, решение задач (10 класс) Получение радиоактивных изотопов и их применение
Получение радиоактивных изотопов и их применение Электромагнитные излучения
Электромагнитные излучения Посадки. Основы построения и расчет предельных отклонений
Посадки. Основы построения и расчет предельных отклонений Електричний струм – упорядковий рух зарядженних частинок
Електричний струм – упорядковий рух зарядженних частинок Главные центральные оси сечения
Главные центральные оси сечения Презентация на тему Скорость механического движения
Презентация на тему Скорость механического движения  Теплопроводность
Теплопроводность Простые механизмы. Рычаг
Простые механизмы. Рычаг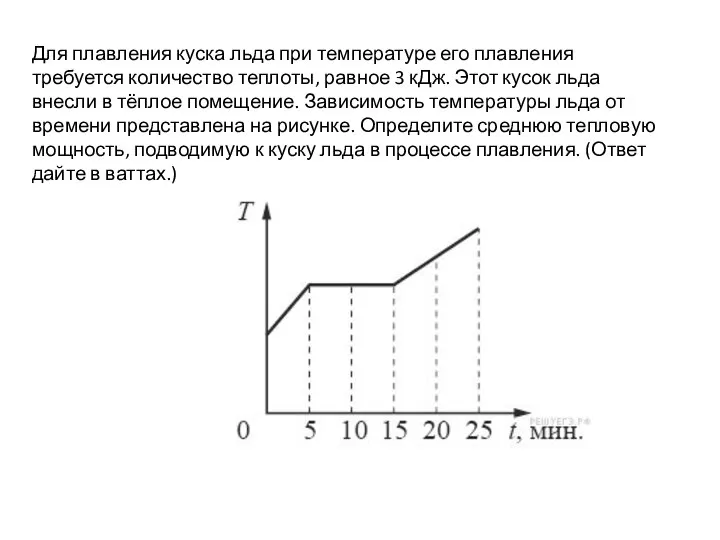 Определение тепловой мощности. ВПР, 9 класс
Определение тепловой мощности. ВПР, 9 класс Презентация на тему Инфракрасное излучение
Презентация на тему Инфракрасное излучение 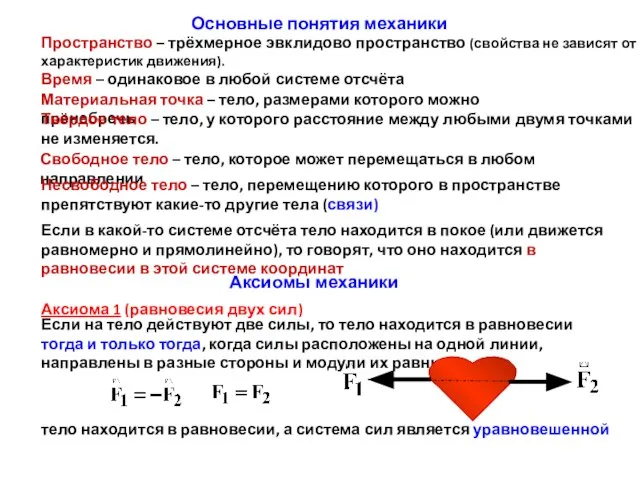 Аксиомы механики
Аксиомы механики Система управления двигателем
Система управления двигателем Электроемкость. Конденсаторы
Электроемкость. Конденсаторы Светодиодный светильник
Светодиодный светильник Тепловые двигатели
Тепловые двигатели №1 Практикалық жұмыс. Бейтараптану реакциясының жылу эффектісін есептеу
№1 Практикалық жұмыс. Бейтараптану реакциясының жылу эффектісін есептеу Инфракрасное, ультрафиолетовое, рентгеновское излучения
Инфракрасное, ультрафиолетовое, рентгеновское излучения 1f712686a0a73c13b3172265a60c76b1
1f712686a0a73c13b3172265a60c76b1 Атомные спектры
Атомные спектры Основы гидродинамического подобия. Лекция №5
Основы гидродинамического подобия. Лекция №5 Работа и мощность. Задачи
Работа и мощность. Задачи Элементы релятивистской механики (продолжение). Лекция № 9
Элементы релятивистской механики (продолжение). Лекция № 9 Строение атома. Опыты Резерфорда
Строение атома. Опыты Резерфорда Судовые двигатели внутреннего сгорания. Лекция 11
Судовые двигатели внутреннего сгорания. Лекция 11 Реактивное движение
Реактивное движение Оптические приборы
Оптические приборы Жоғары рұқсат етілім литографиясы
Жоғары рұқсат етілім литографиясы