Содержание
- 2. Закон сохранения энергии Энергия в природе не возникает из ничего и не исчезает: количество энергии неизменно,
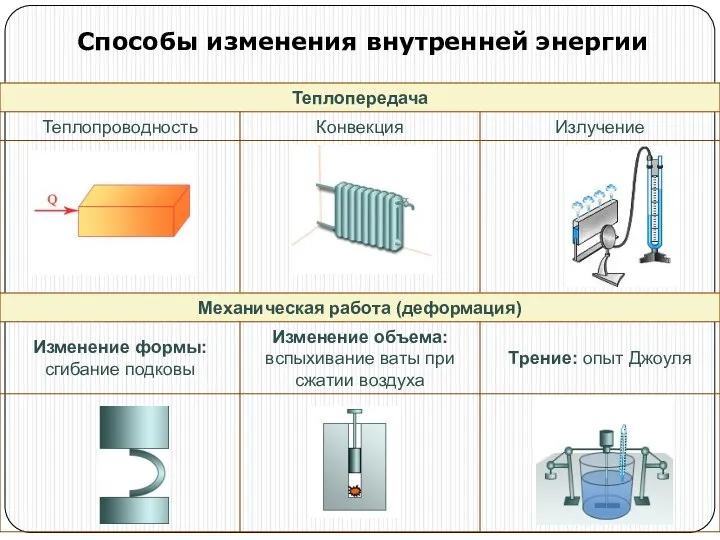
- 3. Способы изменения внутренней энергии
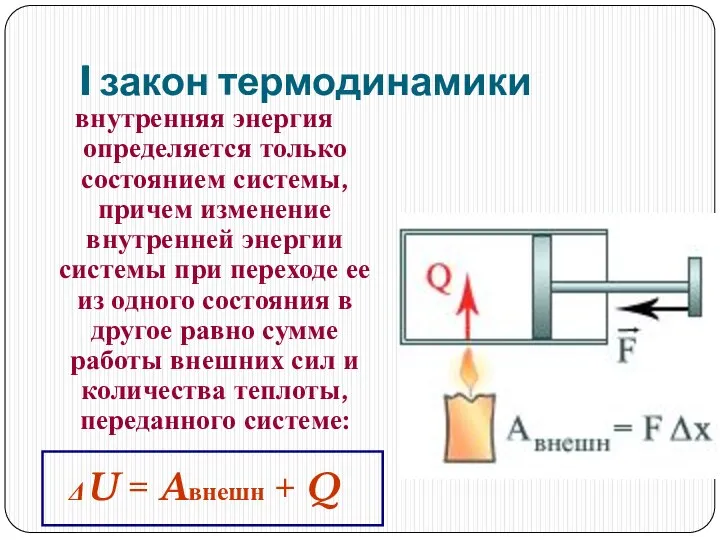
- 4. I закон термодинамики внутренняя энергия определяется только состоянием системы, причем изменение внутренней энергии системы при переходе
- 5. Если при нагревании газ расширяется и при этом совершает работу A, то первый закон термодинамики можно
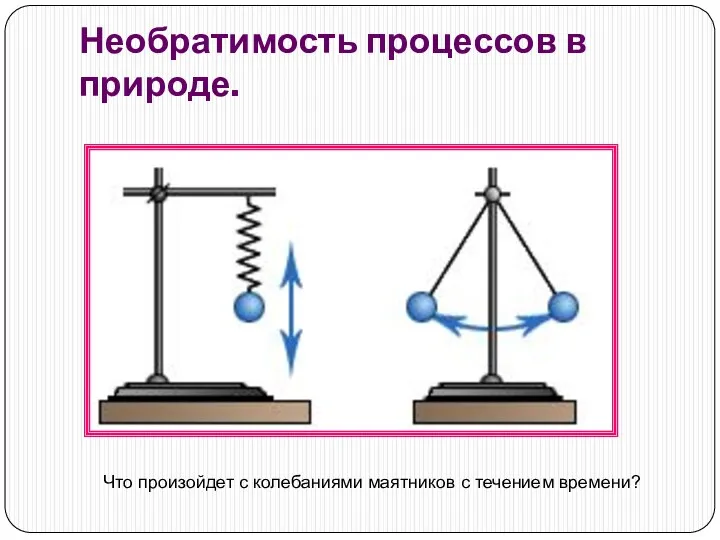
- 6. Необратимость процессов в природе. Необратимые – процессы, которые могут самопроизвольно протекать только в одном направлении. В
- 7. Необратимость процессов в природе. Что произойдет с колебаниями маятников с течением времени?
- 8. Необратимость процессов в природе.
- 9. Необратимость процессов в природе.
- 10. Необратимость процессов в природе. Все процессы в природе НЕОБРАТИМЫ!
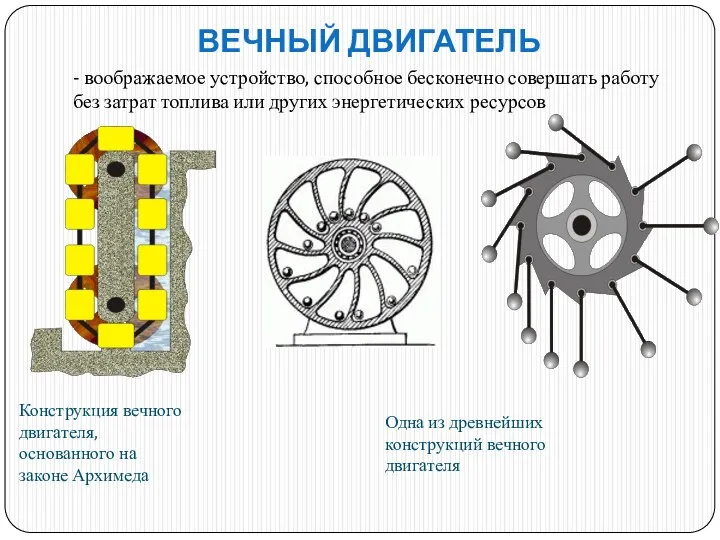
- 11. - воображаемое устройство, способное бесконечно совершать работу без затрат топлива или других энергетических ресурсов Одна из
- 12. ПОЧЕМУ НЕВОЗМОЖНО СОЗДАТЬ ВЕЧНЫЙ ДВИГАТЕЛЬ?
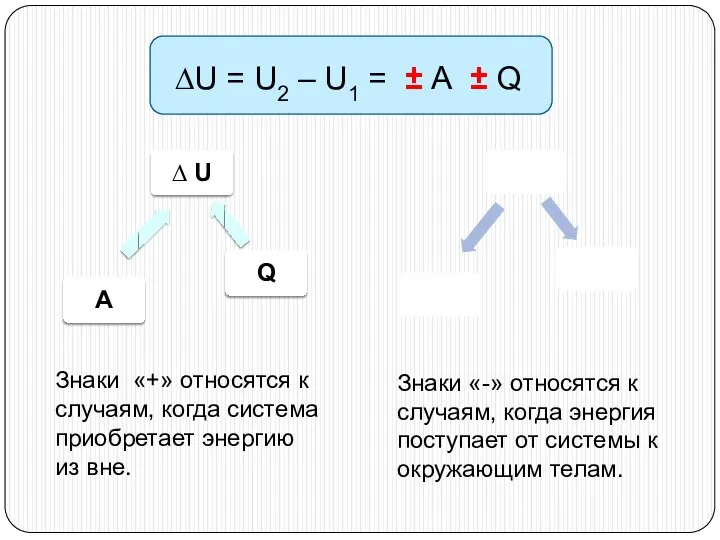
- 13. Изменение внутренней энергии системы при переходе её из одного состояния в другое равно сумме работы внешних
- 14. Знаки «+» относятся к случаям, когда система приобретает энергию из вне. Знаки «-» относятся к случаям,
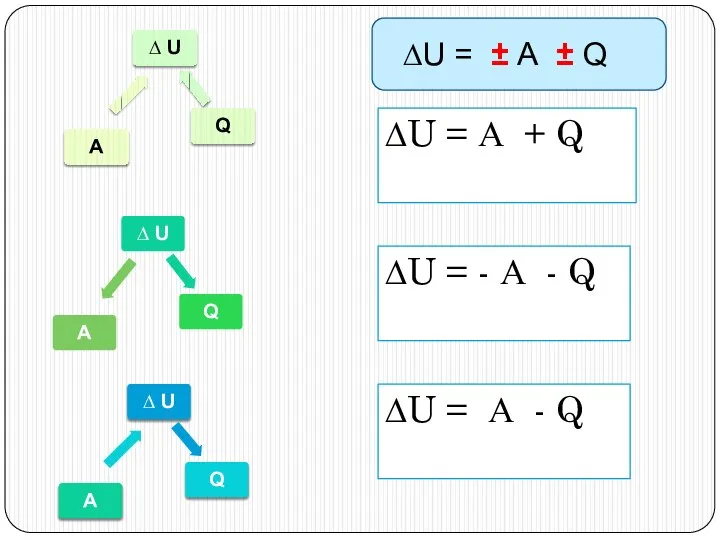
- 15. ∆U = А + Q ∆U = - А - Q ∆U = А - Q
- 16. Газ в сосуде сжали, совершив работу 25 Дж. Внутренняя энергия газа при этом увеличилась на 30
- 17. В тепловом двигателе газ получил 300 Дж тепла и совершил работу 36 Дж. Как изменилась внутренняя
- 18. Чему равно изменение внутренней энергии газа, если ему передано количество теплоты 300 Дж и внешние силы
- 20. Скачать презентацию











 Презентация на тему Конвекция
Презентация на тему Конвекция  Однофазный синусоидальный ток
Однофазный синусоидальный ток Система охлаждения двигателя
Система охлаждения двигателя Давление газа
Давление газа Магнитные свойства вещества. Сила Лоренца
Магнитные свойства вещества. Сила Лоренца Исследование радиального профиля параметров активной среды лазеров с разрядом в полом катоде
Исследование радиального профиля параметров активной среды лазеров с разрядом в полом катоде 14 Лучистый теплообмен. Расчёт угловых коэффициентов. Казаков +
14 Лучистый теплообмен. Расчёт угловых коэффициентов. Казаков + Геометрическая оптика. Свет. Источники света
Геометрическая оптика. Свет. Источники света Проектирование компрессорных установок горных предприятий. Занятие 7
Проектирование компрессорных установок горных предприятий. Занятие 7 Источники света. Прямолинейное распространение света
Источники света. Прямолинейное распространение света Инерция
Инерция Учимся мыслить
Учимся мыслить Деление ядер урана
Деление ядер урана Генератор 2ГВ-008
Генератор 2ГВ-008 Движение и его относительность
Движение и его относительность Электричество. Простейшая электрическая цепь. Первая помощь при ударе электрическим током
Электричество. Простейшая электрическая цепь. Первая помощь при ударе электрическим током Радиоактивные превращения. Экспериментальные методы исследования частиц
Радиоактивные превращения. Экспериментальные методы исследования частиц Звездный час (викторина)
Звездный час (викторина) Презентация на тему Планетарная модель атома
Презентация на тему Планетарная модель атома  Поглощенная доза излучения. Основы дозиметрии
Поглощенная доза излучения. Основы дозиметрии Подготовка к ЕГЭ на уроках физики
Подготовка к ЕГЭ на уроках физики Динамика моря и Условия судоходства
Динамика моря и Условия судоходства Презентация на тему Колебательный контур
Презентация на тему Колебательный контур  Решение задач Закон сохранения энергии
Решение задач Закон сохранения энергии Испарение и конденсация
Испарение и конденсация Магнитное поле. Лекция 20
Магнитное поле. Лекция 20 Презентация на тему Построения в линзах
Презентация на тему Построения в линзах  Физика. Вводная лекция
Физика. Вводная лекция