Содержание
- 2. 1891 год Ирландский физик Стони вел понятие ЭЛЕКТРОН (по-гречески «янтарь») – частица, которая переносит электричество. Английский
- 3. 1897 год ДЖ. Томсон предложил модель атома – «Пудинг с изюмом» электрон +
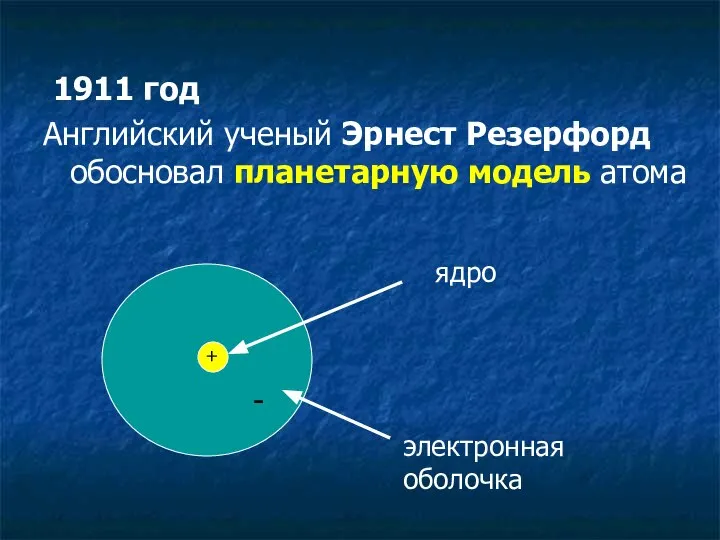
- 4. 1911 год Английский ученый Эрнест Резерфорд обосновал планетарную модель атома + ядро электронная оболочка -
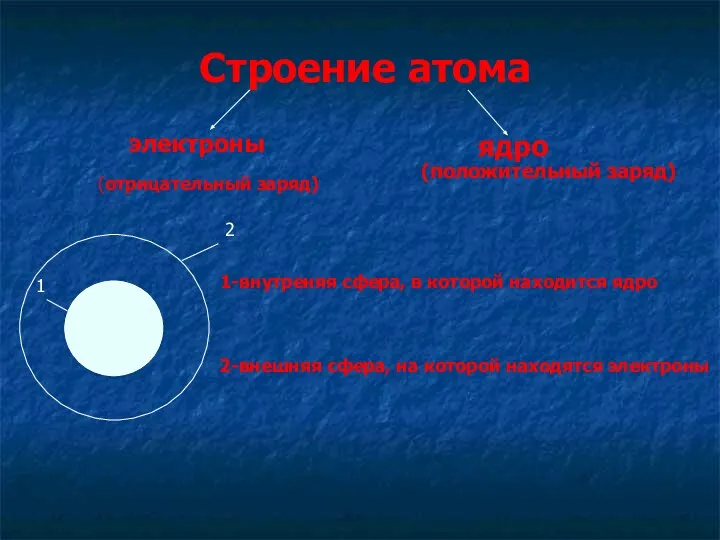
- 5. Строение атома электроны ядро 1-внутреняя сфера, в которой находится ядро 2-внешняя сфера, на которой находятся электроны
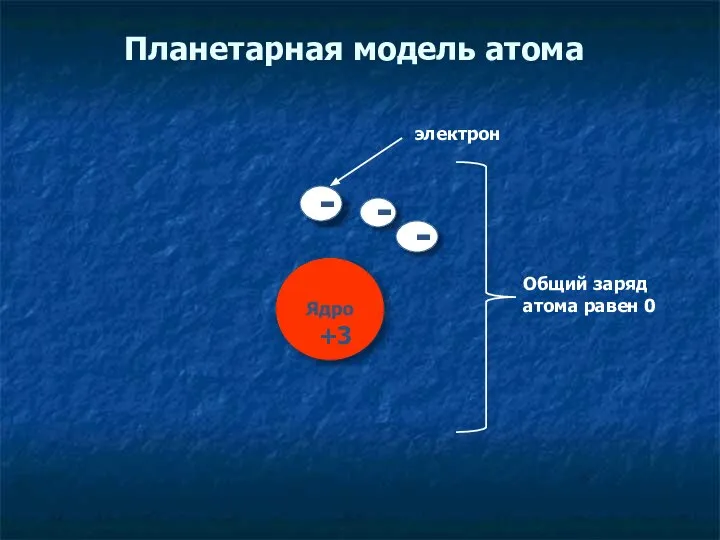
- 6. Планетарная модель атома электрон + Общий заряд атома равен 0 - 3 - -
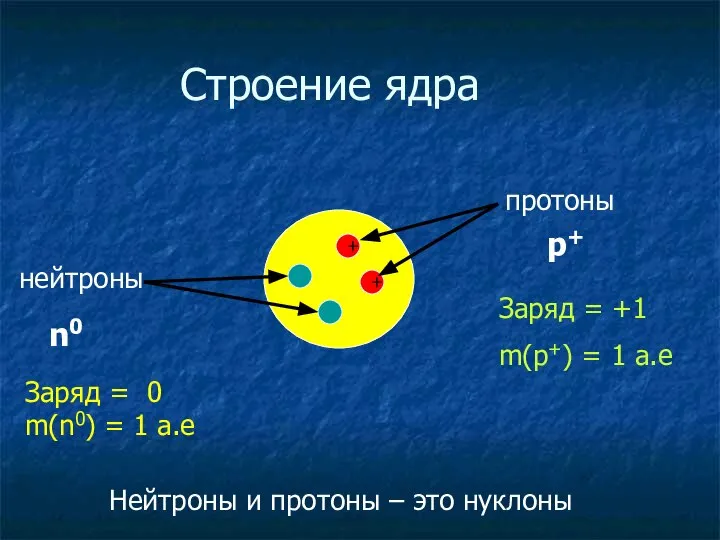
- 8. + + Строение ядра протоны нейтроны n0 p+ Заряд = +1 m(p+) = 1 a.e Заряд
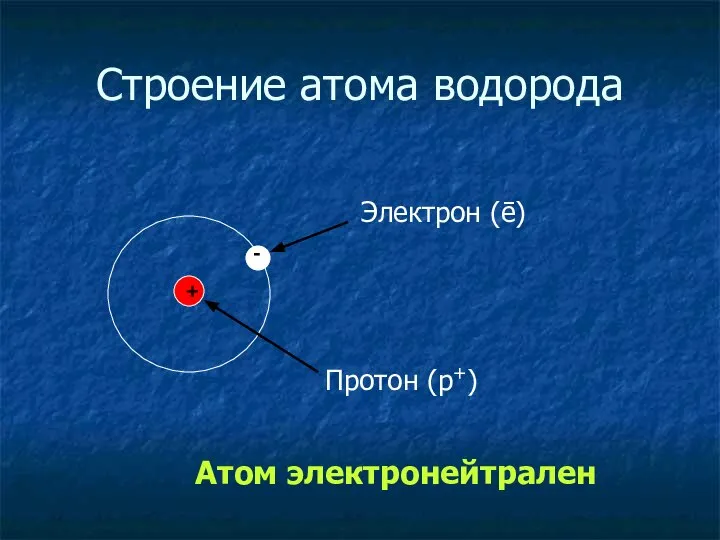
- 9. Строение атома водорода + - Протон (p+) Электрон (ē) Атом электронейтрален
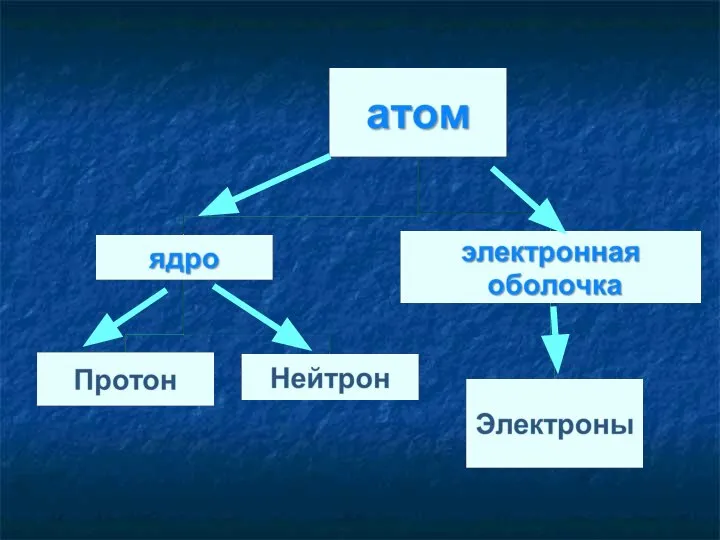
- 10. Современная модель атома Атом – электронейтральная частица Ядро атома – положительно заряженное Электроны – отрицательно заряженные
- 11. Число протонов = заряду атомного ядра = числу электронов = = порядковому номеру элемента Mg 12
- 12. Состав ядра атома Протоны. Масса = 1, заряд = +1 Нейтроны. Масса = 1, заряд =
- 13. Масса атома – это масса его ядра. Число протонов + число нейтронов = массовое число (А)
- 14. Задание Укажите состав атома натрия Na 11 23 p+ = 11 ē = 11 n0 =
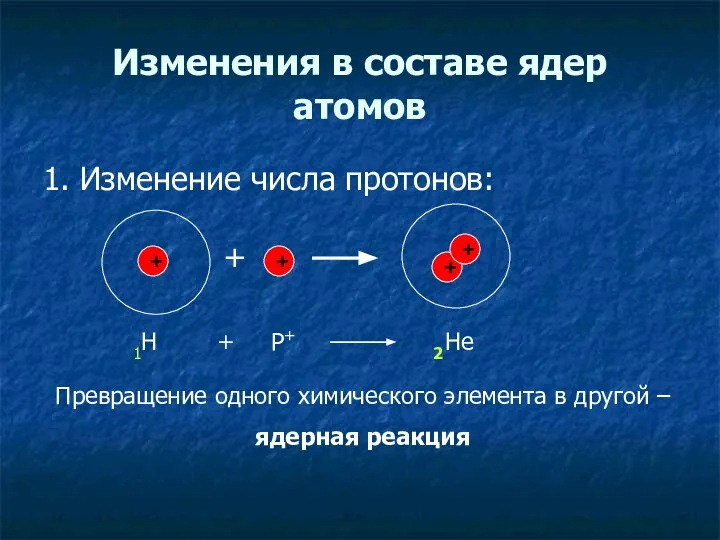
- 15. Изменения в составе ядер атомов 1. Изменение числа протонов: + + + + + 1Н Р+
- 16. Химический элемент – это вид атомов с одинаковым зарядом ядра (с одинаковым числом протонов в ядре)
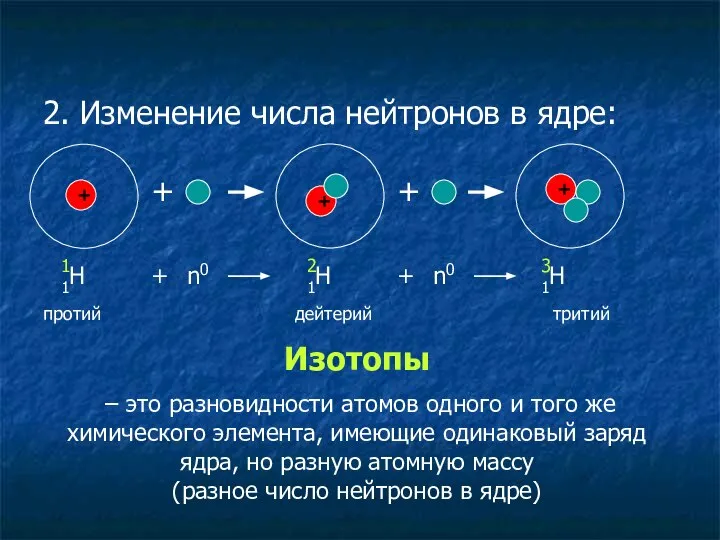
- 17. 2. Изменение числа нейтронов в ядре: + 1Н + + + + 1 + n0 1Н
- 18. 17 Сl 35 17 Сl 37 75% 25% Ar = 0.75 * 35 + 0.25 *
- 20. Скачать презентацию









 Презентация на тему Сила трения покоя
Презентация на тему Сила трения покоя  Закон радиоактивного распада. Период полураспада
Закон радиоактивного распада. Период полураспада Движение тела по окружности с постоянной по модулю скоростью
Движение тела по окружности с постоянной по модулю скоростью Второй закон Ньютона. Динамика материальной точки
Второй закон Ньютона. Динамика материальной точки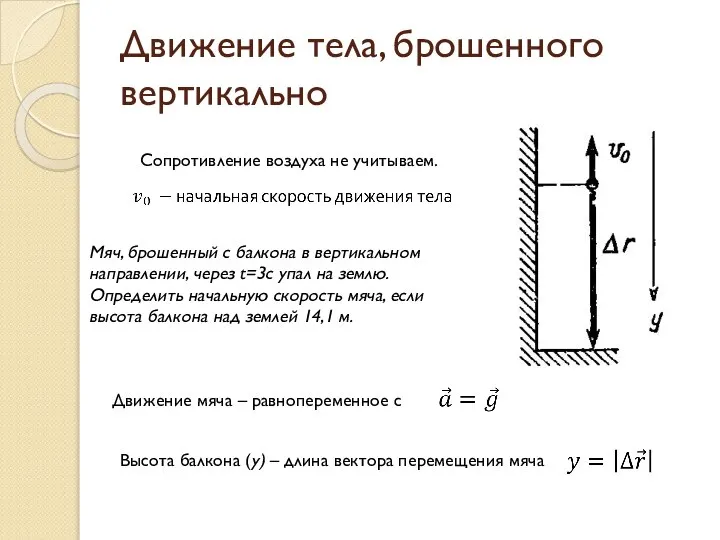 Движение тела, брошенного вертикально
Движение тела, брошенного вертикально Некоторые положения Теории относительности
Некоторые положения Теории относительности Перемещение при прямолинейном равноускоренном движении. Урок 1
Перемещение при прямолинейном равноускоренном движении. Урок 1 Расчёт аэродинамических характеристик самолётов
Расчёт аэродинамических характеристик самолётов Энергия заряженного конденсата
Энергия заряженного конденсата Переменное прямолинейное движение
Переменное прямолинейное движение Решение задач на закон электромагнитной индукции
Решение задач на закон электромагнитной индукции Презентация на тему Строение и свойства вещества
Презентация на тему Строение и свойства вещества  Control of nonlinear dynamics of electromechanical systems
Control of nonlinear dynamics of electromechanical systems Масса молекул. Количество вещества
Масса молекул. Количество вещества Классификация нагрузок
Классификация нагрузок Сообщающиеся сосуды
Сообщающиеся сосуды Соединения фитингами
Соединения фитингами Электромагнитная индукция
Электромагнитная индукция Теоретическая механика
Теоретическая механика Электрический ток. Источники тока
Электрический ток. Источники тока Специзмерения системах автоматики и телемеханики
Специзмерения системах автоматики и телемеханики Изучение явления электромагнитной индукции. Лабораторная работа
Изучение явления электромагнитной индукции. Лабораторная работа Магнитное поле
Магнитное поле Запись и воспроизведение звука
Запись и воспроизведение звука Фотоэффект
Фотоэффект Вечный двигатель в истории
Вечный двигатель в истории Физика. Вводная лекция
Физика. Вводная лекция Электроэнергетические системы и сети. Определение параметров элементов электрической сети
Электроэнергетические системы и сети. Определение параметров элементов электрической сети