Содержание
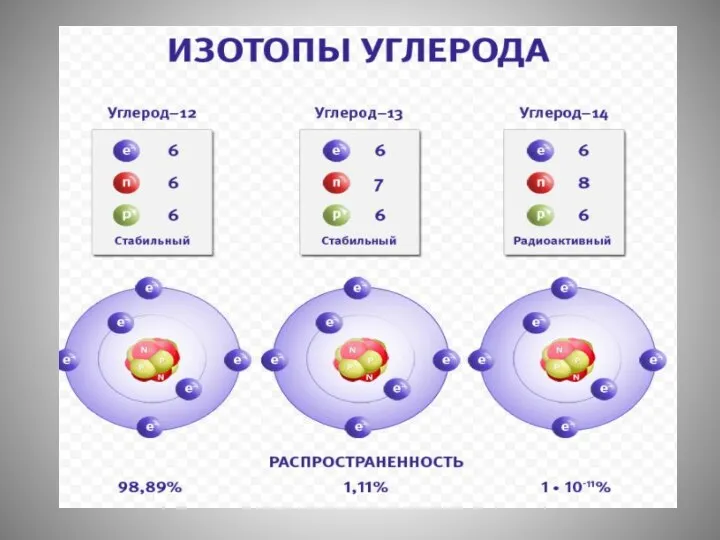
- 13. ИЗОТОПЫ Это объясняется существованием изотопов.
- 15. Название «изотопы» было предложено в 1912 английским радиохимиком Фредериком Содди, который образовал его из двух греческих
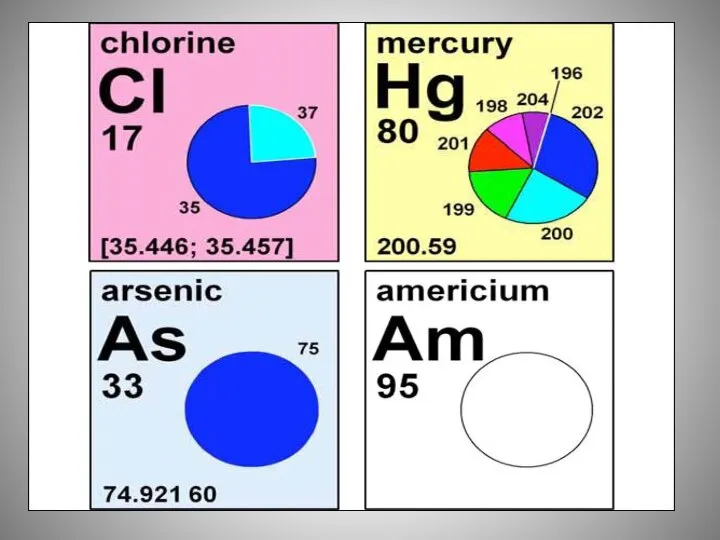
- 19. Наибольшее количество изотопов (по 36 у каждого) у ксенона (Xe), открыт в 1898 г. Рамзаем и
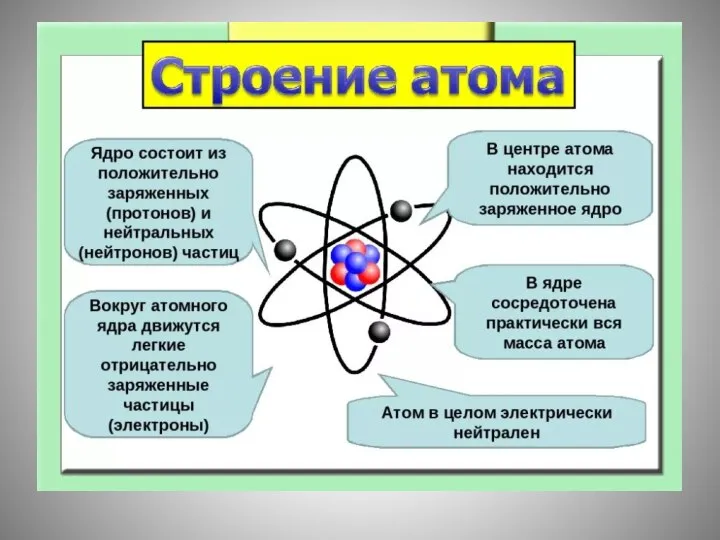
- 21. Обобщение Заряд ядра совпадает с порядковым номером элемента в периодической системе химических элементов Д. И. Менделеева.
- 23. Скачать презентацию














 Закон сохранения массы веществ
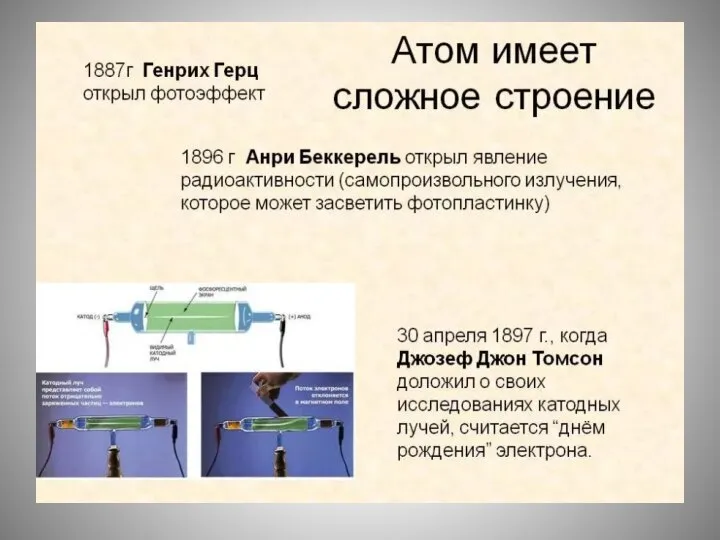
Закон сохранения массы веществ Строение атома. Опыты Резерфорда
Строение атома. Опыты Резерфорда Стакан-непроливайка
Стакан-непроливайка Автоматическое управление. Типовая упрощенная структура САУ
Автоматическое управление. Типовая упрощенная структура САУ Физические явления языком литературы
Физические явления языком литературы Реактивное движение в технике, животном и растительном мире. 10 класс
Реактивное движение в технике, животном и растительном мире. 10 класс Закон сохранения импульса
Закон сохранения импульса Соединения проводников. Задачи
Соединения проводников. Задачи Рулевое устройство судна
Рулевое устройство судна Импульс. Закон сохранения импульса
Импульс. Закон сохранения импульса Посадочный размер блока. Диаметр ТЭНа
Посадочный размер блока. Диаметр ТЭНа Итоговая контрольная работа
Итоговая контрольная работа Иллюзии и Физика. Вечная Борьба
Иллюзии и Физика. Вечная Борьба Внутренняя энергия. Агрегатные состояния вещества. Занятие 1. Часть 1
Внутренняя энергия. Агрегатные состояния вещества. Занятие 1. Часть 1 Относительность движения
Относительность движения Үйкеліс күшін зерттеу
Үйкеліс күшін зерттеу Преломление света. Закон преломления
Преломление света. Закон преломления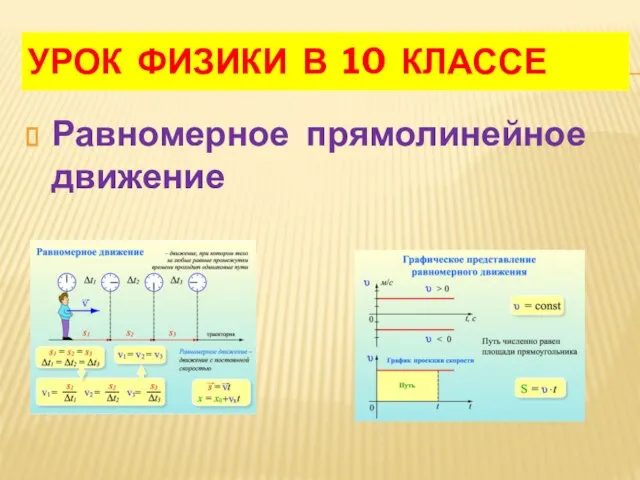 Урок4 РПД
Урок4 РПД Механика деформируемого твердого тела
Механика деформируемого твердого тела ЯМР-спектроскопия. Часть 1
ЯМР-спектроскопия. Часть 1 Строение атома
Строение атома Теплофизика процесса резания
Теплофизика процесса резания Курс физики в домашней школе ФОКСФОРД. Базовый уровень
Курс физики в домашней школе ФОКСФОРД. Базовый уровень High-speed Machining
High-speed Machining Изменение внутренней энергии газа в процессе теплообмена и совершения работы. Первое начало термодинамики. Лекция 5
Изменение внутренней энергии газа в процессе теплообмена и совершения работы. Первое начало термодинамики. Лекция 5 The atom
The atom Технология наночастиц металлов. Тема 4
Технология наночастиц металлов. Тема 4 Паровые двигатели
Паровые двигатели