Содержание
- 2. Гипотеза о том, что вещества состоят из большого числа атомов, зародилась свыше двух тысячелетий назад. Позиция
- 3. Конкретные представления о строении атома развивались по мере накопления физикой фактов о свойствах вещества 1887г. -
- 4. Сэр Джо́зеф Джон То́мсон (1856 - 1940) — английский физик, лауреат Нобелевской премии по физике 1906
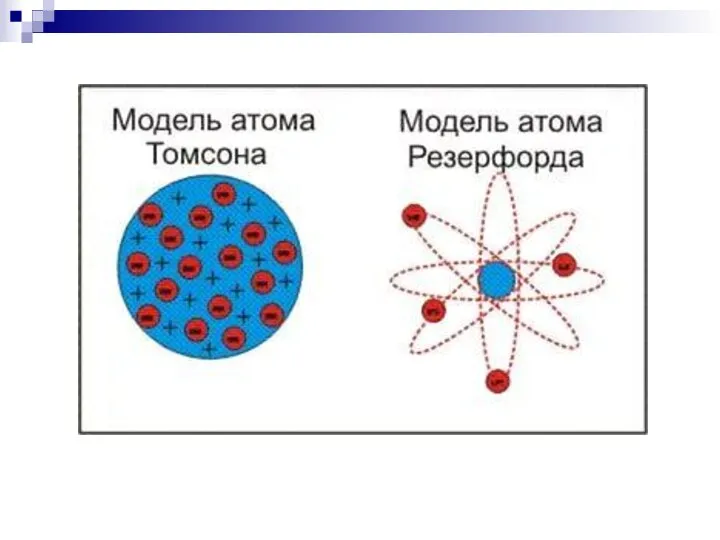
- 5. Модель строения атома Томсона Атом – шар, по всему объёму которого равномерно распределён положительный заряд. Внутри
- 6. Модель Томсона нуждалась в экспериментальной проверке. Важно было убедиться, действительно ли положительный заряд распределён по всему
- 7. Резерфорд Эрнест Резерфорд Эрнест (1871–1937) – английский физик, основоположник ядерной физики. Его исследования посвящены атомной и
- 8. Опыты Резерфорда 1906 г. Идея опыта Резерфорда: Зондировать атом альфа–частицами. Альфа-частицы возникают при распаде радия. Масса
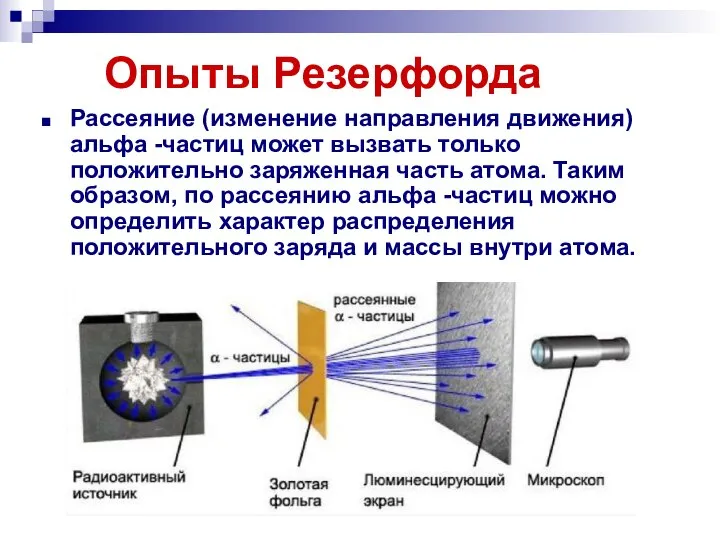
- 9. Опыты Резерфорда Рассеяние (изменение направления движения) альфа -частиц может вызвать только положительно заряженная часть атома. Таким
- 10. Опыты Резерфорда Модифицируя экспериментальную установку, Резерфорд попытался обнаружить отклонение альфа -частиц на большие углы. Для этого
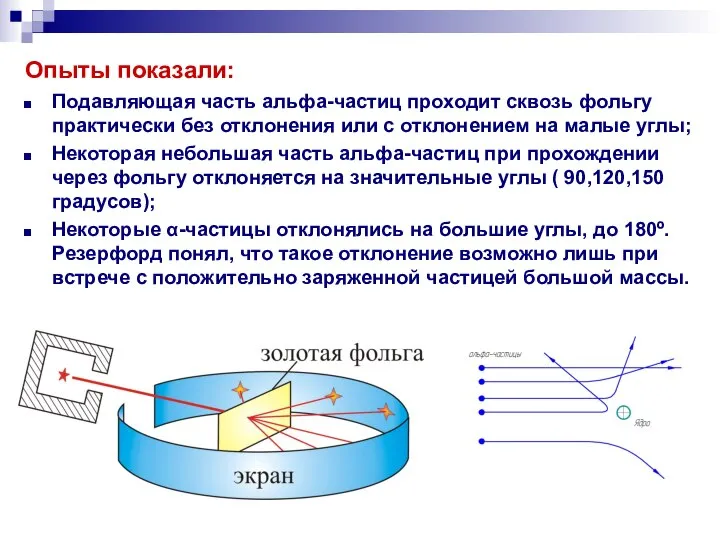
- 11. Опыты показали: Подавляющая часть альфа-частиц проходит сквозь фольгу практически без отклонения или с отклонением на малые
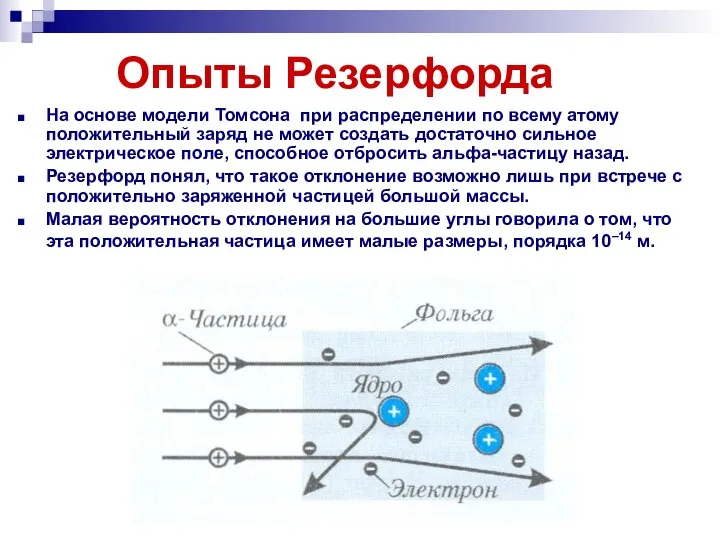
- 12. Опыты Резерфорда На основе модели Томсона при распределении по всему атому положительный заряд не может создать
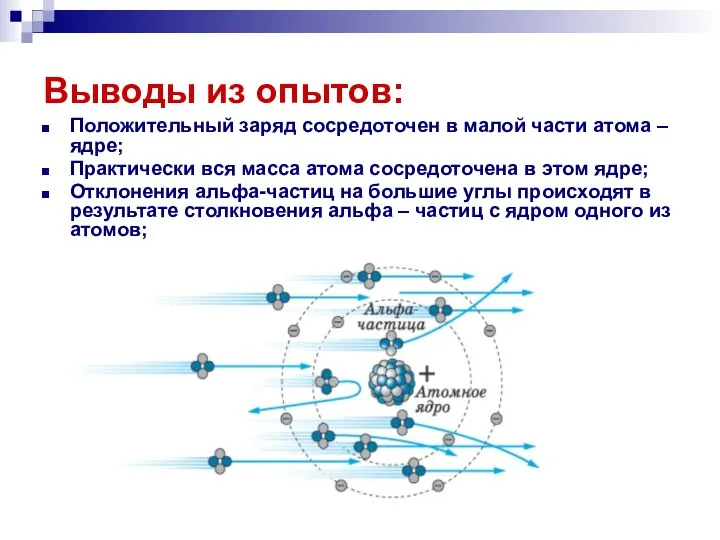
- 13. Выводы из опытов: Положительный заряд сосредоточен в малой части атома – ядре; Практически вся масса атома
- 14. Определение размеров атомного ядра Подсчитывая число альфа-частиц, рассеянных на различные углы, Резерфорд смог оценить размеры ядра.
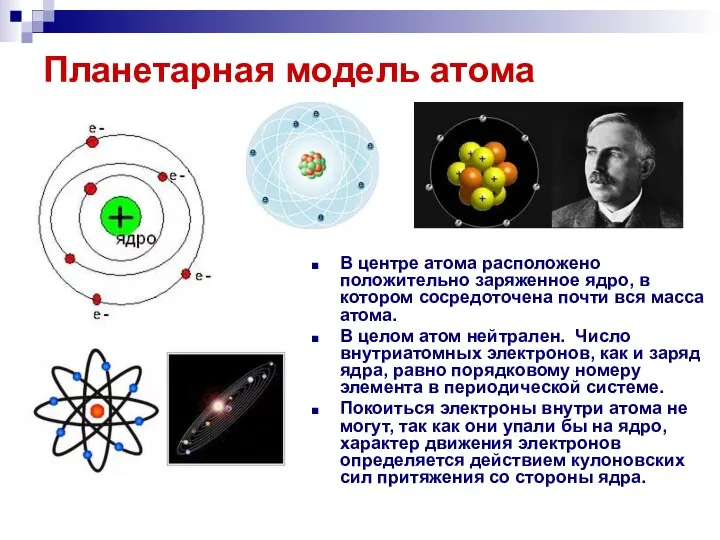
- 15. Планетарная модель атома В центре атома расположено положительно заряженное ядро, в котором сосредоточена почти вся масса
- 17. Недостатки модели атома Резерфорда Эта модель не согласуется с наблюдаемой стабильностью атомов. По законам классической электродинамики
- 18. Попыткой спасения планетарной модели атома стали постулаты Нильса Бора
- 19. Первый постулат Бора (постулат стационарных состояний) В атоме существуют стационарные состояния, в которых он не излучает
- 20. Второй постулат Бора (правило частот) При переходе электрона с одной стационарной орбиты на другую излучается (поглощается)
- 21. Границы применимости модели атома Резерфорда - Бора Следует отметить, что модель атома Резерфорда—Бора достаточно хорошо описывает
- 23. Скачать презентацию














 Взаимосвязь электрического сопротивления графита с его положением в пространстве
Взаимосвязь электрического сопротивления графита с его положением в пространстве Презентация на тему Радиоактивные отходы и методы их захоронения
Презентация на тему Радиоактивные отходы и методы их захоронения  Источники звука. Характеристики звука
Источники звука. Характеристики звука Подход Лагранжа
Подход Лагранжа Prezentatsia_5
Prezentatsia_5 Изменение агрегатного состояния вещества
Изменение агрегатного состояния вещества Воздухоплавание
Воздухоплавание Презентация на тему Сила упругости
Презентация на тему Сила упругости  Связи и реакции связей. Гладкая поверхность
Связи и реакции связей. Гладкая поверхность Управление потоком поверхностных плазмонполяритонов с помощью внешних полей
Управление потоком поверхностных плазмонполяритонов с помощью внешних полей Технология рентгеновских трубок. (Лекция 6)
Технология рентгеновских трубок. (Лекция 6) Радиоактивность в жизни современного человека, значения ядерной энергетики
Радиоактивность в жизни современного человека, значения ядерной энергетики Презентация по физике "Ядерная энергия" -
Презентация по физике "Ядерная энергия" -  Твердофазные реакции
Твердофазные реакции Кинематика. Курс лекций по теоретической механике
Кинематика. Курс лекций по теоретической механике Презентация на тему Молекулы. Диффузия. Взаимодействие молекул
Презентация на тему Молекулы. Диффузия. Взаимодействие молекул  Фотоэффект. (11 класс)
Фотоэффект. (11 класс) Молекулярно-кинетическая теория (МКТ). Масса и размеры молекул
Молекулярно-кинетическая теория (МКТ). Масса и размеры молекул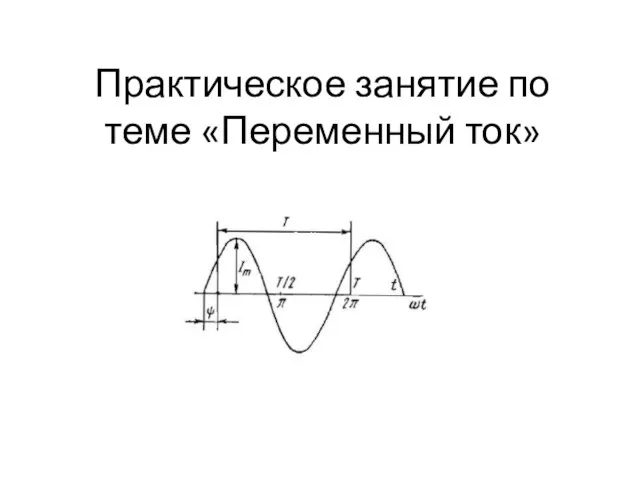 Переменный ток. Практическое занятие
Переменный ток. Практическое занятие Явление механического резонанса
Явление механического резонанса Строение атома
Строение атома Потенциальная энергия
Потенциальная энергия Структурные схемы. Правила преобразования. ТАУ 3-2
Структурные схемы. Правила преобразования. ТАУ 3-2 Формулы по физике
Формулы по физике Термодинамика негіздері
Термодинамика негіздері Морской бой. Игра
Морской бой. Игра График скорости. График координаты. Задачи
График скорости. График координаты. Задачи Эпюры
Эпюры