Содержание
- 2. Лекция 21 μ- пространство. Распределения Максвелла по скоростям и Больцмана по энергиям. Колебательные и вращательные суммы
- 3. Энтропия в каноническом ансамбле. Найдите правильную формулу: 3. 2. 1. 4. 1 балла
- 4. Характеристическая температура, θ. Найдите правильное утверждение. 4. Характеризует расстояние между уровнями энергии, в джоулях ! 3.
- 5. В системе А-В установилось фазовое равновесие жидкий раствор-пар и все химические равновесия. В паре обнаружены молекулы
- 6. Число компонентов системы – это минимальное число независимых химических частиц, которое необходимо для описания состава всех
- 7. Средняя кинетическая энергия и средняя скорость молекул в идеальном газе. Найдите верные утверждения! 4. Средняя энергия
- 8. Для расчета суммы по состояниям Q существуют формулы (1) и (2) которой из них нужно пользоваться?
- 9. Чем мембранное равновесие отличается от фазового? Найдите верные утверждения! 2 балла
- 11. Сумма по состояниям для колебательного движения
- 12. Уровни колебательной энергии
- 13. Колебательная сумма по состояниям 2-х атомной молекулы
- 14. Колебательная сумма Zкол и термодинамические функции
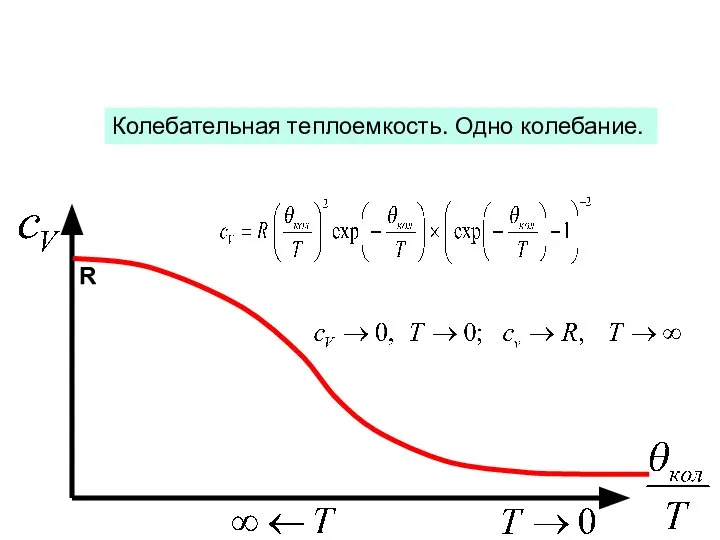
- 15. R Колебательная теплоемкость. Одно колебание.
- 16. Статистический расчет теплоемкости кристаллов (атомных кристаллов).
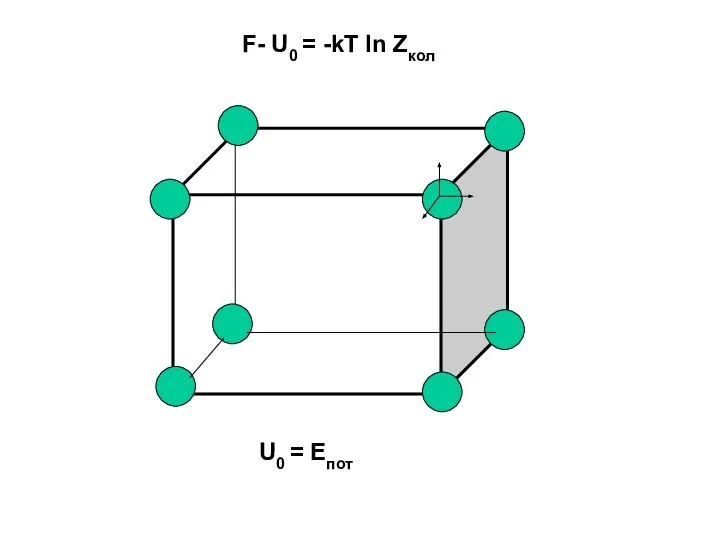
- 18. F- U0 = -kT ln Zкол U0 = Eпот
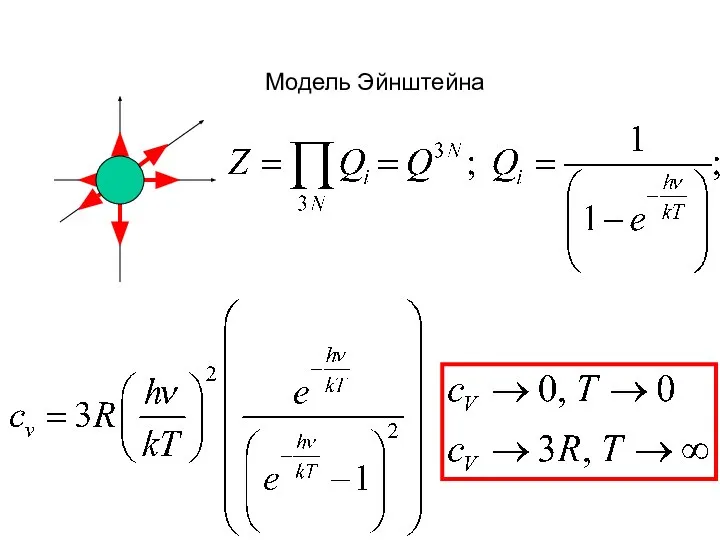
- 19. Модель Эйнштейна
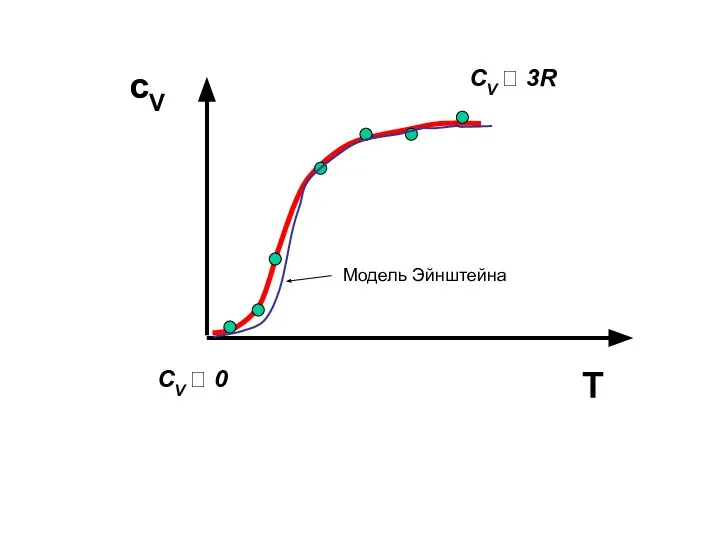
- 20. сV T Модель Эйнштейна СV ? 0 СV ? 3R
- 21. Модель Дебая
- 22. Модели Дебая и Эйнштейна. Обе модели позволяют рассчитать теплоемкость кристаллов Обе модели рассчитывают энергию кристалла E
- 23. Модель Дебая
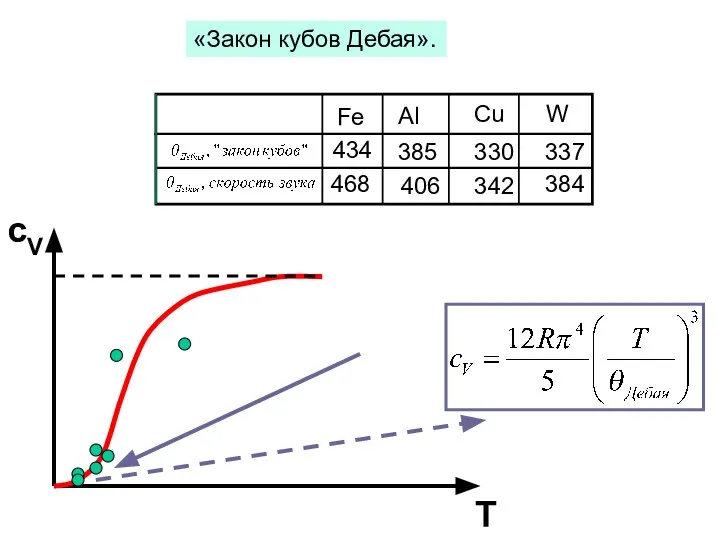
- 24. сV T «Закон кубов Дебая». Fe Al Cu W 434 385 330 337 468 406 342
- 25. Поиски новых способов оценки теплоемкости кристаллов
- 26. Теплоемкость молекулярных кристаллов
- 27. Вращательная и ядерная суммы по состояниям.
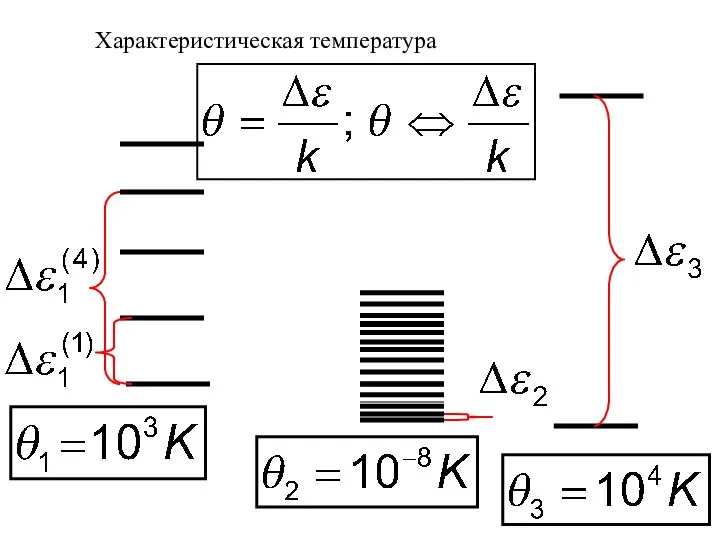
- 28. Характеристическая температура
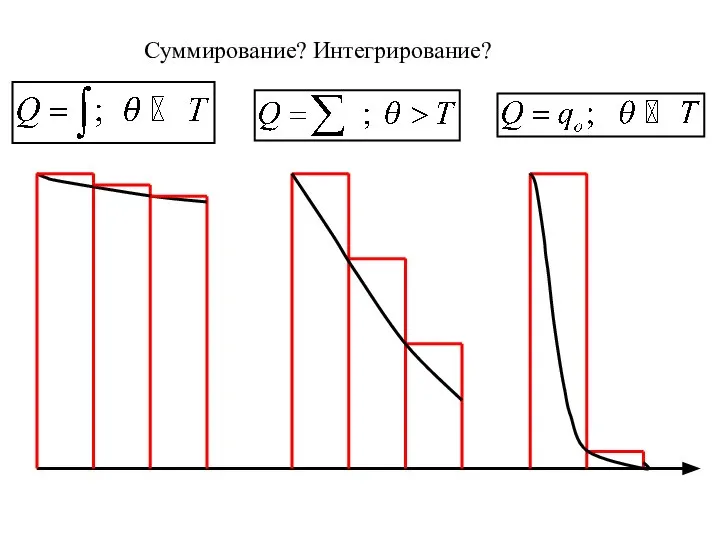
- 29. Суммирование? Интегрирование?
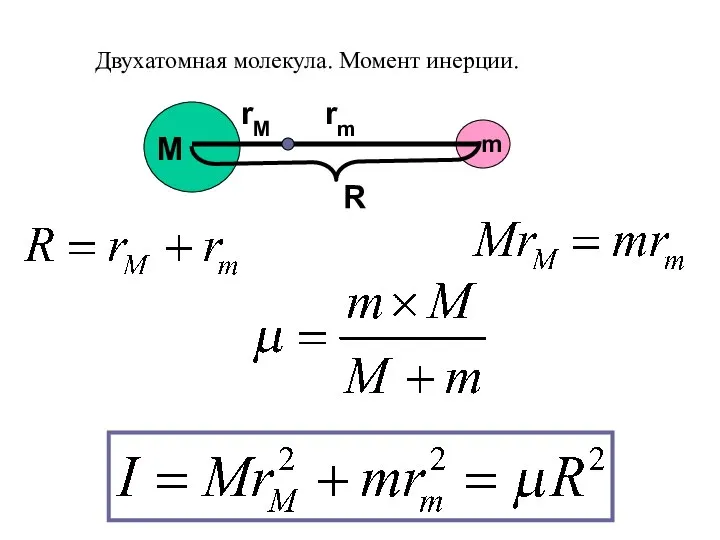
- 30. M m rm rM R Двухатомная молекула. Момент инерции.
- 31. Двухатомная молекула. Вращательное движение
- 32. J=0 J=1 J=2 gвр = 1 gвр= 5 gвр = 3 Уровни вращательной энергии
- 33. Вращательная сумма двухатомной молекулы
- 34. Вращательная сумма двухатомной молекулы
- 35. Вращательная сумма двухатомной молекулы. Вклад в термодинамические функции.
- 36. Вращательная сумма для многоатомной молекулы. Нелинейная молекула: Линейная молекула:
- 37. Вращательная сумма для многоатомной молекулы. Вклад в термодинамические функции Нелинейная молекула: Линейная молекула:
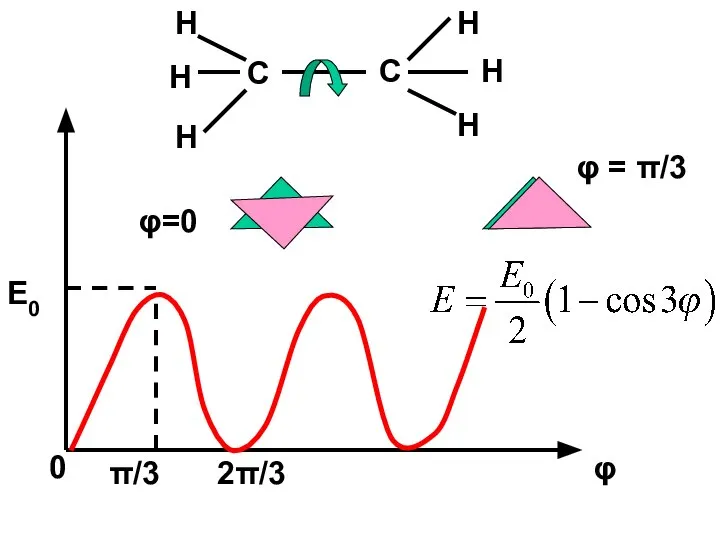
- 38. Внутреннее вращение
- 39. C H H H C H H H φ=0 φ = π/3 2π/3 π/3 φ 0
- 40. Сумма по состоянию для внутреннего вращения Число степеней свободы: 3 пост. +3(2) вр. +вв. +(3N-6(5)-вв.) кол.
- 41. Ядерные и вращательные суммы по состоянию
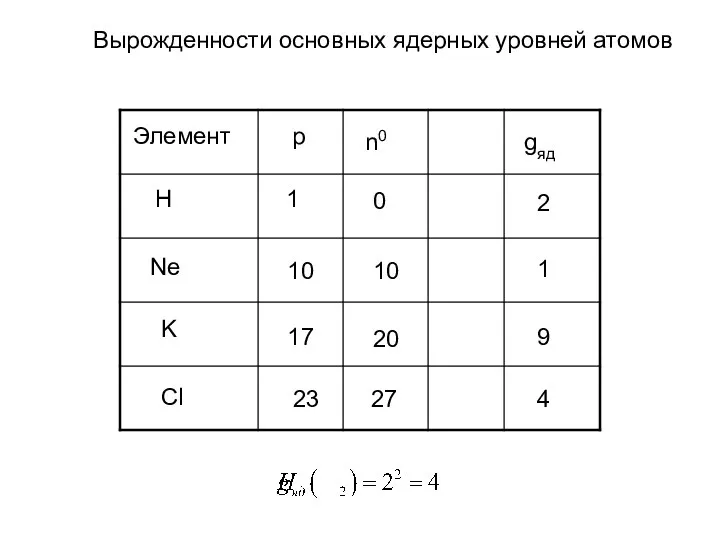
- 42. Ядерные суммы по состояниям Для атома: Для молекулы: Для химической реакции:
- 43. Элемент gяд H Ne K Cl p n0 1 10 17 0 10 20 23 27
- 44. Вращательная и ядерная суммы гомоядерной двухатомной молекулы А2 Для молекулы из ядер с нечетной массой :
- 45. Вращательная и ядерная суммы гомоядерной двухатомной молекулы А2 Для молекулы из ядер с нечетной массой :
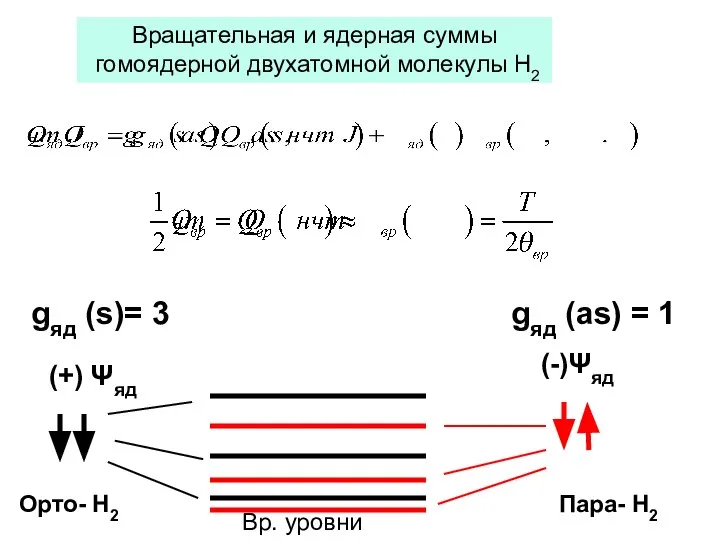
- 46. (-)Ψяд (+) Ψяд gяд (s)= 3 gяд (as) = 1 Пара- Н2 Орто- Н2 Вр. уровни
- 47. Орто- Н2 (Qяд(s), Qвр(as, J=1,3….) Пара- Н2 Qяд( as), Qвр(s, J=0,2….) Пара- и орто-водород при низких
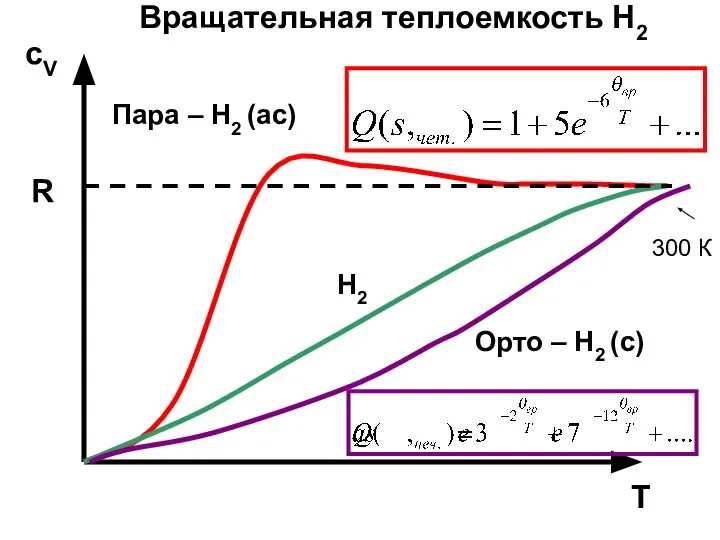
- 48. R cV T H2 Орто – Н2 (с) Пара – Н2 (ас) Вращательная теплоемкость Н2 300
- 49. Расчет термодинамических функций
- 51. Скачать презентацию




































 16M33┐є┐и▓ё╙═╗·┐к╖в┼р╤╡╫╩┴╧пер
16M33┐є┐и▓ё╙═╗·┐к╖в┼р╤╡╫╩┴╧пер Трансорматор и АД
Трансорматор и АД Сложение двух сил, направленных по одной прямой. Равнодействующая сил
Сложение двух сил, направленных по одной прямой. Равнодействующая сил Электромагнитное поле и излучение
Электромагнитное поле и излучение Решение задач динамики машин с учетом сил упругости
Решение задач динамики машин с учетом сил упругости Основное отличие химических явлений от физических?
Основное отличие химических явлений от физических? Явления переноса
Явления переноса Законы Ньютона
Законы Ньютона Виды теплопередачи
Виды теплопередачи Метрология
Метрология Организация технического обслуживания и ремонта системы питания дизельного двигателя Mitsubishi L200
Организация технического обслуживания и ремонта системы питания дизельного двигателя Mitsubishi L200 Машина и механизм
Машина и механизм Классификация механических испытаний
Классификация механических испытаний Уроки физики в 9 , 11 классах
Уроки физики в 9 , 11 классах Откуда берется радуга?
Откуда берется радуга? Весёлые вопросы и задачи по физике. Внеклассное мероприятие для учащихся 10-11 классов
Весёлые вопросы и задачи по физике. Внеклассное мероприятие для учащихся 10-11 классов Преобразование энергии в тепловых процессах
Преобразование энергии в тепловых процессах Молекулярная физика. Введение. Уравнение состояния. (Лекция 1)
Молекулярная физика. Введение. Уравнение состояния. (Лекция 1)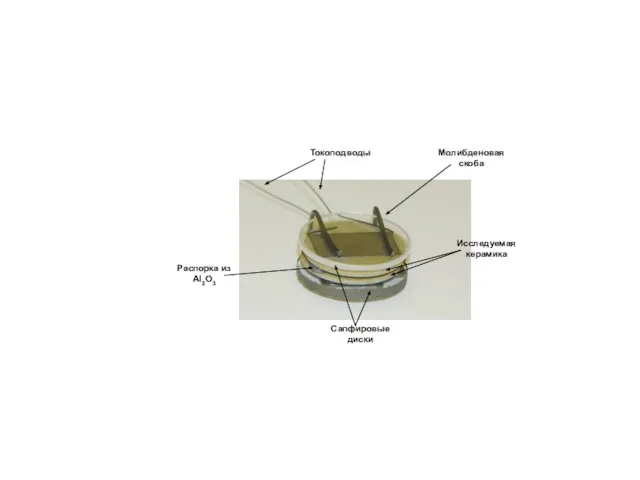 Электросмачивание. Вакуум
Электросмачивание. Вакуум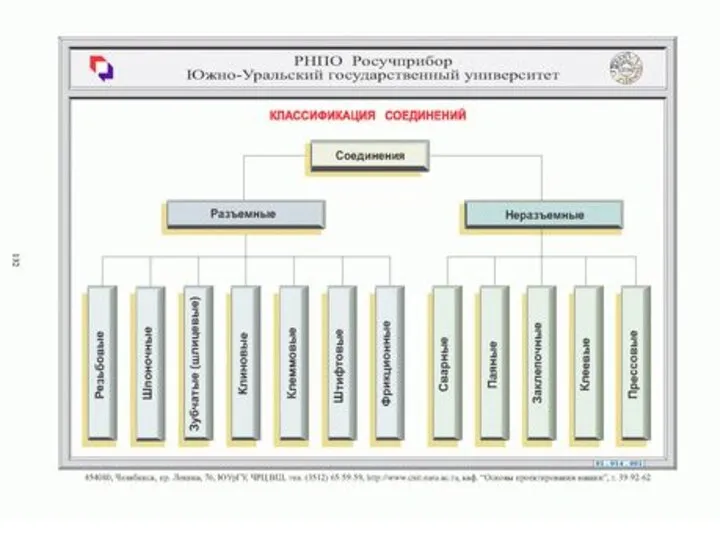 Классаификация соединений
Классаификация соединений Свинцово-кислотные аккумуляторы
Свинцово-кислотные аккумуляторы Разработка проекта устройства снижающего тяжесть последствий при потере устойчивости дорожных катков и компакторов
Разработка проекта устройства снижающего тяжесть последствий при потере устойчивости дорожных катков и компакторов Обзор доказательств ложности утверждений о возможности самосовершенствования
Обзор доказательств ложности утверждений о возможности самосовершенствования Кольца Гельмгольца
Кольца Гельмгольца Механика. Теории механизмов и машин, детали машин и основы конструирования. Курс лекций
Механика. Теории механизмов и машин, детали машин и основы конструирования. Курс лекций Преломление света
Преломление света ЯМР спектроскопия
ЯМР спектроскопия Барометр-анероид
Барометр-анероид