Слайд 22.5. Уравнение адиабатического процесса для идеального газа.

Слайд 4Приведение подобных слагаемых.

Слайд 9Расчёт работы в адиабатическом процессе.

Слайд 102.6. Второе начало термодинамики.
На основе первого начала термодинамики можно решить много термодинамических

задач. Однако, не все явления термодинамики описываются этим законом. Этот закон не устанавливает направленность процессов.
Progr D: Progr E: Progr F: Progr G: Progr H:
Progr D: Progr E: Progr F: Progr G: Progr H:
Слайд 11Необратимость потоков тепла.
Как мы видели выше, тепловые процессы сами по себе протекают

всегда в направлении, когда тепло перетекает от более горячего тела к более холодному. В этом и состоит одна из формулировок второго начала термодинамики. Иначе говоря, не возможны процессы, при которых тепло самопроизвольно перетекало бы от холодного тела к горячему.
Слайд 12Замечание.
В этой формулировке существенным является уточнение «самопроизвольно». Перекачка тепла от холодного тела

к горячему возможна (это подтверждает работа холодильников), но для этого необходимо затратить дополнительную энергию, т.е. произвести работу над системой.
Слайд 14Равновесные и неравновесные процессы.
Определение. Процессы, протекающие при конечных разностях термодинамических параметров, называются

неравновесными.
Это название обусловлено тем, в течение этих процессов система не успевает прийти к равновесию.
Определение. Процессы, протекающие при бесконечно малых разностях термодинамических параметров, называются равновесными.
Слайд 15Характеристика равновесных процессов.
Они характерны тем, что каждое промежуточное состояние системы в этих

процессах можно считать равновесным. Такие процессы, очевидно должны быть достаточно медленными, чтобы успевали пройти тепловые процессы выравнивания термодинамических параметров.
Слайд 18Энтропия при равновесных процессах.

Слайд 19Передача тепла при конечной разности температур.

Слайд 21Вторая формулировка второго начала.
Существует ряд других формулировок второго начала.
Невозможно создать машину, единственным

результатом действия которой было бы отнятие теплоты от некоторого тела и полностью превращение её в работу.
В этом случае коэффициент полезного действия был бы равен 100 %.
Слайд 22Третья формулировка второго начала.
Отсюда вытекает ещё одна формулировка.
Не возможен вечный двигатель второго

рода, т.е. двигатель, кпд которого равен единице.
Можно показать, что все формулировки второго начала термодинамики эквивалентны.
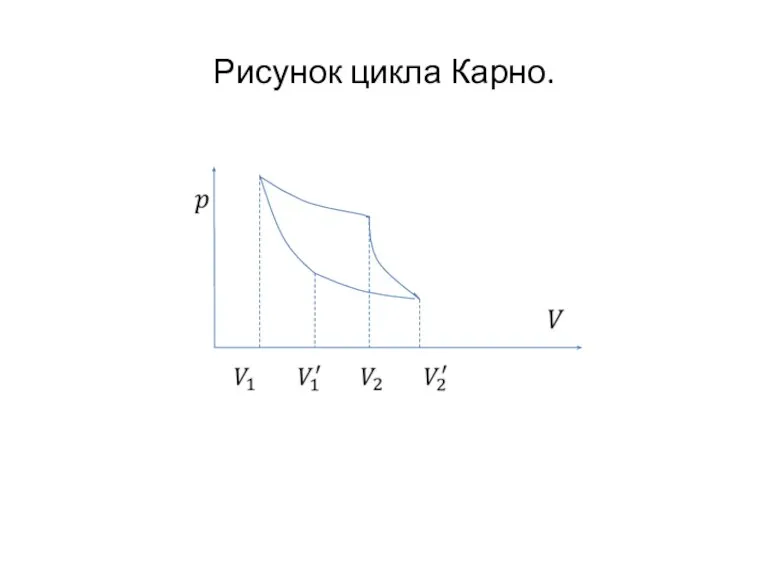
Слайд 232.7. Круговые процессы. Цикл Карно.
Определение. Процессы, при которых термодинамические параметры в начале

и конце процесса совпадают, называются круговыми процессами или термодинамическими циклами.
Одним из самых важных в термодинамике циклов является цикл Карно. Он состоит из двух адиабат и двух изотерм.
Слайд 26Количество теплоты на первой изотерме цикла.

Слайд 27Теплота на втором изотермическом участке цикла.

Слайд 33Функции состояния.
Определение. Параметры термодинамической системы, изменение которых за полный цикл равно нулю,

называются функциями состояния системы.
С математической точки зрения это означает, что их элементарное изменение представляет собой полный дифференциал.
Согласно определению и последнему равенству энтропия есть функция состояния системы.
Слайд 34Первое начало с использованием энтропии.

Слайд 37Связь энтропии с давлением и теплоёмкостью.

Слайд 38Соотношения между термодинамическими параметрами.
Таким образом, только из того факта, что некоторая величина

есть функция состояния, можно находить соотношения между термодинамическими параметрами.




































 Вода
Вода Логарифмическая шкала децибелов
Логарифмическая шкала децибелов Механическая работа
Механическая работа Георг Ом (1787-1854) немецкий физик
Георг Ом (1787-1854) немецкий физик Применение ядерной энергии в различных отраслях. Доза радиоактивного излучения. Ядерная реакция
Применение ядерной энергии в различных отраслях. Доза радиоактивного излучения. Ядерная реакция Презентация на тему Солнце и другие звезды
Презентация на тему Солнце и другие звезды  Конвекция. Примеры конвекции
Конвекция. Примеры конвекции Ф. Савар, его вклад в развитие физики
Ф. Савар, его вклад в развитие физики Общие сведения о системе пуска
Общие сведения о системе пуска Физика для химиков день третий. МКТ и электричество
Физика для химиков день третий. МКТ и электричество Работа газа и пара при расширении. Двигатель внутреннего сгорания
Работа газа и пара при расширении. Двигатель внутреннего сгорания Уравнение состояния идеального газа
Уравнение состояния идеального газа Сопротивление материалов. Металлический тип химической связи и основные свойства металлов
Сопротивление материалов. Металлический тип химической связи и основные свойства металлов Некогерентность рассеяния. (Тема 15)
Некогерентность рассеяния. (Тема 15) Физика. Границы применимости
Физика. Границы применимости Последовательное соединение проводников
Последовательное соединение проводников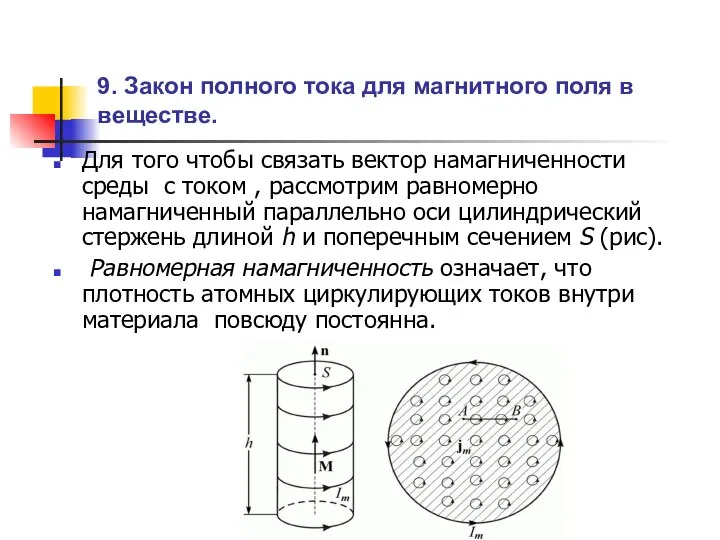 Закон полного тока для магнитного поля в веществе
Закон полного тока для магнитного поля в веществе Закон сохранения импульса
Закон сохранения импульса Газовые законы
Газовые законы Оптические иллюзии
Оптические иллюзии Классификация томографов и магнитов
Классификация томографов и магнитов Механические передачи. Цепные передачи. (Лекция 3)
Механические передачи. Цепные передачи. (Лекция 3) ВСР №15. Голография и ее применение
ВСР №15. Голография и ее применение Параметры сопряжения деталей
Параметры сопряжения деталей Викторина по физике
Викторина по физике Понятие смены скорости - ось. Модели расширения и сужения
Понятие смены скорости - ось. Модели расширения и сужения Рационализация организации движения автобусов на маршруте Ул. Украинская - МКР. Соцгород
Рационализация организации движения автобусов на маршруте Ул. Украинская - МКР. Соцгород Реактивное движение. Ракеты
Реактивное движение. Ракеты