Слайд 2Столкновения молекул
В газовой среде могут иметь место неоднородности концентрации компонентов газовой смеси,

скорости перемещения макроскопических масс вещества, температуры.
Равновесие в газе устанавливается в результате столкновений между молекулами.
Для этого достаточно, чтобы каждая молекула испытала одно-два столкновения.
Слайд 3Столкновения молекул
Для упрощения расчета предположим, что движется только одна молекула с постоянной

скоростью v, а все остальные молекулы неподвижны.
Будем называть движущуюся молекулу молекулой А. Вообразим, что с молекулой А жестко связана концентрическая с ней твердая сфера S вдвое большего диаметра.
Назовем эту сферу сферой ограждения молекулы А. В момент столкновения расстояние между центрами сталкивающихся молекул равно диаметру молекулы d.
Слайд 4Столкновения молекул
Между двумя последовательными столкновениями молекулы А ее сфера ограждения описывает цилиндр,

длина которого и есть свободный пробег молекулы А. Из таких цилиндров складывается поверхность, описываемая с течением времени сферой ограждения
Если центр другой молекулы лежит внутри или на боковой поверхности этого цилиндра, то она столкнется с молекулой А. В противном случае столкновения не произойдет.
Слайд 5Столкновения молекул
Пусть V – объем ломаного цилиндра, описываемого сферой S в единицу

времени. Среднее число z столкновений движущейся молекулы с остальными молекулами в единицу времени равно среднему числу последних в объеме V,
z = Vn,
где n – число молекул в единице объема.
Слайд 12Длина свободного пробега
Длина свободного пробега не зависит от температуры.
Физический смысл этого

явления можно понять, если вспомнить, что с повышением температуры увеличивается средняя скорость молекул.
Они при этом быстрее двигаются, но и чаще сталкиваются, в итоге ничего не выигрывая в свободном пробеге.
Слайд 14Рассеяние молекулярного пучка в газе
Допустим, что в газе распространяется параллельный пучок молекул.

Пусть Jo — интенсивность пучка, когда он пересекает плоскость АВ, перпендикулярную к нему.
Найдем интенсивность J того же пучка на расстоянии х от плоскости АВ.
Слайд 15Рассеяние молекулярного пучка в газе
Возьмем бесконечно тонкий слой газа с толщиной dx

и площадью поперечного сечения S = 1.
Число молекул газа в нем равно nSdx = ndx.
Среднее число частиц, выбывающих из пучка из-за столкновений с одной молекулой газа, равно Jσ,
из-за столкновений с ndx молекулами
dN = Jσndx = (J/λ)dx. На такую величину уменьшится интенсивность пучка после прохождения слоя dx
Слайд 16Рассеяние молекулярного пучка в газе

Слайд 17Рассеяние молекулярного пучка в газе

Слайд 18Рассеяние молекулярного пучка в газе

Слайд 19Принцип локального равновесия
Принцип (или гипотезы) локального равновесия, который состоит в следующем. Как

уже говорилось, в результате столкновений молекул друг с другом устанавливается равновесное распределение их по скоростям поступательного движения. Причем достаточно, чтобы каждая из молекул испытала одно-два соударения. В принципе локального равновесия предполагается, что все молекулы, попавшие в объем, размеры которого порядка <λ>, испытают в нем соударения и что в этом малом объеме устанавливается локальное равновесие с некоторой температурой, плотностью и т. д. В другом подобном объеме также устанавливается равновесное состояние, но по другим по величине параметрами. Таким образом, каждой точке пространства можно приписать свои локальные параметры.
Слайд 20Диффузия
Допустим, что закрытая горизонтальная труба разделена на две части перегородкой. По одну

сторону перегородки находится какой-то газ 1, а по другую – газ 2.
Пусть давления и температуры обоих газов одинаковы. Если удалить перегородку, то газы начнут перемешиваться. Причиной этого является хаотическое тепловое движение молекул. Спустя некоторое время концентрации компонентов смеси станут одинаковыми по обе стороны перегородки.
Такое проникновение молекул одного газа в среду молекул другого газа называется взаимной, или концентрационной диффузией газов.
Если газы по обе стороны перегородки тождественны, то диффузия также будет происходить. В этом случае она называется самодиффузией.
Слайд 21Диффузия
Рассмотрим случай, когда в газе есть примесь другого газа. Общее давление везде

одинаково, а концентрация примеси n(х) меняется вдоль оси х .
Выделим перпендикулярную этой оси единичную площадку. Потоки молекул в единицу времени с одной и другой стороны пропорциональны концентрациям в элементах объема, находящихся на расстояниях, отстоящих примерно на величину свободного пробега слева и справа от площадки.
Будем приближенно считать, что по направлению к площадке двигаются 1/6 часть молекул с одинаковой скоростью равной средней скорости молекул примеси.
Слайд 24Связь между коэффициентами подвижности и диффузии

Слайд 25Связь между коэффициентами подвижности и диффузии

Слайд 26Связь между коэффициентами подвижности и диффузии

Слайд 27Связь между коэффициентами подвижности и диффузии

Слайд 32 Теплопроводность
Поток тепла пропорционален градиенту температуры и направлен против него.
Этот факт

был установлен экспериментально и назван законом Фурье.
Слайд 33Вязкость газа
Между двумя параллельными пластинками АВ и СD) находится воздух или другой

газ. При движении пластинки CD появляется сила, действующая на пластинку АВ и направленная в сторону движения. Эта сила и есть сила вязкости.
Слайд 34Вязкость газа
Будем представлять себе газ неограниченным и движущимся стационарно плоскопараллельными слоями в

горизонтальном направлении. Скорость этого макроскопического движения u меняется в направлении, перпендикулярном к слоям. Это направление мы примем за ось X Таким образом, мы предполагаем, что u = u(х).
Слайд 35Вязкость газа
При наличии упорядоченного движения газа средняя скорость молекулы не нуль, а

равна u = u(х). С этой скоростью связано количество движения mu, которым обладает рассматриваемая молекула. Такое количество движения условимся называть упорядоченным.
Молекулы, лежащие над плоскостью А В, обладают большим упорядоченным количеством движения, чем молекулы, расположенные под ней.
Переходя из пространства над плоскостью MN в пространство под ней, молекулы передают часть своего упорядоченного количества движения молекулам, с которыми они сталкиваются в пространстве ниже плоскости МN.
Слайд 37Вязкость газа
Так как λ обратно пропорциональна n, то отсюда следует, что вязкость

и теплопроводность не зависят от плотности газа. К такому выводу впервые пришел Максвелл, и этот вывод показался ему парадоксальным. Однако опыты, поставленные самим Максвеллом и другими физиками, подтвердили указанный вывод.
Слайд 38Вязкость газа
Независимость вязкости и теплопроводности от плотности газа имеет простое объяснение. Если

плотность газа велика, то в переносе импульса и энергии участвует много молекул. Однако передача импульса и энергии за время между двумя последовательными столкновениями производится малыми порциями и на малые расстояния. Если же плотность мала, то уменьшается и число молекул, участвующих в переносе. Но это уменьшение полностью компенсируется тем, что теперь молекулы переносят импульс и энергию более крупными порциями и на большие расстояния.
Слайд 39Явления в разреженных газах
Если средняя длина свободного пробега λ того же порядка,

что и характерный линейный размер сосуда d, в котором заключен газ, или больше, то состояние газа называют вакуумом. Воздух в комнате, например, при атмосферном давлении в состоянии вакуума не находится, так как в этом случае λ ~ 10-5 см. Однако в сосуде, линейные размеры которого меньше 10-5 см (поры дерева и многих других пористых тел), тот же воздух уже находится в условиях вакуума.
Слайд 40Явления в разреженных газах
Различают три вида вакуума:
1) низкий, когда λ меньше

характерного размера сосуда d, но приближается к нему;
2) средний, когда λ сравнима с d,
3) высокий (или глубокий), когда λ значительно больше d.
Газ в состоянии высокого вакуума называется ультраразреженным.
Слайд 43Явления в разреженных газах
Поток молекул газа через отверстие в стенке называется эффузионным

потоком, если размеры отверстия и толщина стенки малы по сравнению с длиной свободного пробега λ.
Допустим теперь, что по разные стороны перегородки находится один и тот же газ, но при разных давлениях и температурах. Если газ находится в состоянии высокого вакуума, то возникнут два эффузионных потока: из А в В и из В в А
Слайд 45Явления в разреженных газах
Пусть два сосуда 1 и 2 соединены между собой

трубкой и поддерживаются при разных температурах Т1 и Т2.
Когда поперечное сечение трубки очень велико по сравнению с длиной свободного пробега,
Условие равновесия носит гидродинамический характер: должны быть равны давления Р1 и P2 в обоих сосудах. В противоположном случае, когда длина свободного пробега очень велика по сравнению с поперечными размерами трубки, гидродинамический подход неприменим.
Слайд 47Явления в разреженных газах
Допустим теперь, что сосуд разделен пористой перегородкой на две

части, поддерживаемые при разных температурах Т1 и Т2. Пусть размеры пор малы по сравнению с длиной свободного пробега.
Тогда, если первоначальные давления Р1 и Р2 были равны, то газ начнет перетекать в направлении от более низкой к более высокой температуре. Это явление называется тепловой диффузией или эффектом Кнудсена.














































 Графический материал к выпускной квалификационной (бакалаврской) работе на тему: Электроснабжение части села кучугуры
Графический материал к выпускной квалификационной (бакалаврской) работе на тему: Электроснабжение части села кучугуры Werkstoffkunde 2020-2021
Werkstoffkunde 2020-2021 Химические источники тока. Хит в будущем
Химические источники тока. Хит в будущем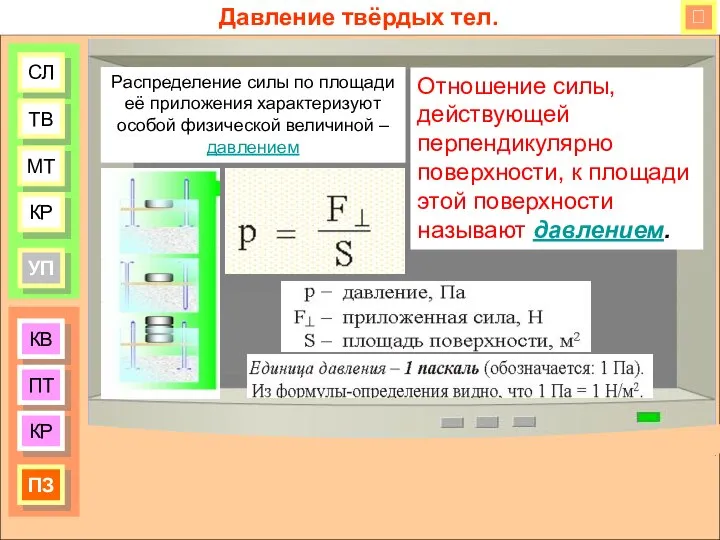 Давление твёрдых тел
Давление твёрдых тел Параметры потребителей и источника электроэнергии
Параметры потребителей и источника электроэнергии Шкала, первый импульс и N-формация
Шкала, первый импульс и N-формация Оптическая сила линзы
Оптическая сила линзы Подвеска
Подвеска Устройство ведущего моста трактора ДТ-75
Устройство ведущего моста трактора ДТ-75 Сила Архимеда – выталкивающая сила
Сила Архимеда – выталкивающая сила Коллективные спасательные средства. Тема 2.3
Коллективные спасательные средства. Тема 2.3 Расчет бункеров
Расчет бункеров Закон Ома. Сопротивление цепи
Закон Ома. Сопротивление цепи Презентация на тему Модели атомов. Опыт Резерфорда
Презентация на тему Модели атомов. Опыт Резерфорда  Магнитное поле
Магнитное поле Кинематика
Кинематика Колесно-моторный блок с МОП качения и ТЭД НБ-514Е
Колесно-моторный блок с МОП качения и ТЭД НБ-514Е Основы энергетики. Строение материи
Основы энергетики. Строение материи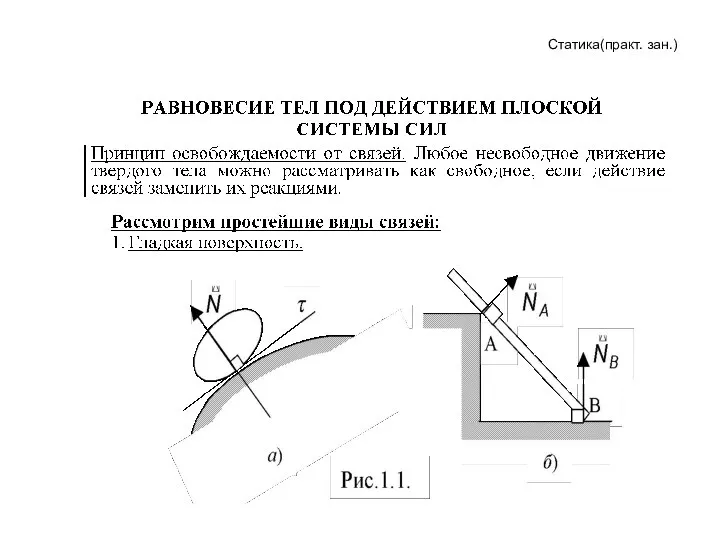 Равновесие тел под действием плоской системы сил
Равновесие тел под действием плоской системы сил Движение искусственных спутников
Движение искусственных спутников Тайны и чудеса зимушки-зимы
Тайны и чудеса зимушки-зимы Теория автоматического управления. Интегрирующие звенья
Теория автоматического управления. Интегрирующие звенья лекция 4_дифр Фраунгофера на ДР
лекция 4_дифр Фраунгофера на ДР Вес воздуха. Атмосферное давление
Вес воздуха. Атмосферное давление Презентация на тему Силы в природе (7 класс)
Презентация на тему Силы в природе (7 класс)  Аккумуляторная батарея
Аккумуляторная батарея Основные и дополнительные средства защиты в сетях напряжением выше 1000 в
Основные и дополнительные средства защиты в сетях напряжением выше 1000 в Применение электромагнитной индукции
Применение электромагнитной индукции