Содержание
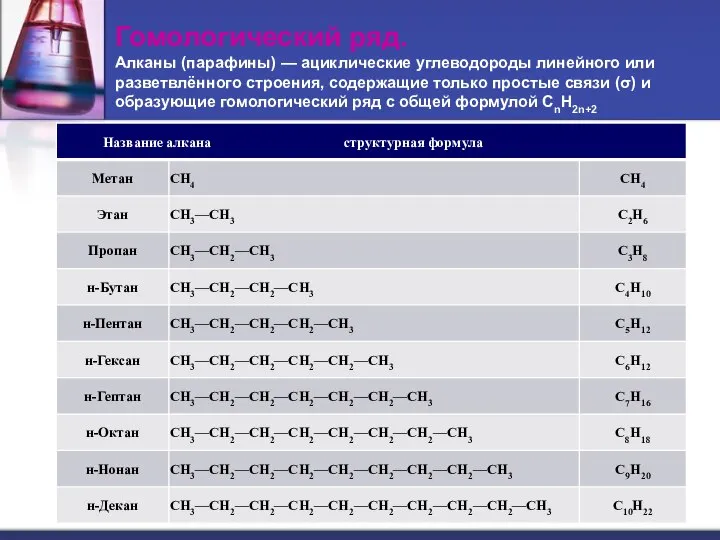
- 2. Гомологический ряд. Алканы (парафины) — ациклические углеводороды линейного или разветвлённого строения, содержащие только простые связи (σ)
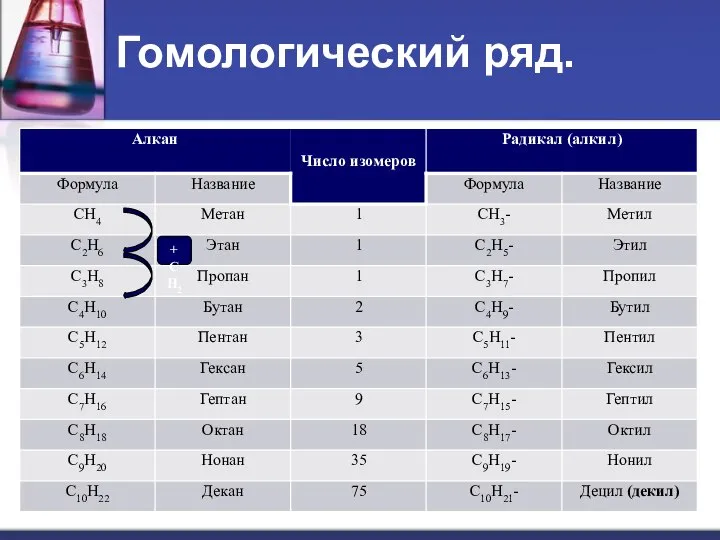
- 3. Гомологический ряд.
- 4. Наиболее часто встречающиеся углеводородные радикалы:
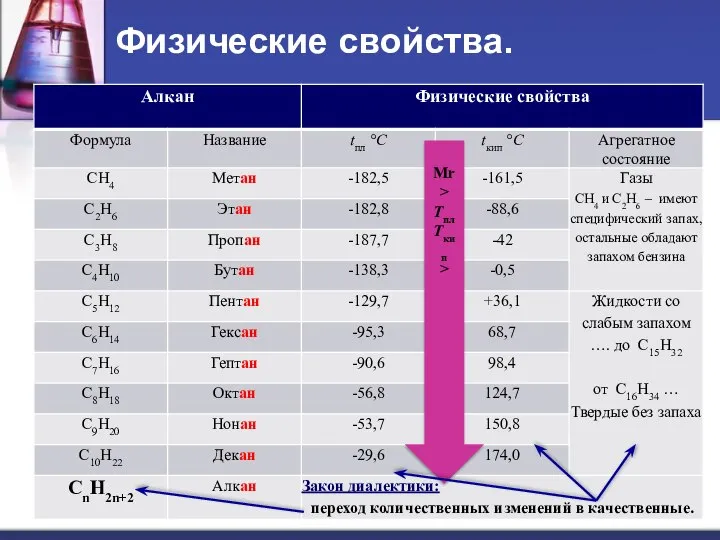
- 5. Мr > Tпл Tкип > Физические свойства.
- 6. Строение. В алканах имеются два типа химических связей: С–С и С–Н. Связь С–С является ковалентной неполярной.
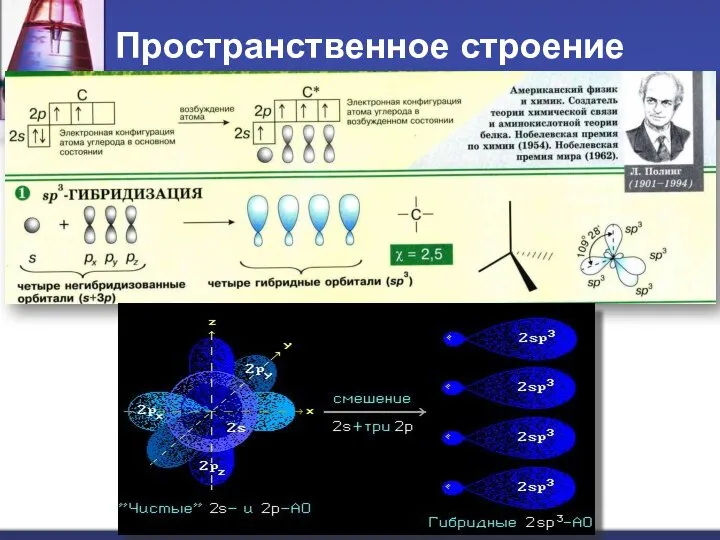
- 7. Пространственное строение
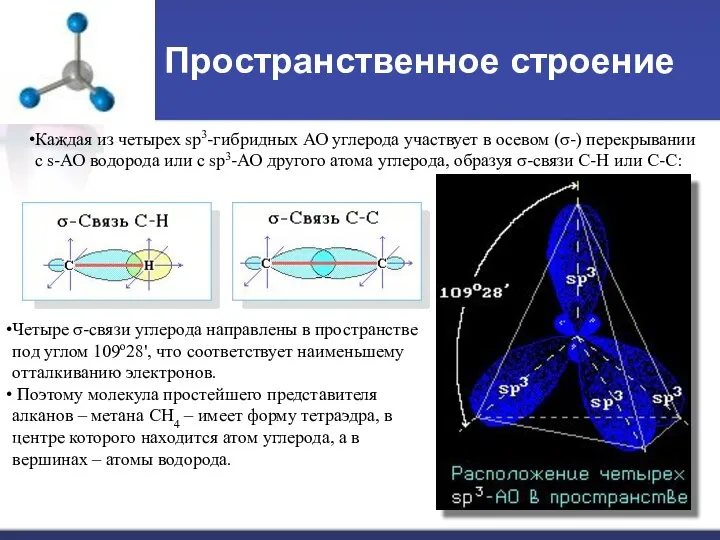
- 8. Пространственное строение Каждая из четырех sp3-гибридных АО углерода участвует в осевом (σ-) перекрывании с s-АО водорода
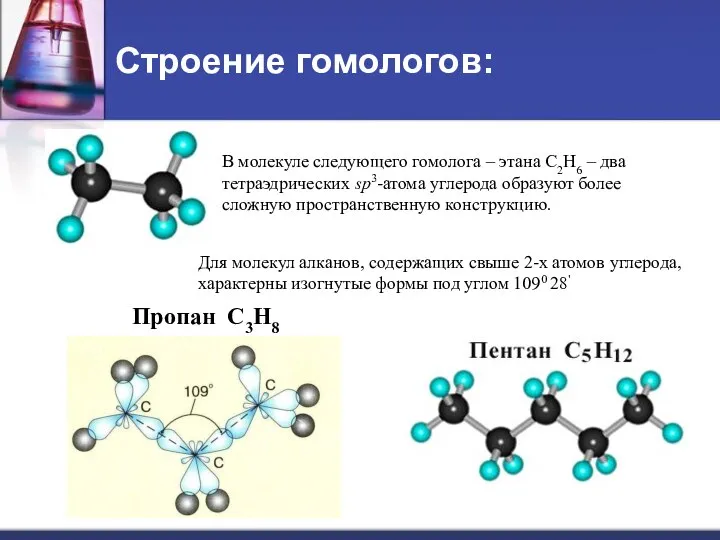
- 9. Строение гомологов: В молекуле следующего гомолога – этана С2Н6 – два тетраэдрических sp3-атома углерода образуют более
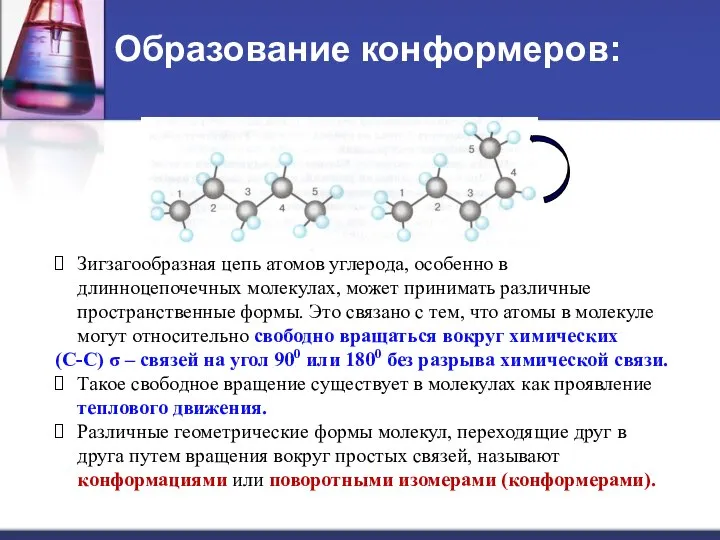
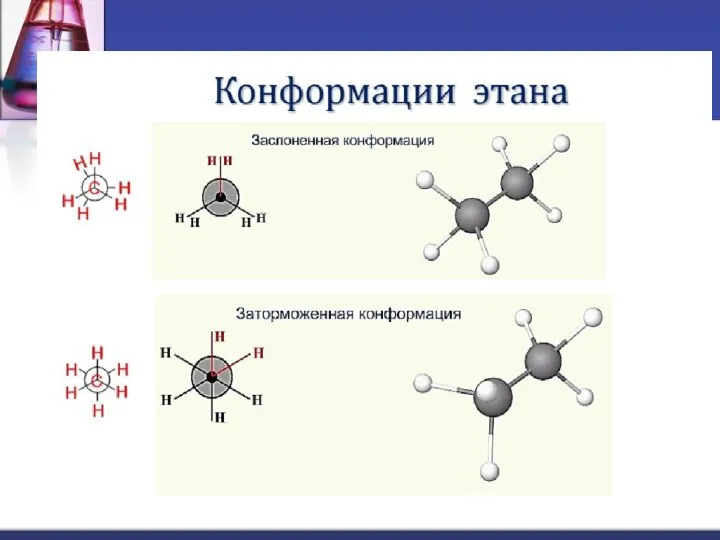
- 10. Образование конформеров: Зигзагообразная цепь атомов углерода, особенно в длинноцепочечных молекулах, может принимать различные пространственные формы. Это
- 12. Пространственное строение – самое главное !
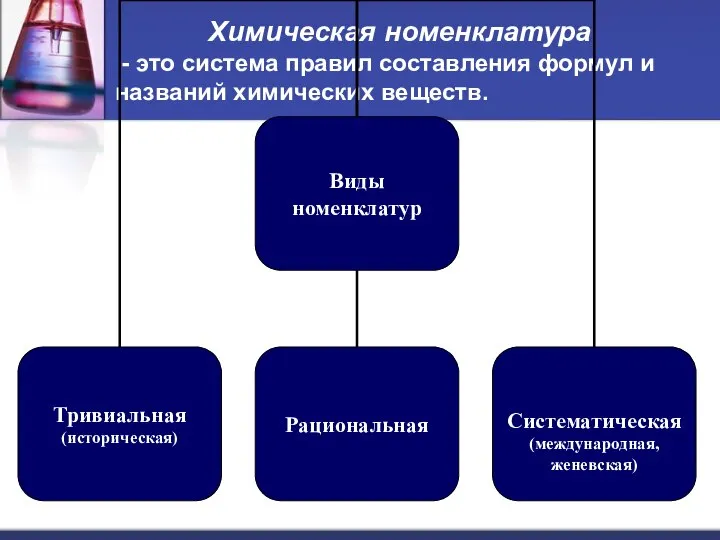
- 13. Химическая номенклатура - это система правил составления формул и названий химических веществ.
- 14. Тривиальная номенклатура Включает случайные названия и названия от греческих числительных (по количеству атомов углерода): С4Н10 –
- 15. Рациональная номенклатура Углеводороды рассматриваются как производные метана, у которого один или несколько атомов водорода замещены на
- 16. Правила систематической номенклатуры ЮПАК (IUPAC). Правило главной цепи: главную цепь выбирают, руководствуясь последовательно следующими критериями: Максимальное
- 17. Правила систематической номенклатуры ЮПАК (IUPAC). Правило радикалов: Все углеводородные боковые группы рассматривают как одновалентные (односвязные) радикалы.
- 18. Систематическая номенклатура Любая разветвленная цепь рассматривается как длинная (главная), в которой атомы водорода замещены на радикалы
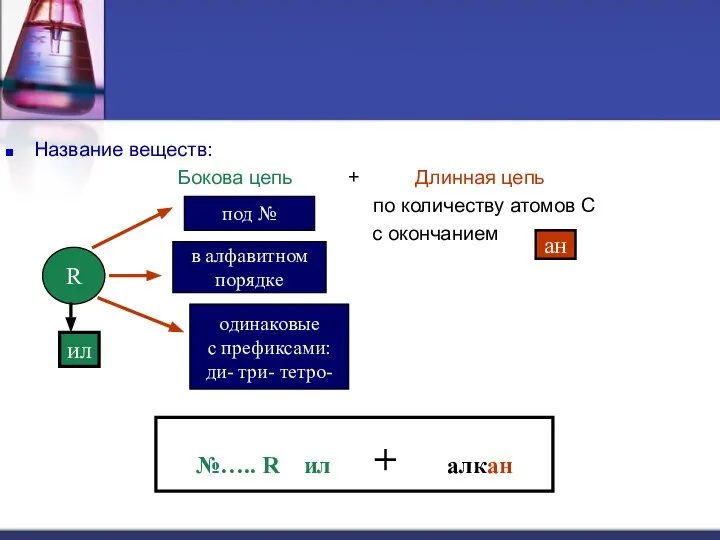
- 19. Название веществ: Бокова цепь + Длинная цепь по количеству атомов С с окончанием ан №….. R
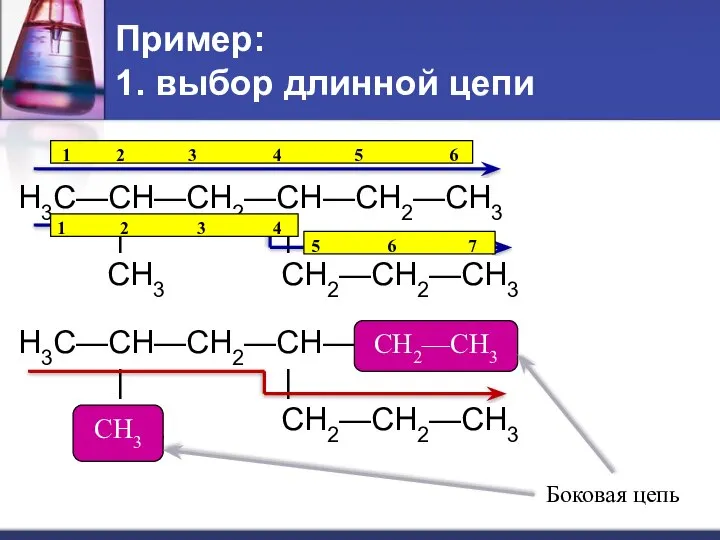
- 20. Пример: 1. выбор длинной цепи H3C—CH—CH2—CH—CH2—CH3 | | CH3 CH2—CH2—CH3 H3C—CH—CH2—CH—CH2—CH3 | | CH3 CH2—CH2—CH3 1
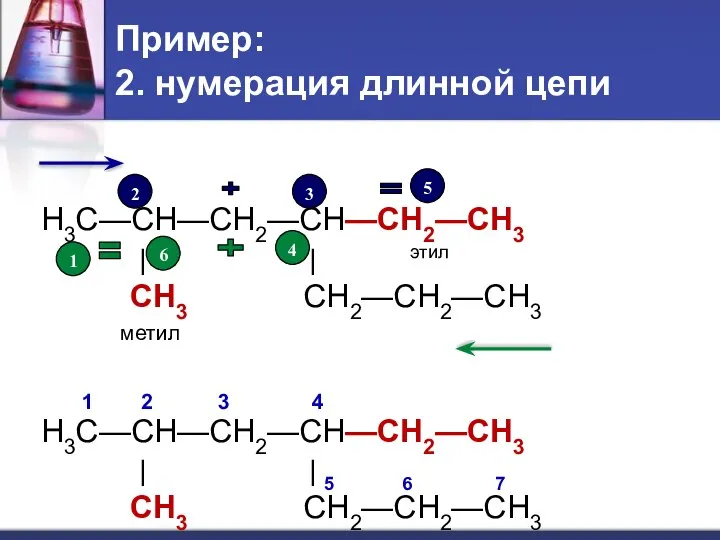
- 21. Пример: 2. нумерация длинной цепи H3C—CH—CH2—CH—CH2—CH3 | | этил CH3 CH2—CH2—CH3 метил 1 2 3 4
- 22. Систематическая номенклатура Любая разветвленная цепь рассматривается как длинная (главная), в которой атомы водорода замещены на радикалы
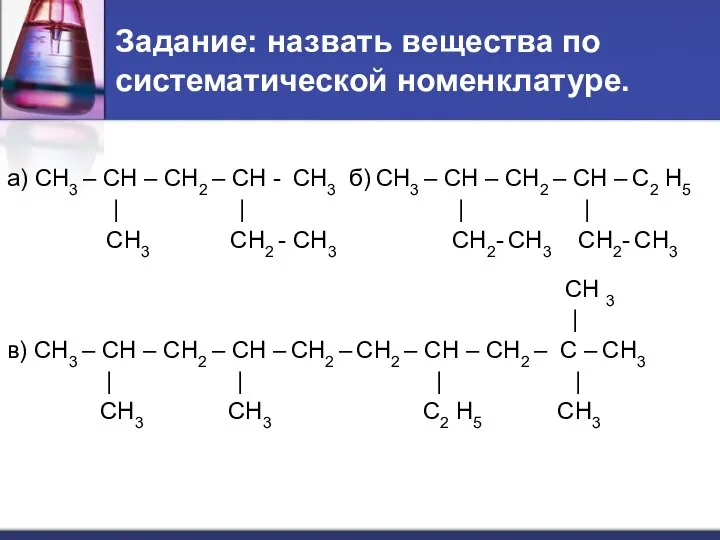
- 23. Задание: назвать вещества по систематической номенклатуре. а) СН3 – СН – СН2 – СН - СН3
- 24. Проверка: Примеры: 1 2 3 4 3 4 5 6,7 а) СН3 – СН – СН2
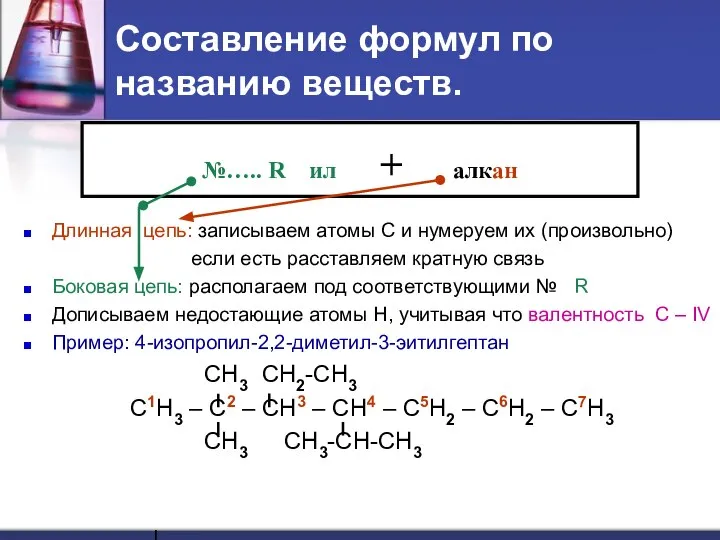
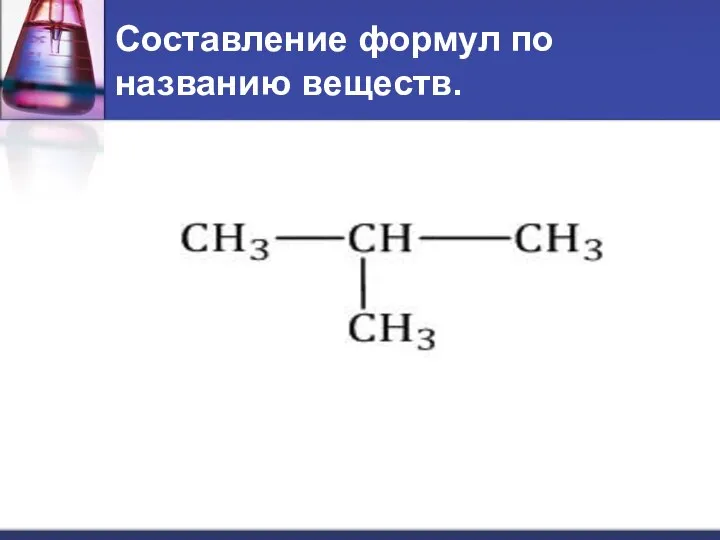
- 25. Составление формул по названию веществ. Длинная цепь: записываем атомы С и нумеруем их (произвольно) если есть
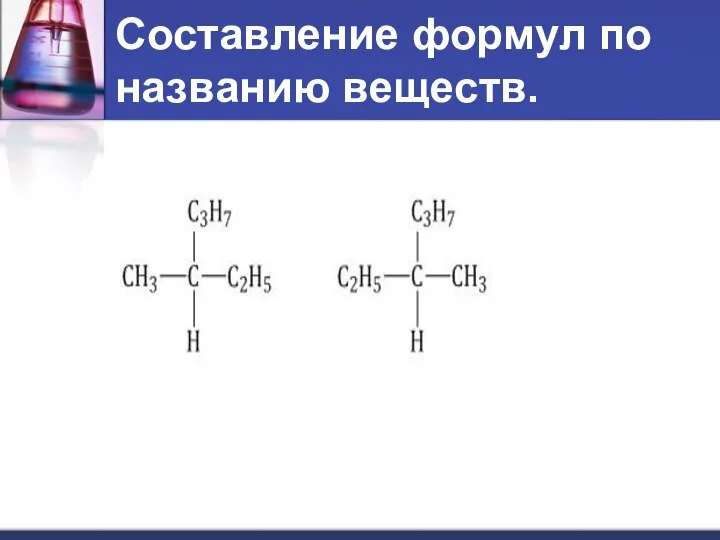
- 26. Составление формул по названию веществ.
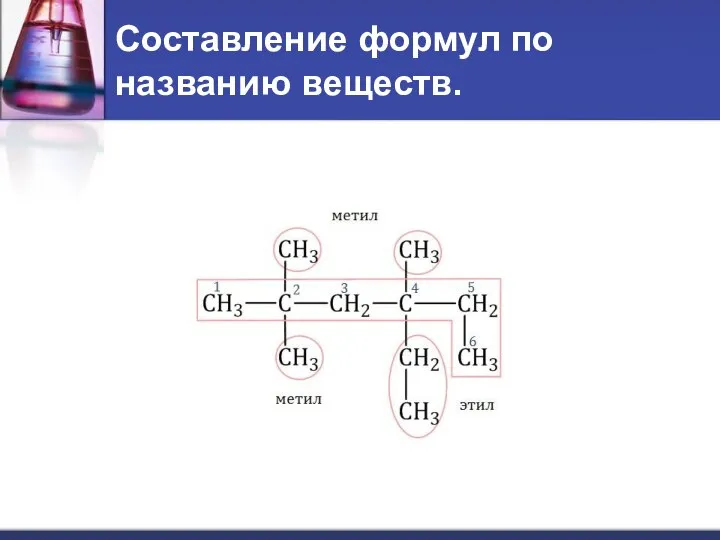
- 27. Составление формул по названию веществ.
- 28. Составление формул по названию веществ.
- 29. Составление формул по названию веществ.
- 31. Скачать презентацию











 Алкины
Алкины Презентация на тему Спирты (10 класс)
Презентация на тему Спирты (10 класс)  Получение и примененипе радиоактивные изотопы
Получение и примененипе радиоактивные изотопы Какой химический элемент алхимики обозначали таким символом? Интеллектуальная игра
Какой химический элемент алхимики обозначали таким символом? Интеллектуальная игра Свойства нефти
Свойства нефти Основные химические законы
Основные химические законы Электролиз растворов и расплавов
Электролиз растворов и расплавов Коррозия металлов
Коррозия металлов Основы химической термодинамики и термохимии. Лекция 3
Основы химической термодинамики и термохимии. Лекция 3 Pomalé a rýchle reakcie v bežnom živote
Pomalé a rýchle reakcie v bežnom živote Вывод формул химических веществ
Вывод формул химических веществ Общая характеристика элементов главной подгруппы II группы
Общая характеристика элементов главной подгруппы II группы Степени окисления и формулы веществ
Степени окисления и формулы веществ Ministry of Education and Science of the Russian Federation
Ministry of Education and Science of the Russian Federation Кислородсодержащие органические вещества
Кислородсодержащие органические вещества Ключевые реакции и регуляторные ферменты начальных этапов углеводного обмена
Ключевые реакции и регуляторные ферменты начальных этапов углеводного обмена Фосфориты. Добыча фосфоритов
Фосфориты. Добыча фосфоритов Алканы. Строение
Алканы. Строение Способы выражения концентраций растворов
Способы выражения концентраций растворов Свойства солёной воды. Море у меня в стакане
Свойства солёной воды. Море у меня в стакане Сплавы со специальными свойствами
Сплавы со специальными свойствами Инновационное производство синтетических мелкокодисперсных оксидов и оборудования для их изготовления
Инновационное производство синтетических мелкокодисперсных оксидов и оборудования для их изготовления Электролиз
Электролиз Электролитическая диссоциация
Электролитическая диссоциация Презентация на тему Химия в промышленности
Презентация на тему Химия в промышленности  Fyzikálne a chemické deje
Fyzikálne a chemické deje Микроэмульсия. Микроэмульсияның макроэмулсиядан айырмашылығы
Микроэмульсия. Микроэмульсияның макроэмулсиядан айырмашылығы Натуральные и синтетические каучуки
Натуральные и синтетические каучуки