Содержание
- 2. Содержание Давыдова Н.Б., учитель химии МБОУ "Вадская СОШ", Вад Подготовка к усвоению нового материала. Изучение нового
- 3. Подготовка к усвоению нового материала 1807 г. английский физик и химик Гемфри Дэви с помощью электричества
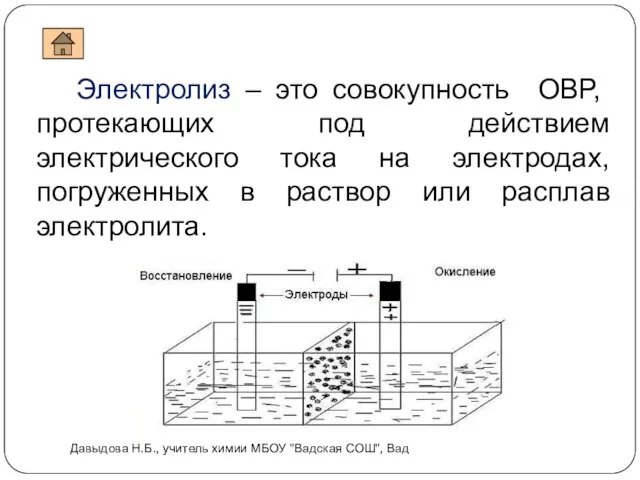
- 4. Электролиз – это совокупность ОВР, протекающих под действием электрического тока на электродах, погруженных в раствор или
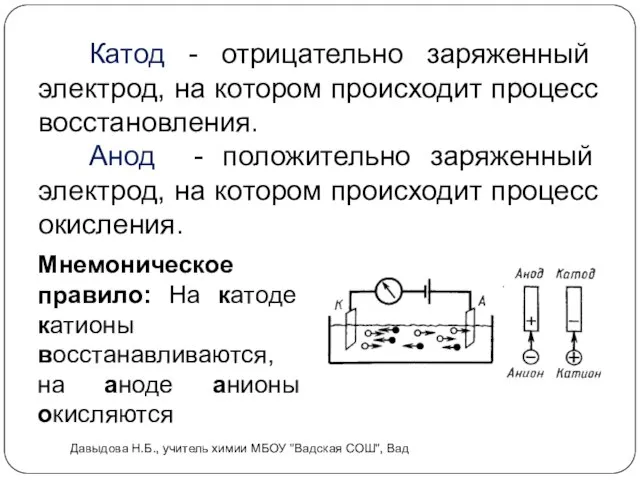
- 5. Катод - отрицательно заряженный электрод, на котором происходит процесс восстановления. Анод - положительно заряженный электрод, на
- 6. Виды анодов: 1. Инертные аноды (нерастворимые, пассивные): материал анода не окисляется, окисляются ионы электролита (платина, графит).
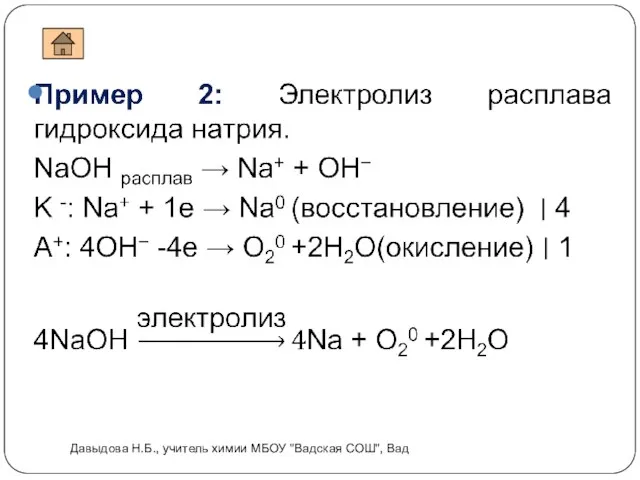
- 7. Электролиз расплавов Давыдова Н.Б., учитель химии МБОУ "Вадская СОШ", Вад
- 8. Давыдова Н.Б., учитель химии МБОУ "Вадская СОШ", Вад
- 9. На катоде: От Li+ до Al 3+ (включительно) восстанавливаются молекулы воды или катионы H+: 2H2O+2e →H2↑+2OH−
- 10. Катодные процессы: От Al 3+ до Н2 восстанавливаются металл и молекулы воды (катионы H+): Men+ +
- 11. Анодные процессы: I. Нерастворимый анод (инертный) Рt, C Окисляются: 1. Анионы бескислородных кислот: I-, Br-, S2-,
- 12. Видеоопыт . Электролиз раствора иодида калия Пример 3: Электролиз раствора иодида калия. Давыдова Н.Б., учитель химии
- 13. Давыдова Н.Б., учитель химии МБОУ "Вадская СОШ", Вад
- 14. Давыдова Н.Б., учитель химии МБОУ "Вадская СОШ", Вад
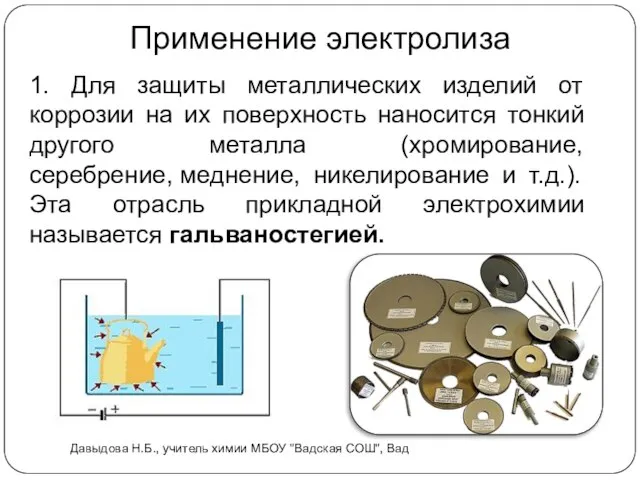
- 15. Применение электролиза 1. Для защиты металлических изделий от коррозии на их поверхность наносится тонкий другого металла
- 16. 2. Гальванопластика - получение точных металлических копий с предметов. С помощью гальванопластики изготавливают клише для печатания
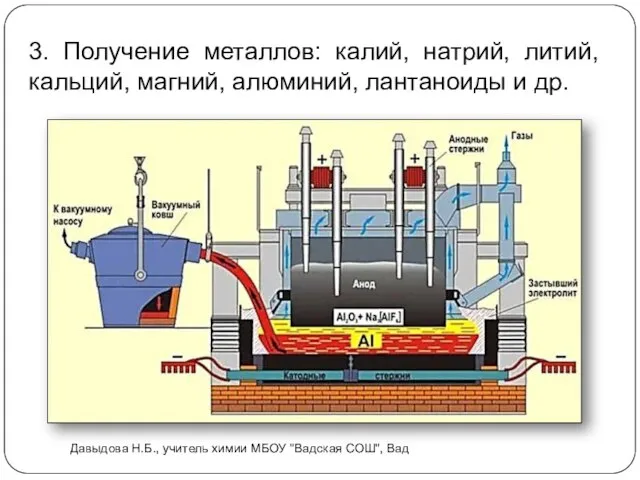
- 17. 3. Получение металлов: калий, натрий, литий, кальций, магний, алюминий, лантаноиды и др. Давыдова Н.Б., учитель химии
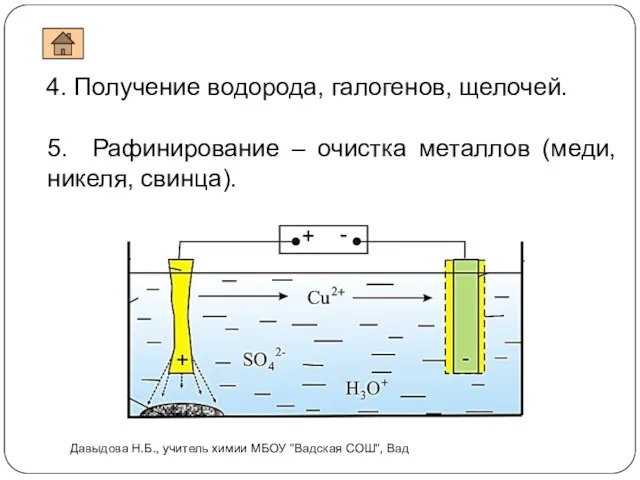
- 18. 4. Получение водорода, галогенов, щелочей. 5. Рафинирование – очистка металлов (меди, никеля, свинца). Давыдова Н.Б., учитель
- 19. Закрепление и применение полученных знаний Базовый уровень сложности 1. При электролизе AgNO3 на катоде выделяется (-ются):
- 20. Закрепление и применение полученных знаний Повышенный уровень сложности 4. Установите соответствие между формулой вещества и продуктами
- 21. Закрепление и применение полученных знаний Повышенный уровень сложности 5. Установите соответствие между формулой соли и продуктом,
- 22. Рефлексия: 1. Что нового вы узнали сегодня на уроке? 2. Что запомнилось? 3. Что понравилось, а
- 23. Домашнее задание: Учебник: Кузнецова Н.Е., Литвинова Т.Н., Левкин А.Н.; под ред. Н. Е. Кузнецовой. Химия: профильный
- 24. 1. Кузнецова Н.Е., Литвинова Т.Н., Левкин А.Н.; под ред. Н. Е. Кузнецовой. Химия: профильный уровень. Ч.1
- 26. Скачать презентацию

















 Общая характеристика неметаллов
Общая характеристика неметаллов Изомерия. Классификация органических веществ.
Изомерия. Классификация органических веществ. Химия спирты одноатомные предельные
Химия спирты одноатомные предельные Композитные материалы
Композитные материалы Демокрит его вклад в развитие взглядов на строение вещества
Демокрит его вклад в развитие взглядов на строение вещества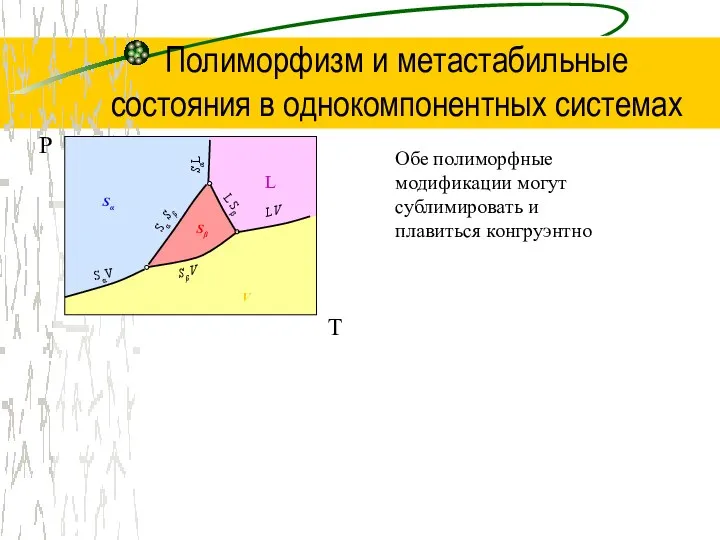 Полиморфизм и метастабильные состояния в однокомпонентных системах
Полиморфизм и метастабильные состояния в однокомпонентных системах Основи масообміну
Основи масообміну Количество вещества. Моль
Количество вещества. Моль Алюміній. Фізичні та хімічні властивості
Алюміній. Фізичні та хімічні властивості Хроматография
Хроматография Углеродистые конструкционные стали
Углеродистые конструкционные стали Жидкокристаллический эластомер как роторный актуатор
Жидкокристаллический эластомер как роторный актуатор Презентация на тему Игра по химии «Остров Периодическая Система»
Презентация на тему Игра по химии «Остров Периодическая Система»  Свойства растворов электролитов
Свойства растворов электролитов Производство аммиака
Производство аммиака Кислород. Общая характеристика, получение и свойства
Кислород. Общая характеристика, получение и свойства Презентация на тему Металлы
Презентация на тему Металлы  Количество вещества, число Авогадро, молярная масса, молярный объём, уравнение связи
Количество вещества, число Авогадро, молярная масса, молярный объём, уравнение связи Алкены
Алкены Презентация на тему Электронное и пространственное строение молекулы метана
Презентация на тему Электронное и пространственное строение молекулы метана  Циклоалканы. Физические свойства
Циклоалканы. Физические свойства Кислород
Кислород Синтетические органические соединения
Синтетические органические соединения Турнир Деда Мороза. Викторина по химии
Турнир Деда Мороза. Викторина по химии Презентация на тему Алмазы Индии
Презентация на тему Алмазы Индии  Алкены
Алкены Значимые личности в химии
Значимые личности в химии Стан електронів у атомі
Стан електронів у атомі