Слайд 21. Алкилирование - получение из галогенпроизводных.
В общем виде процесс можно представить следующей

схемой:
RHal+NH3→RNH2+HHalRHal+NH3→RNH2+HHal
Однако на практике в результате взаимодействия образуется соль амина, например:
CH3CH2−Br+NH3⟶[CH3CH2NH3]+Br−CH3CH2−Br+NH3⟶[CH3CH2NH3]+Br−
В избытке аммиака или под действием щелочи можно выделить первичный амин (этиламин). При последующем бромировании выделенного первичного амина можно аналогично получить вторичный (диэтиламин (CH3CH2)2NH(CH3CH2)2NH ) и затем третичный (триэтиламин (CH3CH2)3N(CH3CH2)3N ) амины. При дальнейшем алкилировании образуется четвертичная аммонийная соль [(CH3CH2)4N]+Br−
Слайд 32. Восстановление нитросоединений. Реакция Зинина.
Восстановление может осуществляться активным водородом в момент его выделения, например,

при взаимодействии соляной кислоты и металлов (Fe, Zn)
RNO2−→−−−−Fe+HClRNH2+2H2ORNO2→Fe+HClRNH2+2H2O
Этот способ наиболее часто используется при получении первичных алкиламинов.
Для получения анилина из нитробензола в промышленности используют нагревание с металлическим железом и водяным паром:
C6H5NO2+6[H]−→−−−−−Fe+H2O,tC6H5NH2+2H2OC6H5NO2+6[H]→Fe+H2O,tC6H5NH2+2H2O
Впервые анилин из нитробензола был получен русским химиком Н.Н. Зининым в 1842 г.:
C6H5NO2+3(NH4)2S→C6H5NH2+3S↓+6NH3+2H2O
Слайд 43. Взаимодействие спиртов с аммиаком.
Амины (первичные, вторичные и третичные) могут быть получены пропусканием

смеси паров спирта и аммиака через нагретые оксиды двухвалентных и трехвалентных металлов (например, алюминия) или тонко измельченные металлы группы железа, играющие роль катализаторов:
NH3+CH3−OH−→−Fe,tCH3NH2+H2O
Слайд 5Амины и природа
Амины широко распространены в природе, так как образуются при гниении

живых организмов. Например, с триметиламином вы встречались неоднократно. Запах селедочного рассола обусловлен именно этим веществом.




 Электролиз. Правила электролиза
Электролиз. Правила электролиза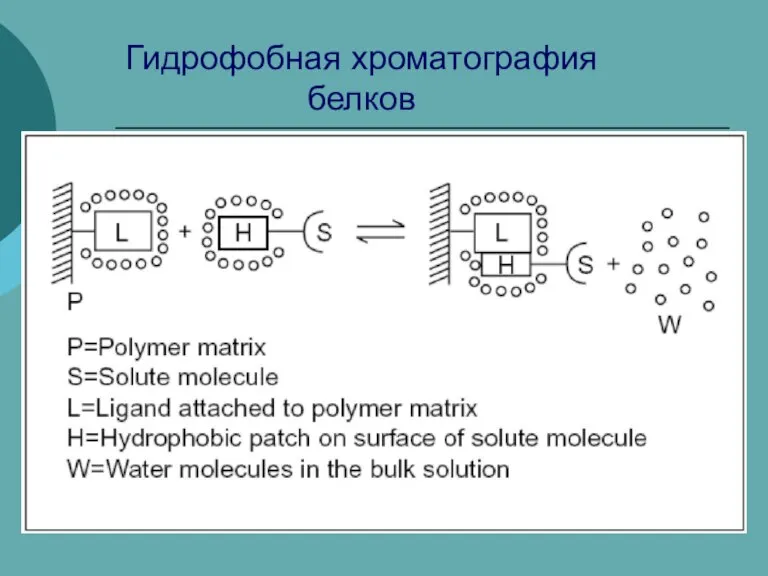 Гидрофобная хроматография белков
Гидрофобная хроматография белков 7609f31d31514fe19b6df19a98197139 (1)
7609f31d31514fe19b6df19a98197139 (1) Бикомпонентные покрытия
Бикомпонентные покрытия Сера и ее соединения
Сера и ее соединения Презентация на тему Строение атома Химическая связь
Презентация на тему Строение атома Химическая связь  Взаимодействие плазмы с поверхностью. Проблемы термоядерного реактора
Взаимодействие плазмы с поверхностью. Проблемы термоядерного реактора Определение времени прохождения диффузии
Определение времени прохождения диффузии Презентация на тему Сплавы металлов
Презентация на тему Сплавы металлов  Химия. Спирты
Химия. Спирты Углерод и его аллотропные модификации. Органическая химия - химия углерода
Углерод и его аллотропные модификации. Органическая химия - химия углерода Газообразные (газ)
Газообразные (газ) Химические свойства алкенов. Получение
Химические свойства алкенов. Получение Хлорорганические соединения
Хлорорганические соединения Химические элементы
Химические элементы Соли: получение
Соли: получение Азотная кислота
Азотная кислота Белки-1 2020
Белки-1 2020 Основания (Ме+n(ОН)-n)
Основания (Ме+n(ОН)-n) Расчётно-графическая работа по теме Мыловарение
Расчётно-графическая работа по теме Мыловарение Альдегиды. Получение и применение
Альдегиды. Получение и применение Презентация на тему Изотопы
Презентация на тему Изотопы  Типы химических реакций
Типы химических реакций Растительные жиры. Пальмовое масло
Растительные жиры. Пальмовое масло Химия в быту
Химия в быту Кристаллическое строение металлов и сплавов. Аморфные и кристаллические тела
Кристаллическое строение металлов и сплавов. Аморфные и кристаллические тела Алкены. Ҳимические свойства алкенов
Алкены. Ҳимические свойства алкенов Порядок в жидкостях
Порядок в жидкостях