Содержание
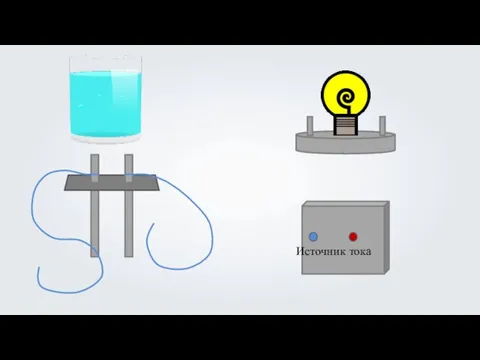
- 2. Растворы веществ (по способности проводить электрический ток) электролиты кислота
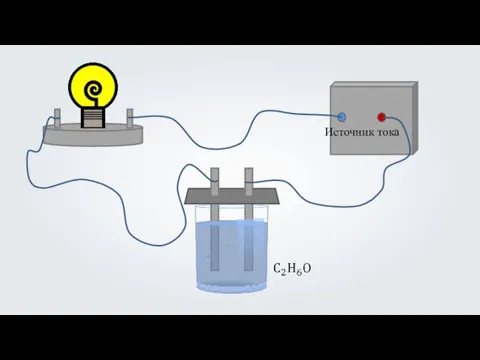
- 3. Растворы веществ (по способности проводить электрический ток) электролиты 1 неэлектролиты Rainer Zenz спирт кислота
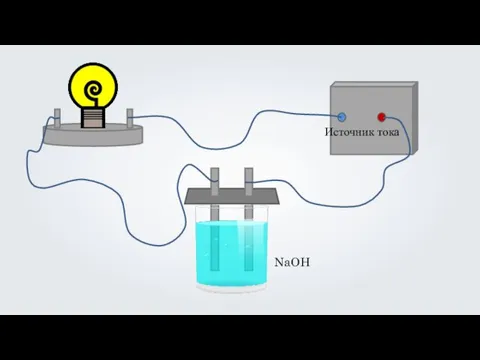
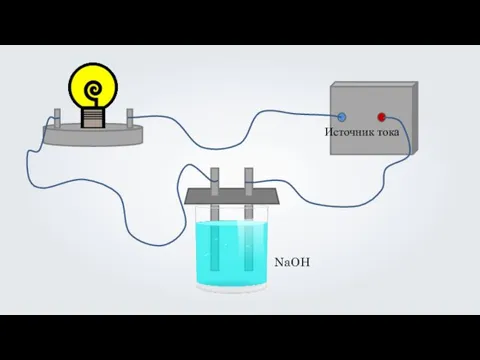
- 5. NaOH
- 6. NaOH
- 8. Растворы веществ
- 9. Растворы веществ электролиты вещества, растворы которых проводят электрический ток.
- 10. Растворы веществ электролиты 1 неэлектролиты вещества, растворы которых проводят электрический ток. вещества, растворы которых не проводят
- 13. Майкл Фарадей XIX век — получено представление об образовании ионов в растворах электролитов.
- 14. Сванте Аррениус 1877 год — сформулирована теория электролитической диссоциации.
- 15. Электролитическая диссоциация — процесс распада электролита на ионы.
- 16. Иван Алексеевич Каблуков Владимир Александрович Кистяковский
- 17. При растворении электролита происходит химическое взаимодействие растворённого вещества с водой, которое приводит к образованию гидратов, которые
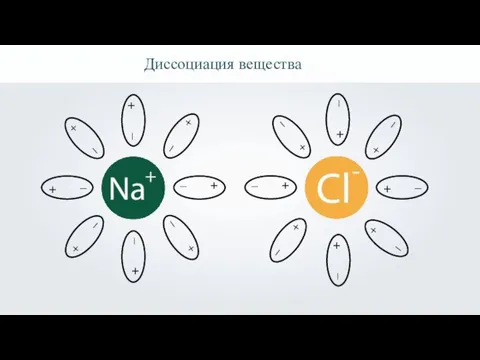
- 18. Диссоциация вещества
- 19. Диссоциация вещества
- 20. H2O CaCl2 хлорид кальция вода Диссоциация хлорида кальция
- 21. Диссоциация хлорида кальция - - -
- 22. Процессы при диссоциации веществ в воде 1. Ориентация двухполярных молекул воды около ионов кристалла. 2. Взаимодействие
- 23. CaCl2 = Ca2+ + 2Cl Уравнение диссоциации хлорида кальция Каждая частица хлорида кальция диссоциирует на катионы
- 24. Ассоциация — процесс, при котором хаотически движущиеся гидратированные ионы могут столкнуться и объединиться.
- 25. Степень диссоциации (α) — это отношение количества вещества электролита, распавшегося на ионы (nД), к общему количеству
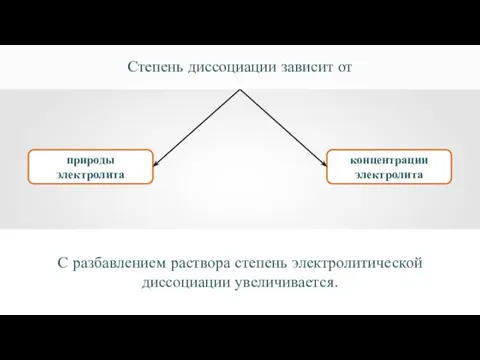
- 26. природы электролита концентрации электролита Степень диссоциации зависит от С разбавлением раствора степень электролитической диссоциации увеличивается.
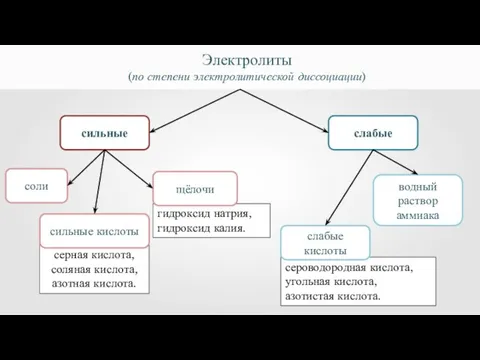
- 27. сильные слабые Электролиты (по степени электролитической диссоциации) соли гидроксид натрия, гидроксид калия. щёлочи водный раствор аммиака
- 28. Растворы веществ (по способности проводить электрический ток) электролиты 1 неэлектролиты Rainer Zenz спирт кислота
- 30. Скачать презентацию




















 Белки
Белки Разбор заданий
Разбор заданий Exotermické a endotermické reakcie
Exotermické a endotermické reakcie Роль органической химии в производстве и повседневной жизни человека
Роль органической химии в производстве и повседневной жизни человека Увлекательный мир химии
Увлекательный мир химии Nevarne snovi
Nevarne snovi Химики на службе у дорог
Химики на службе у дорог Способы получения веществ 14 (IVА) группы элементов
Способы получения веществ 14 (IVА) группы элементов Алкины в жизни человека
Алкины в жизни человека Жири. Склад жирів, фізичні властивості. Природні й гідрогенізовані жири. Біологічна роль жирів
Жири. Склад жирів, фізичні властивості. Природні й гідрогенізовані жири. Біологічна роль жирів Соляная кислота и ее свойства
Соляная кислота и ее свойства Степень окисления
Степень окисления Титан — металл фей
Титан — металл фей Природные смолы: мирра, ладан и шеллак
Природные смолы: мирра, ладан и шеллак Кристаллическое строение металлов и сплавов. Аморфные и кристаллические тела
Кристаллическое строение металлов и сплавов. Аморфные и кристаллические тела Электролитическая диссоциация
Электролитическая диссоциация 03. Основы номенклатуры
03. Основы номенклатуры Коды Менделеева
Коды Менделеева Презентация на тему Фуллерены и нанотрубки
Презентация на тему Фуллерены и нанотрубки  Алкены. Непредельные углеводороды
Алкены. Непредельные углеводороды Системно-деятельностный подход в обучении химии
Системно-деятельностный подход в обучении химии Добыча золота в России По теме «Внешние эффекты и права собственности»
Добыча золота в России По теме «Внешние эффекты и права собственности» Решение расчетных задач по химии
Решение расчетных задач по химии Prezentatsia_k_uroku
Prezentatsia_k_uroku Общие способы получения металлов
Общие способы получения металлов Типичные экспериментальные кинетические данные
Типичные экспериментальные кинетические данные Типы химической связи и виды кристаллических решеток
Типы химической связи и виды кристаллических решеток Роль элементов 5 группы
Роль элементов 5 группы