Слайд 2Цель урока:
знать названия, размер и расположение протона, нейтрона и электрона в

атоме.
знать подробную структуру атома в отношении протонов, нейтронов и электронов (только первых 20 элементов); знать значение числа протонов и числа нуклонов.
уметь объяснить полное описание ядра для названия элемента и определения количества фундаментальных частиц.
Слайд 3Цели обучения
описывать строение атома
знать понятие изотоп
определять состав атомного ядра нуклидов первых

20 элементов
описывать элемент по названию и по количеству частиц, содержащихся в его атоме
Слайд 4Ожидаемый результат
Знает названия субатомных частиц атома, структуру расположения и их заряд.
Знает что

атомный номер совпадает числами протонов и электронов.
Умеет находить число нейтронов использовав атомный номер и массовый номер.
Может определить атомное и массовое число с помощью субатомных частиц каждого элемента.
Может определить число субатомных частиц используя полное описание ядра.
Слайд 5XIX в было доказано, что атом делим, что он состоит из более

мелких или элементарных частиц.
Атом-это электронейтральная система взаимодействия элементарных частиц, состоящая из ядра и электронной оболочки.
Слайд 7Запомните!
Заряд ядра определятся только количеством протонов и равен атомному номеру элемента и

обозначается Z .
Количество электронов равно количеству протонов.
Общее число нуклонов в ядре называется массовым числом и обозначается А
Количество нейтронов можно узнать по разности между массой атома количеством протонов (N=A-Z).
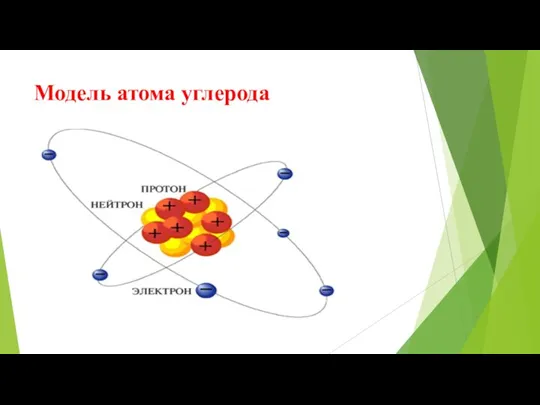
Слайд 8Состав атома углерода.
Z=+6
P+= 6
e−=6
N=A-Z
N=12-6=6

Слайд 10Задание
Подпишите под рисунками химические знаки и названия частиц.

Слайд 11Задание:
Определите количество элементарных частиц в атоме кислорода, азота, натрия, углерода, хлора и

бора, данные занесите в таблицу и зарисуйте модель строения атома
Название элемента
Химический знак
Количество
протонов
Количество
нейтронов
Количество
электронов
Слайд 12Домашнее задание:
Учащиеся выбирают один уровень по своему желанию
Уровень А (средний) изготовить модель

строения атома одного из 20 первых элементов
Уровень В (творческий) изготовить 2 модели строения атома одного из 20 первых элементов
Уровень С (креативный) создать видео о модели строения атома одного из 20 первых элементов
Слайд 13РЕФЛЕКСИЯ
-Были ли цели урока/цели обучения реалистичными?
-Все ли учащиеся достигли ЦО? Если нет,

то почему?
-Правильно ли проведена дифференциация на уроке?
-Выдержаны ли были временные этапы урока?
-Какие отступления были от плана урока и почему?











 Свойства кислорода. Оксиды
Свойства кислорода. Оксиды Задача №8: Не тормози. Команда: Карбораны
Задача №8: Не тормози. Команда: Карбораны Натуральный каучук
Натуральный каучук Электростанция в кармане
Электростанция в кармане Железо. Физические свойства
Железо. Физические свойства Общая характеристика неметаллов подгруппы кислород
Общая характеристика неметаллов подгруппы кислород Полимеры
Полимеры Смог як хімічне явище
Смог як хімічне явище Презентация на тему Классы неорганических веществ
Презентация на тему Классы неорганических веществ  Массовая доля элемента в веществе
Массовая доля элемента в веществе Химия и производство
Химия и производство Стеклообразование, структура и свойства стекол системы Na2O – B2O3 – SiO2 на основе комплексного борсодержащего сырья
Стеклообразование, структура и свойства стекол системы Na2O – B2O3 – SiO2 на основе комплексного борсодержащего сырья Использование информационноко-ммуникационных технологий по формированию УУД на уроках химии
Использование информационноко-ммуникационных технологий по формированию УУД на уроках химии Алкины. Ацетилен
Алкины. Ацетилен Оксиды
Оксиды Непредельные углеводороды
Непредельные углеводороды Наркотики и прекурсоры
Наркотики и прекурсоры Повторение классов соединений. Составление формул по названиям
Повторение классов соединений. Составление формул по названиям Основные классы неорганических соединений
Основные классы неорганических соединений Презентация на тему Степень окисления
Презентация на тему Степень окисления  Кислоты основания и соли как электролиты
Кислоты основания и соли как электролиты 14257fc50bc406ef33f49ad14aa3f48b
14257fc50bc406ef33f49ad14aa3f48b Химия и производство
Химия и производство Реакции разложения
Реакции разложения Химическая кибернетика
Химическая кибернетика Титриметрический анализ. Основные понятия
Титриметрический анализ. Основные понятия Метод окислительно - восстановительного титрования
Метод окислительно - восстановительного титрования Химия на войне
Химия на войне