Содержание
- 2. Одноатомные предельные спирты Молекулы спиртов содержат одну (одноатомные) гидроксильную группу – ОН-. Группа –ОН является функциональной
- 3. Номенклатура и изомерия Причины: Изомерия углеродного скелета – прямая или разветвленная цепь; Положение гидроксильной группы. Пример:
- 6. Многоатомные спирты Этиленгликоль или этандиол-1,2 Н2С1 – ОН │ Н2С2 – ОН двухатомный спирт, ЯД! Глицерин
- 7. Номенклатура и изомерия Основа названия – название предельного углеводорода с таким же числом атомов углерода с
- 8. Физические свойства спиртов Одноатомные предельные спирты – жидкости с С12Н25ОН твердые вещества С увеличением молекулярной массы
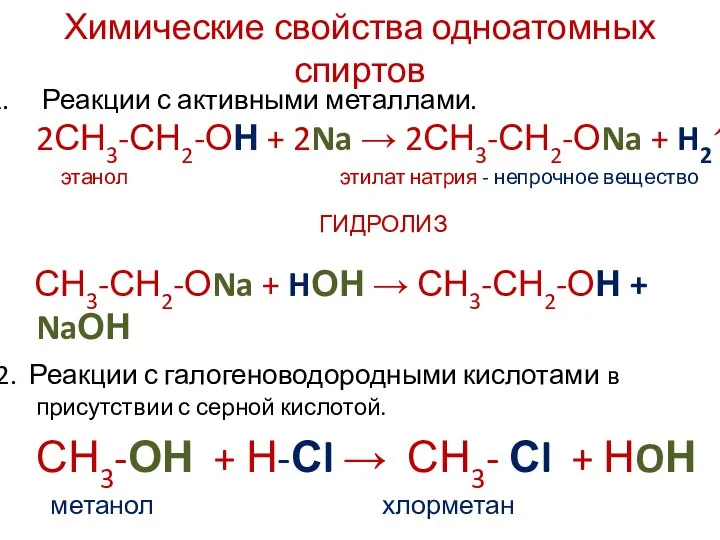
- 9. Химические свойства одноатомных спиртов Реакции с активными металлами. 2СН3-СН2-ОН + 2Na → 2СН3-СН2-ОNa + H2↑ этанол
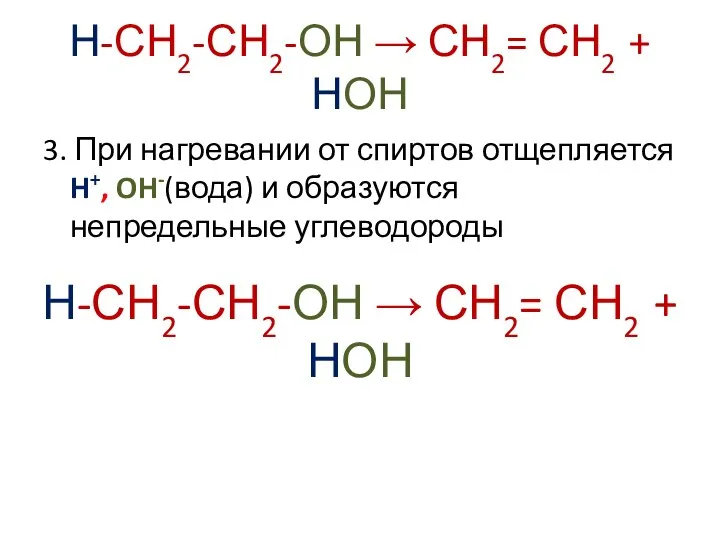
- 10. Н-СН2-СН2-ОН → СН2= СН2 + НОН 3. При нагревании от спиртов отщепляется H+, OH-(вода) и образуются
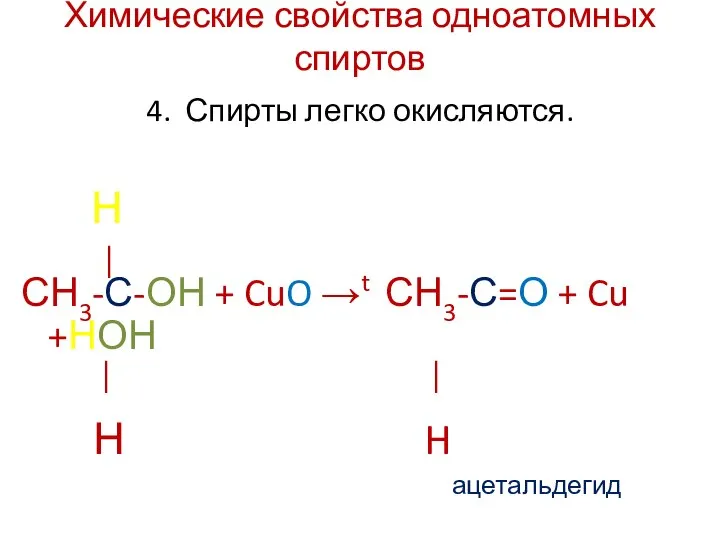
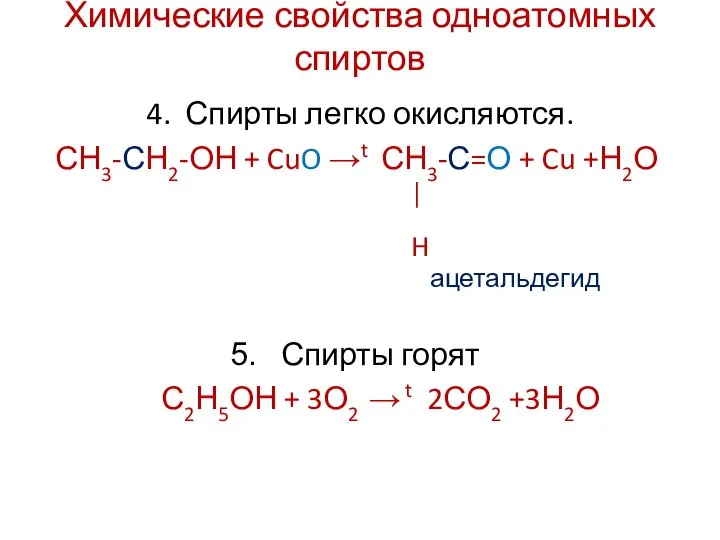
- 11. Химические свойства одноатомных спиртов 4. Спирты легко окисляются. Н │ СН3-С-ОН + CuO →t СН3-С=О +
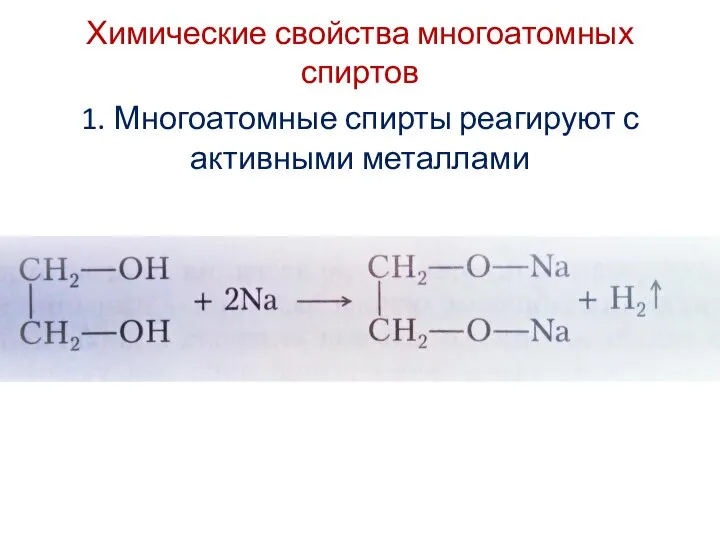
- 12. Химические свойства многоатомных спиртов 1. Многоатомные спирты реагируют с активными металлами
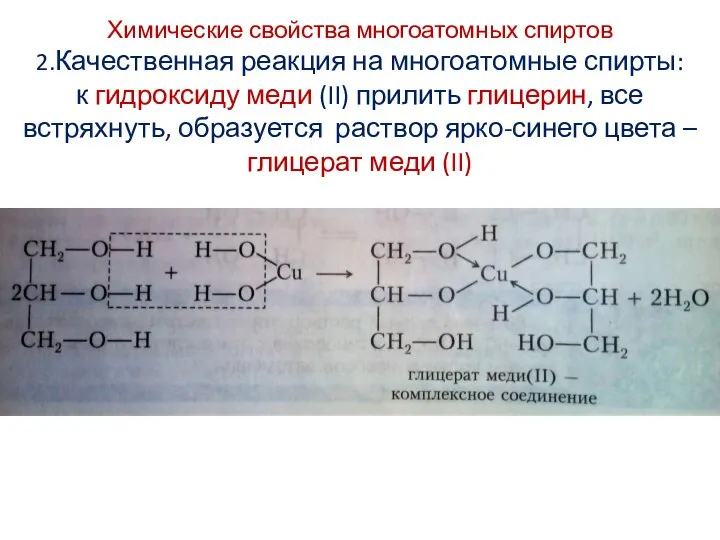
- 13. Химические свойства многоатомных спиртов 2.Качественная реакция на многоатомные спирты: к гидроксиду меди (II) прилить глицерин, все
- 14. Химические свойства многоатомных спиртов 3. Глицерин взаимодействует с азотной кислотой
- 15. Задания для студентов 1. Напишите структурные формулы всех изомеров гексилового спирта (гексанола). Дайте им названия. 2.
- 16. Химические свойства одноатомных спиртов Реакции с активными металлами. 2СН3-СН2-ОН + 2Na → 2СН3-СН2-ОNa + H2↑ этанол
- 17. Химические свойства одноатомных спиртов 4. Спирты легко окисляются. СН3-СН2-ОН + CuO →t СН3-С=О + Cu +Н2О
- 22. Скачать презентацию













 Развитие познавательной активности творческих способностей и индивидуализация на уроках химии
Развитие познавательной активности творческих способностей и индивидуализация на уроках химии Углеродистые стали
Углеродистые стали Целестин
Целестин Презентацию выполнила ученица 10 класса Поликарпова Диана 2010 год
Презентацию выполнила ученица 10 класса Поликарпова Диана 2010 год Гальванический элемент
Гальванический элемент Углеводы. Классификация углеводов
Углеводы. Классификация углеводов Степень окисления. Классификация неорганических соединений
Степень окисления. Классификация неорганических соединений Катаболизм пуриновых нуклеотидов
Катаболизм пуриновых нуклеотидов Органическая химия
Органическая химия Соединения азота в атмосфере. Лекция 4
Соединения азота в атмосфере. Лекция 4 Структура к свойства веществ
Структура к свойства веществ Химические вещества парабены
Химические вещества парабены Влияние меди на коррозию низколегиованных сталей
Влияние меди на коррозию низколегиованных сталей Серная кислота
Серная кислота Основные свойства и опасности нефти. Безопасность для танкеров
Основные свойства и опасности нефти. Безопасность для танкеров Окислители в пиросоставах
Окислители в пиросоставах Вода. Строение молекулы. Водородная связь. Физические и химические свойства
Вода. Строение молекулы. Водородная связь. Физические и химические свойства Презентация на тему Гидролиз
Презентация на тему Гидролиз  Электролиз
Электролиз Презентация на тему Глюкоза (10 класс)
Презентация на тему Глюкоза (10 класс)  Основания и их свойства
Основания и их свойства Презентация на тему Многоатомные спирты
Презентация на тему Многоатомные спирты  Жидкое состояние вещества
Жидкое состояние вещества Поделочный камень родонит
Поделочный камень родонит Фосфор. Аллотропия фосфора. Физические и химические свойства фосфора
Фосфор. Аллотропия фосфора. Физические и химические свойства фосфора Кремний и 4 группа. 9 класс
Кремний и 4 группа. 9 класс Получение металлов
Получение металлов Степени окисления
Степени окисления