Слайд 2Что такое электролиз?
Электро́лиз — физико-химический процесс, состоящий в выделении на электродах составных

частей растворённых веществ или других веществ, являющихся результатом вторичных реакций на электродах, который возникает при прохождении электрического тока через раствор, либо расплав электролита.
Слайд 3Применение электролиза
Электролиз широко применяется в современной промышленности. В частности, электролиз является одним

из способов промышленного получения алюминия , меди, водорода, диоксида марганца[2], пероксида водорода. Большое количество металлов извлекается из руд и подвергается переработке с помощью электролиза (электроэкстракция, электрорафинирование). Также электролиз является основным процессом, благодаря которому функционирует химический источник тока.
Электролиз находит применение в очистке сточных вод (процессы электрокоагуляции, электроэкстракции, электрофлотации).
Применяется для получения многих веществ (металлов, водорода, хлора и др.), при нанесении металлических покрытий (гальваностегия), воспроизведении формы предметов (гальванопластика).
Слайд 5Законы электролиза Фарадея
Зако́ны электро́лиза Фараде́я являются количественными соотношениями, основанными на электрохимических исследованиях, опубликованных Майклом Фарадеем в 1836

году.
Слайд 6Мнемоническое правило
Для запоминания катодных и анодных процессов в электрохимии существует следующее мнемоническое

правило:
У анода анионы окисляются.
На катоде катионы восстанавливаются.
В первой строке все слова начинаются с гласной буквы, во второй — с согласной.
Или проще:
КАТод — КАТионы (ионы у катода)
АНод — АНионы (ионы у анода)
Слайд 7Электролиз в газах
Электролиз в газах, при наличии ионизатора, объясняется тем, что при

прохождении через них постоянного электрического тока наблюдается выделение веществ на электродах. Законы Фарадея в газах не действительны, но существуют несколько закономерностей:
при отсутствии ионизатора электролиз проводиться не будет, даже при высоком напряжении;
электролизу подвергаются только бескислородные кислоты в газообразном состоянии и некоторые газы;
уравнения электролиза, как в электролитах, так и в газах, всегда остаются постоянными.
Слайд 8Некоторые схемы электролиза:
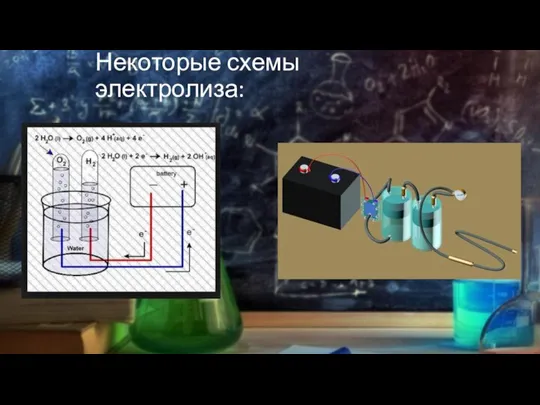
Слайд 9Примеры Электрохимических уравнений:









 Альдегиды. Общая формула
Альдегиды. Общая формула Спирты. Понятие о спиртах
Спирты. Понятие о спиртах Презентация на тему Дисперсные системы и растворы
Презентация на тему Дисперсные системы и растворы  Металлы. Общие свойства
Металлы. Общие свойства Научный эксперимент в химической технологии
Научный эксперимент в химической технологии Вспоминаем химию
Вспоминаем химию Свойства отдельных классов неорганических и органических веществ на примере лекарственных средств
Свойства отдельных классов неорганических и органических веществ на примере лекарственных средств Электролиз (катод)
Электролиз (катод) Цикл трикарбоновых кислот (цикл Кребса)
Цикл трикарбоновых кислот (цикл Кребса) Классификация химических реакций
Классификация химических реакций Вуглеводи. Визначення вуглеводів
Вуглеводи. Визначення вуглеводів Примеры методов разделения белков (фракционирования)
Примеры методов разделения белков (фракционирования) Дезактивація радіаційних речовин у зоні ядерного ураження
Дезактивація радіаційних речовин у зоні ядерного ураження Молекулы. Свойства молекул
Молекулы. Свойства молекул Полимеры
Полимеры Енергетика хімічних реакцій
Енергетика хімічних реакцій Полипропилен (ПП)
Полипропилен (ПП) Металлы и их соединения
Металлы и их соединения Перициклические реакции
Перициклические реакции Органическая химия. Химические свойства и типы реакций. (9 класс)
Органическая химия. Химические свойства и типы реакций. (9 класс) Общие химические свойства металлов
Общие химические свойства металлов Кислоты: состав, классификация, номенклатура, получение
Кислоты: состав, классификация, номенклатура, получение Электролиз
Электролиз Периодический закон. Периодическая таблица химических элементов. 8 класс
Периодический закон. Периодическая таблица химических элементов. 8 класс Нефть: история и ее применение
Нефть: история и ее применение Понятие о скорости химической реакции
Понятие о скорости химической реакции Алкины. Понятие об алкинах
Алкины. Понятие об алкинах Непредельные углеводороды. Алкены
Непредельные углеводороды. Алкены