Содержание
- 2. Необходимость проведения расчетов по горению топлива Большинство современных высокотемпературных технологий связаны со сжиганием топлив, состав и
- 3. Топливо, его виды и основные характеристики Топливом называют горючее вещество, которое при окислении (горении) выделяет значительное
- 4. Принципы топливной политики 1. Планомерный рост добычи всех видов топлив. 2. Преимущественное развитие добычи наиболее экономичных
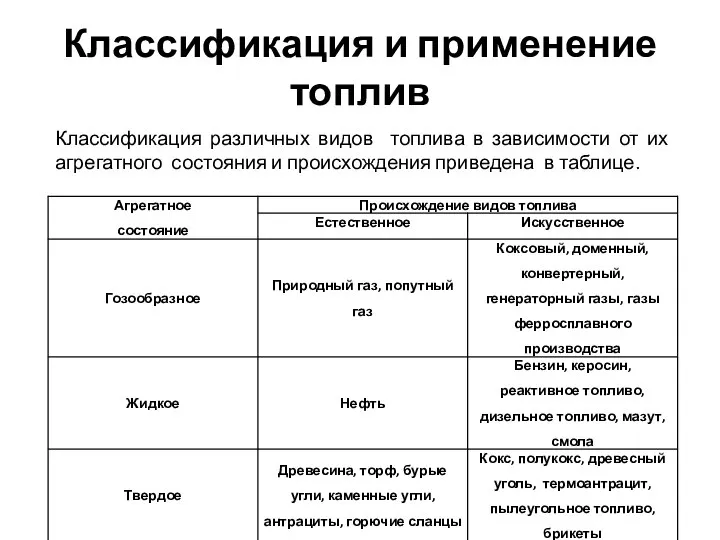
- 5. Классификация и применение топлив Классификация различных видов топлива в зависимости от их агрегатного состояния и происхождения
- 6. Химический состав жидких и твердых видов топлива Эти топлива представляют собой вещества органического происхождения. Оценка их
- 7. Виды анализов состава жидких и твердых топлив Различают два вида анализов: технический и элементарный. Первый доступен
- 8. Различные массы жидкого и твердого топлива Элементарный состав жидкого и твердого видов топлива может быть отнесен
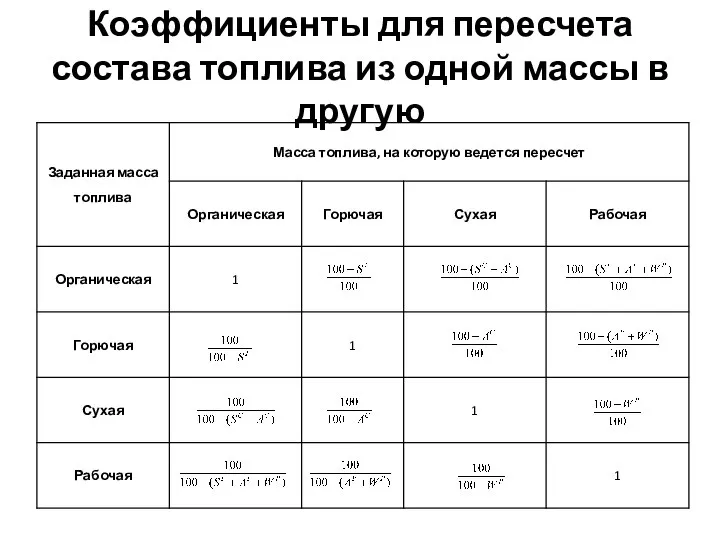
- 9. Коэффициенты для пересчета состава топлива из одной массы в другую
- 10. Химический состав газообразных видов топлива Газообразные виды топлива представляют собой смесь газов: водорода Н2, метана СН4,
- 11. Химический состав газообразного топлива определяют экспериментально с помощью приборов –газоанализаторов в объемных процентах на сухую массу
- 12. Тепловые характеристики органических видов топлива Теплота сгорания топлива. Представляет собой количество теплоты Q, кДж, которое выделяется
- 13. Влага в продуктах сгорания топлива образуется при горении водорода HP, а также при испарении начальной влаги
- 14. Методы определения теплоты сгорания топлива Их два: экспериментальный и расчетный. При экспериментальном методе заданную навеску топлива
- 15. Для жидкого и твердого топлива используют формулу Д.И.Менделеева: =339Cp +1030Hp–109(OР–SР)–25Wp. Для газообразного топлива формула имеет вид:
- 16. Условное топливо Для сравнения показателей тепловой работы тепловых агрегатов, применяющих различные виды топлива, введено понятие условного
- 17. Характеристики окислителя. Коэффициент избытка воздуха Для горения топлива в качестве окислителя используется кислород. Он поступает с
- 18. РАСЧЕТЫ ПРОЦЕССА ГОРЕНИЯ ТОПЛИВА
- 19. Расчеты процесса горения топлива Производят с целью определения теплоты сгорания топлива, расхода воздуха, количества и состава
- 20. Аналитический метод расчета процесса горения жидкого и твердого топлива Определение расхода кислорода и воздуха на горение
- 21. Кислород топлива ОР может участвовать в реакциях окисления. При массе одного моля О2, равной 32 кг,
- 22. где – содержание водяного пара, условно отнесенное к сухому воздуху, г/ м3 ; 18– молекулярная масса
- 23. Определение выхода и состава продуктов горения жидкого и твердого топлива Продукты полного горения жидкого и твердого
- 24. При сгорании 1 кг водорода образуется влаги в количестве 22,4 : 2=11,2 м3. В топливе содержится
- 25. Объем азота в продуктах сгорания складывается из азота, содержащегося в топливе (NР) и азота поступающего с
- 26. м3/кг. м3/кг. м3/кг. Тогда м3/кг.
- 27. Аналитический метод расчета процесса горения газообразного топлива Определение расхода кислорода и воздуха на горение Состав влажного
- 28. В данном случае удобнее воспользоваться объемным соотношением горючего и кислорода. Тогда теоретически необходимый объем кислорода для
- 29. Определение выхода и состава продуктов горения газообразного топлива Выход продуктов горения V0 представляет собой сумму оксидов
- 30. Состав продуктов горения для этих условий (⍺ = 1,0) будет следующим: Для практических условий горения при
- 31. Состав продуктов горения для ⍺ > 1,0 можно определить по формуле: где i относится к тому
- 32. Приближенный метод расчета процесса горения топлива Часто при решении инженерных задач не требуется особой точности и
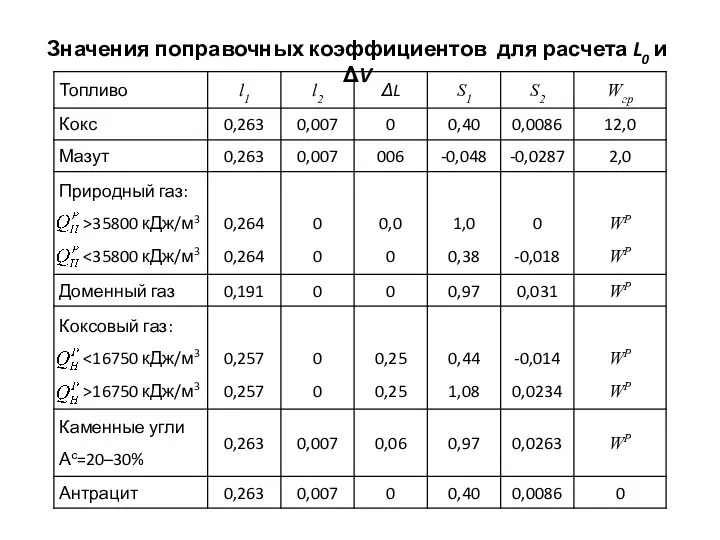
- 33. Значения поправочных коэффициентов для расчета L0 и ΔV
- 34. Расчет температур горения топлива Производится на основе анализа и решения уравнения теплового баланса процесса горения топлива,
- 35. – тепловая энергия подогретого топлива, равная – тепловая энергия, вносимая подогретыми материалами и теплота экзотермических реакций.
- 36. – потери тепловой энергии на разогрев кладки рабочего пространства теплового агрегата; – невязка теплового баланса. Принимаем
- 37. Если учитывается только теплота диссоциации продуктов горения при температуре горения, т.е. то такую температуру называют теоретической
- 38. Тогда Для отыскания теоретических и балансовых температур процесса горения определяют теплосодержание 1 м3 продуктов горения или
- 39. Затем по i–t – диаграммам С.Г. Тройба находят и предварительно определив параметр: Необходимые для расчетов по
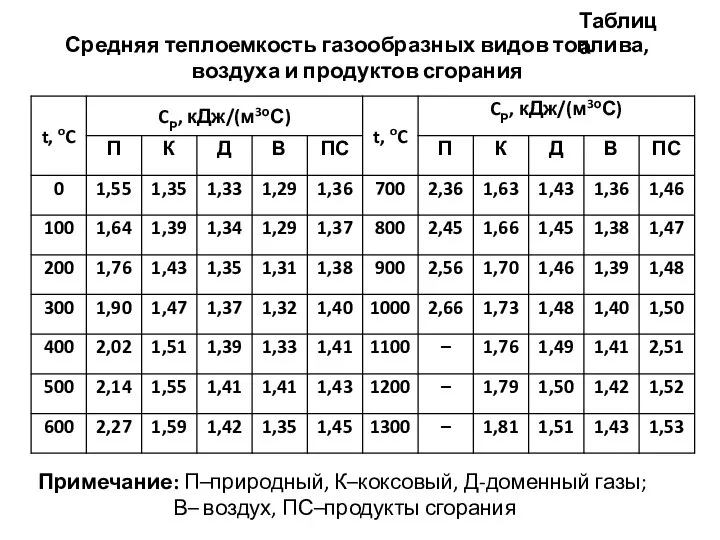
- 40. Средняя теплоемкость газообразных видов топлива, воздуха и продуктов сгорания Примечание: П–природный, К–коксовый, Д-доменный газы; В– воздух,
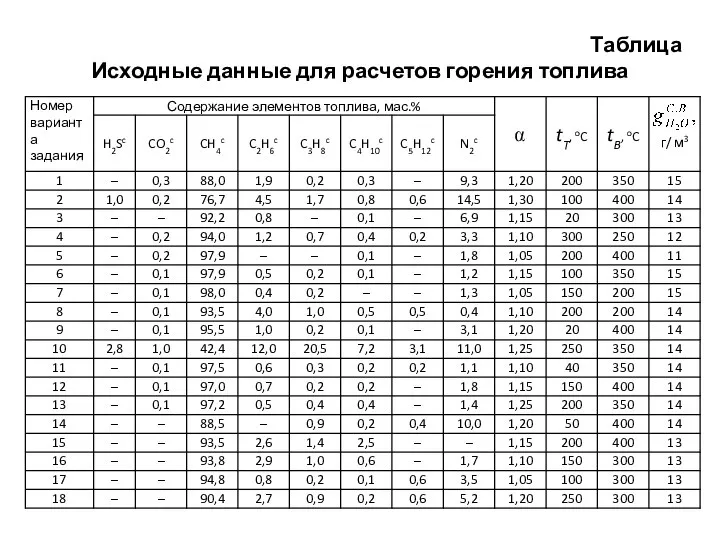
- 41. Таблица Исходные данные для расчетов горения топлива
- 43. Скачать презентацию



































 Нобелевские лауреаты и их достижения
Нобелевские лауреаты и их достижения Алканы. Строение,номенклатура, изомерия
Алканы. Строение,номенклатура, изомерия Органическая химия
Органическая химия Презентация на тему Увлекательные факты из жизни Менделеева
Презентация на тему Увлекательные факты из жизни Менделеева  Презентация на тему Изучение реакции среды в зависимости от типа гидролиза соли
Презентация на тему Изучение реакции среды в зависимости от типа гидролиза соли  Растворы электролитов
Растворы электролитов Пятичленные гетероциклы с двумя и более атомами азота
Пятичленные гетероциклы с двумя и более атомами азота Гидролиз солей
Гидролиз солей Скорость химических реакций
Скорость химических реакций Веселый химический КВН
Веселый химический КВН Понятие об ароматических спиртах и фенолах. Особенности строения фенола
Понятие об ароматических спиртах и фенолах. Особенности строения фенола Химическая коррозия
Химическая коррозия Строение атома
Строение атома Проблемы и меры по защите окружающей среды ПМР
Проблемы и меры по защите окружающей среды ПМР Алкены. Гомологический ряд алкенов. Изомерия алкенов
Алкены. Гомологический ряд алкенов. Изомерия алкенов Современные способы защиты ОТТ
Современные способы защиты ОТТ Закон сохранения массы веществ. 8 класс
Закон сохранения массы веществ. 8 класс Криогенный разрыв пласта
Криогенный разрыв пласта Виготовлення водних розчинів з заданою масовою часткою розчиненої речовини
Виготовлення водних розчинів з заданою масовою часткою розчиненої речовини Применение неметаллов
Применение неметаллов Растворение
Растворение алотропні модифікації неметалів
алотропні модифікації неметалів Закон Авогадро. Молярный объём газов
Закон Авогадро. Молярный объём газов Разбор заданий на амины
Разбор заданий на амины Интеллектуальный турнир для старшеклассников Умножая таланты 2020
Интеллектуальный турнир для старшеклассников Умножая таланты 2020 Презентация на тему Теория электролитической диссоциации обобщающий урок
Презентация на тему Теория электролитической диссоциации обобщающий урок  Теория химического строения органических веществ А.М. Бутлерова
Теория химического строения органических веществ А.М. Бутлерова Сода: мифы и реальность
Сода: мифы и реальность