Содержание
- 2. Электролиз – это окислительно-восстановительный процесс, протекающий на электродах, при пропускании постоянного электрического тока через раствор или
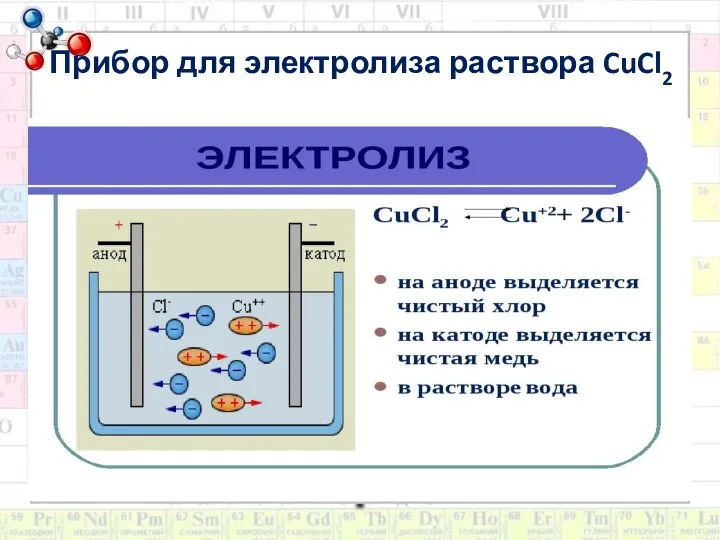
- 6. Прибор для электролиза раствора CuCl2
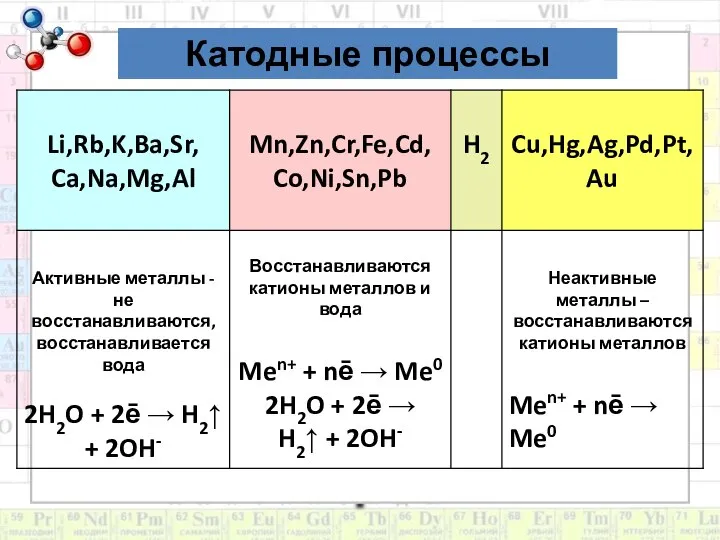
- 7. Катодные процессы: Катионы металлов после Н (от Cu2+ до Au3+) полностью восстанавливаются на катоде. 2. Катионы
- 8. Катодные процессы
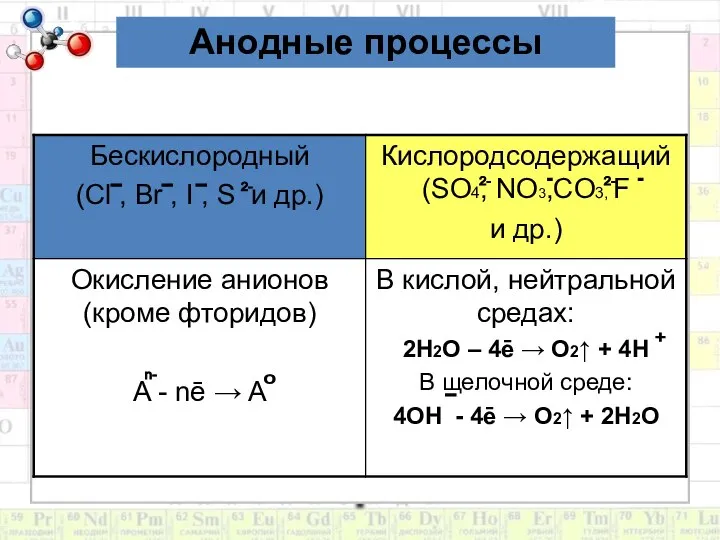
- 9. Анодные процессы В первую очередь на аноде окисляются бескислородные анионы: S²ˉ, Iˉ, Brˉ, Clˉ (кроме Fˉ
- 10. + n- 0 Анодные процессы
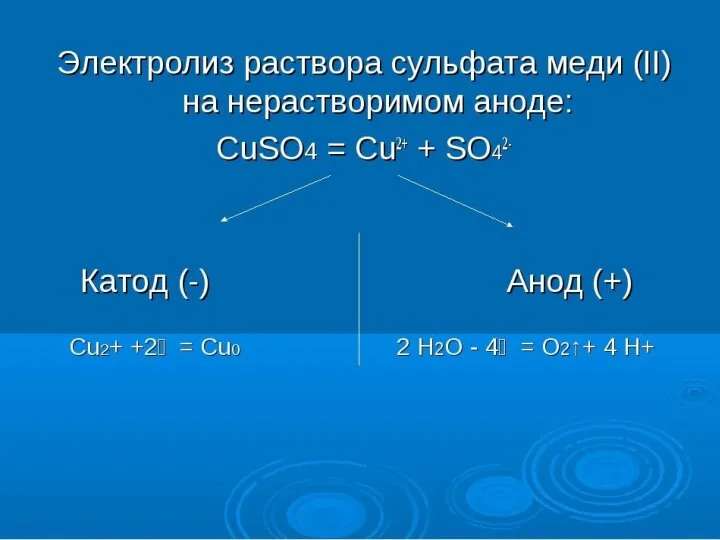
- 11. CuSO4 → Cu2+ + SO4²ˉ -К: Cu2+ + 2ē → Cuº +A: 2H2O – 4ē →
- 12. Na2CО3 → 2Na+ + CО3²ˉ -K: 2H2O + 2ē → H2º +2OH ˉ +А : 2H2O
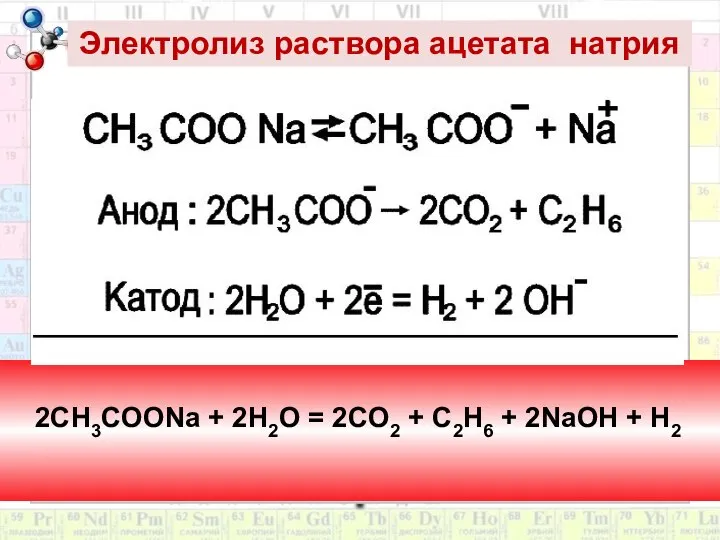
- 13. Электролиз раствора ацетата натрия
- 15. Опыт 1 Электролиз водного раствора йодида калия В U-образную трубку налить раствор йодида калия. В оба
- 17. Опыт 2 Электролиз водного раствора сульфата меди (II) с инертными электродами В U-образную трубку налить раствор
- 20. Опыт 3 Электролиз водного раствора сульфата меди (II) с активным медным анодом Поменять местами электроды (опыт
- 22. Опыт 4 Электролиз водного раствора сульфата натрия В U-образную трубку налить раствор сульфата натрия, опустить в
- 24. Скачать презентацию
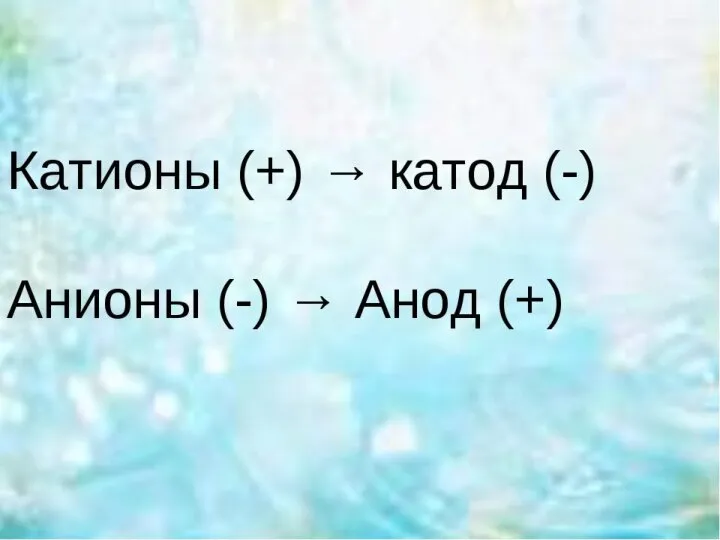














 Алкины. Строение, номенклатура, изометрия, физические свойства
Алкины. Строение, номенклатура, изометрия, физические свойства Электроотрицательность (ЭО)
Электроотрицательность (ЭО) Химическае препараты
Химическае препараты Туф вулканический
Туф вулканический 9_OSNOVY_KOLANALIZA
9_OSNOVY_KOLANALIZA получение Ме презентация
получение Ме презентация Ионообменные материалы для сорбции биологически активных веществ
Ионообменные материалы для сорбции биологически активных веществ Селективная экстракция отдельных групп БАВ сверхкритическими флюидами
Селективная экстракция отдельных групп БАВ сверхкритическими флюидами Обобщение. Неметаллы
Обобщение. Неметаллы Опыты по теме Свойства основных классов неорганических соединений
Опыты по теме Свойства основных классов неорганических соединений Процессы переработки нефти
Процессы переработки нефти Аналитические методы в современных исследованиях химии
Аналитические методы в современных исследованиях химии Расчеты по уравнениям химических реакций
Расчеты по уравнениям химических реакций Химия в нашей жизни
Химия в нашей жизни Соли
Соли Уравнения диссоциации
Уравнения диссоциации Сера. Физические и химические свойства. Нахождение в природе
Сера. Физические и химические свойства. Нахождение в природе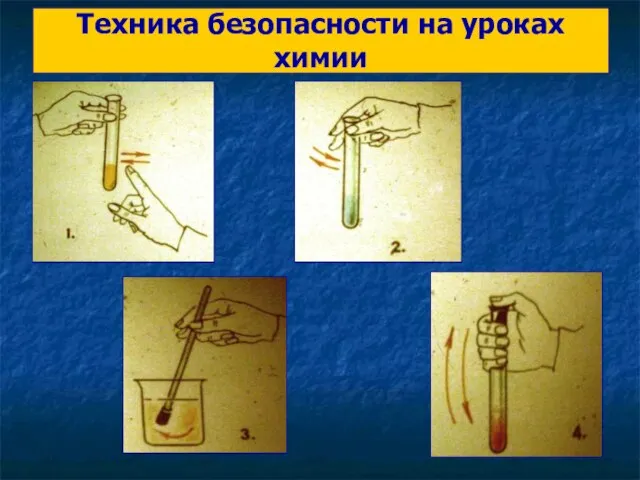 Техника безопасности на уроках химии
Техника безопасности на уроках химии История развития технологий термического крекинга в России и мире
История развития технологий термического крекинга в России и мире Пиримидин (шестичленный гетероцикл с двумя атомами азота)
Пиримидин (шестичленный гетероцикл с двумя атомами азота) Вещество и тело. Чистые вещества и смеси
Вещество и тело. Чистые вещества и смеси Минералы
Минералы Газовые смеси. Способы задания газовых смесей. Лекция 5
Газовые смеси. Способы задания газовых смесей. Лекция 5 способы разделения смесей
способы разделения смесей (+)-Plumisclerin A. Плюмисклин А
(+)-Plumisclerin A. Плюмисклин А Растворы полимеров
Растворы полимеров Получение бутандиола, как способ переработки природного газа
Получение бутандиола, как способ переработки природного газа Основной органический синтез
Основной органический синтез