Слайд 2ЦЕЛИ УРОКА:
ОЗНАКОМИТЬСЯ С О СТРОЕНИЕМ МОЛЕКУЛЫ ВОДЫ
РАССМОТРЕТЬ ФИЗИЧЕСКИЕ СВОЙСТВА ВОДЫ
РАССМОТРЕТЬ

ХИМИЧЕСКИЕ СВОЙСТВА ВОДЫ
Слайд 3СТРОЕНИЕ МОЛЕКУЛЫ ВОДЫ:
ФОРМУЛА - Н2О
2 атома водорода и 1 атом
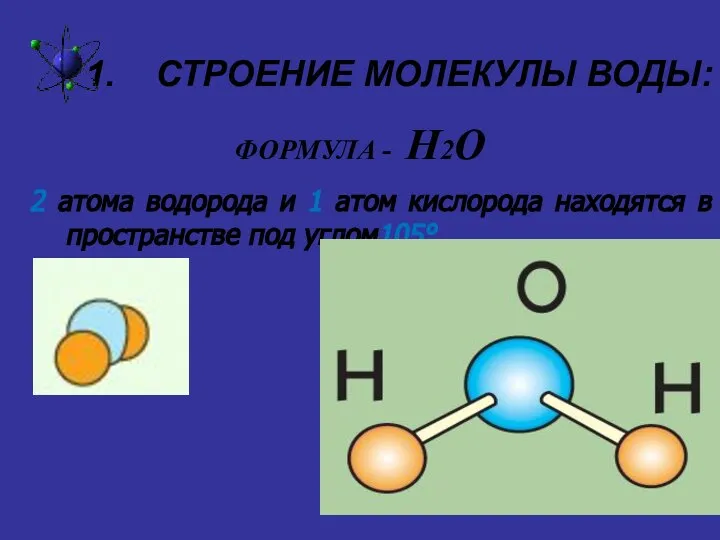
кислорода находятся в пространстве под углом105°
Слайд 52. ФИЗИЧЕСКИЕ СВОЙСТВА ВОДЫ:
ЖИДКОСТЬ - БЕЗ ЦВЕТА, ВКУСА И ЗАПАХА
СУЩЕСТВУЕТ В

ТРЕХ АГРЕГАТНЫХ СОСТОЯНИЯХ
КИПИТ ПРИ 100°С
ЗАМЕРЗАЕТ (ПЛАВИТСЯ) ПРИ 0°С
ПЛОТНОСТЬ 1 Г/МЛ
ОБЛАДАЕТ САМОЙ БОЛЬШОЙ ТЕПЛОЁМКОСТЬЮ
НЕ ПРОВОДИТ ЭЛЕКТРИЧЕСКИЙ ТОК
ПЛОТНОСТЬ ЛЬДА МЕНЬШЕ ПЛОТНОСТИ ВОДЫ
УНИВЕРСАЛЬНЫЙ РАСТВОРИТЕЛЬ
Слайд 73. ХИМИЧЕСКИЕ СВОЙСТВА ВОДЫ
1. ВЗАИМОДЕЙСТВИЕ С МЕТАЛЛАМИ:
а) очень активные металлы при взаимодействии
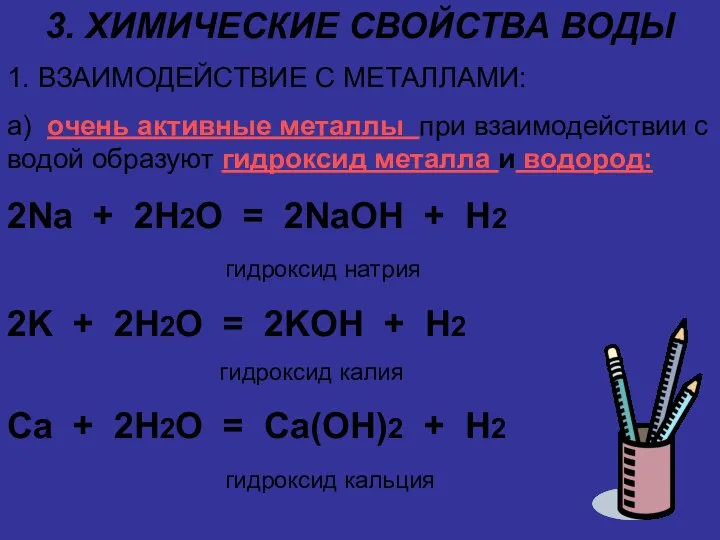
с водой образуют гидроксид металла и водород:
2Na + 2H2O = 2NaOH + H2
гидроксид натрия
2K + 2H2O = 2KOH + H2
гидроксид калия
Ca + 2H2O = Ca(OH)2 + H2
гидроксид кальция
Слайд 8Взаимодействие воды с кальцием

Слайд 9Вопрос:
Почему вода мутнеет от гидроксида кальция и не мутнеет от гидроксидов натрия,

калия и лития?
Слайд 10б) металлы средней активности взаимодействуют с водой при нагревании, образуя оксид металла

и водород:
Zn + H2O = ZnO + H2
оксид цинка
3Fe + 4H2O = Fe3O4 + 4H2
железная окалина
в) малоактивные металлы с водой
не реагируют:
Cu + H2O =
Слайд 112. ВЗАИМОДЕЙСТВИЕ ВОДЫ С ОКСИДАМИ:
а) оксиды активных металлов при взаимодействии с водой

образуют гидроксиды:
CaO + H2O = Ca(OH)2
гидроксид кальция
K2O + H2O = 2 KOH
гидроксид калия
Слайд 12Взаимодействие оксида серы (IV) с водой

Слайд 13б) оксиды неметаллов при взаимодействии с водой образуют кислоты:
SO2 + H2O

= H2SO3
cернистая кислота
SO3 + H2O = H2SO4
серная кислота
Слайд 14P2O5 + 3H2O = 2H3PO4
ортофосфорная кислота

Слайд 153. Разложение воды под действием электрического тока (электролиз):
2H2O = 2H2 ↑ +

O2 ↑
Слайд 17Рефлексия:
Я узнал, что…
Я научился…
Я понял…


















 Типы кристаллических решеток
Типы кристаллических решеток Судын оксидтермен реакциясы
Судын оксидтермен реакциясы Ионная химическая связь
Ионная химическая связь Классы неорганических соединений
Классы неорганических соединений Истина - дочь времени, а не авторитета
Истина - дочь времени, а не авторитета Презентация на тему Виды кристаллических решеток
Презентация на тему Виды кристаллических решеток 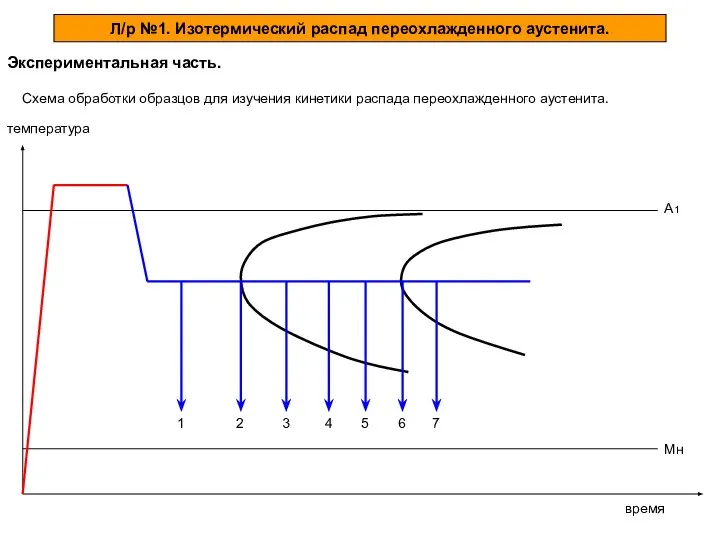 Изотермический распад переохлажденного аустенита. Экспериментальная часть
Изотермический распад переохлажденного аустенита. Экспериментальная часть Содержание варианта ЕГЭ
Содержание варианта ЕГЭ 11_.21
11_.21 Использование комплексно-ориентированных заданий на уроках
Использование комплексно-ориентированных заданий на уроках Окислительно-восстановительные реакции (ОВР)
Окислительно-восстановительные реакции (ОВР) Реакции окисления-восстановления в химическом анализе. (Лекция 7.2)
Реакции окисления-восстановления в химическом анализе. (Лекция 7.2) Алканы
Алканы Химия и автомобиль
Химия и автомобиль Общая характеристика элементов подгруппы углерода. Углерод – его строение и свойства
Общая характеристика элементов подгруппы углерода. Углерод – его строение и свойства Природный каучук
Природный каучук Классификация оксидов
Классификация оксидов Химические реакции
Химические реакции Образование и получение веществ. 6 класс
Образование и получение веществ. 6 класс Металлы
Металлы Закон сохранения массы веществ. Уравнения химических реакций.
Закон сохранения массы веществ. Уравнения химических реакций. Сравнительная характеристика стиральных порошков
Сравнительная характеристика стиральных порошков Валентность. Определение валентности по формулам
Валентность. Определение валентности по формулам Кроссворд. Плотность
Кроссворд. Плотность Алкены
Алкены Коррозия металлов
Коррозия металлов Вещества с атомной кристаллической решеткой
Вещества с атомной кристаллической решеткой Cкорость химических реакций
Cкорость химических реакций