Содержание
- 2. Обратимые и необратимые реакции. Обратимые химические реакции – это реакции, одновременно протекающие в прямом и обратном
- 3. Признаки необратимости. CuCl2 + 2KOH=Cu(OH)2↓ +2KOH – выпал осадок Na2CO3 + 2HCl=2NaCl + H2O + CO2↑
- 4. Химическое равновесие. H2 + I2 ↔ 2HI Вернемся к обратимой реакции водорода с парами йода. В
- 5. Константа химического равновесия. H2 + I2 ↔ 2HI Состояние химического равновесия характеризуется особой величиной – константой
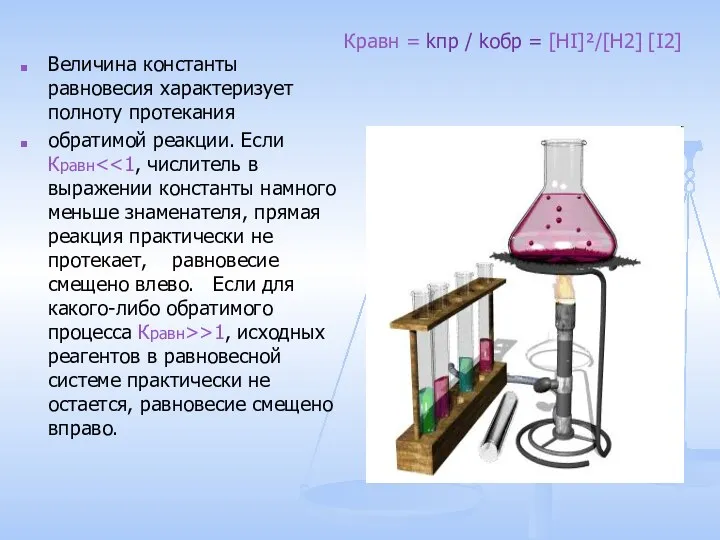
- 6. Величина константы равновесия характеризует полноту протекания обратимой реакции. Если Кравн >1, исходных реагентов в равновесной системе
- 7. Факторы, вызывающие смещение химического равновесия. Состояние химического равновесия может сохраняться долго при неизменных внешних условиях: температуры,
- 8. Историческая справка. Французский ученый- химик, занимался исследованиями процессов протекания химических реакций. Принцип смещения равновесий- самое известное,
- 9. Принцип Ле Шателье. Известен всюду на Земле Анри Луи Де Шателье. Он не был королем и
- 10. Изменение концентрации: 3H2 + N2 ↔ 2NH3 А) если увеличиваем концентрацию конечных продуктов, рав- новесие смещается
- 11. Изменение давления А) при увеличения давления равновесие смещается в сторону той реакции, при которой объем образовавшихся
- 12. Изменение температуры А) при повышении температуры химическое равновесие смещается в сторону эндотермической реакции. Б) при понижении
- 13. Значение принципа Ле Шателье.
- 14. Закрепление. Химик толкает реакцию в спину: «Давай-ка тебя я немного подвину!» Она отвечает: «Ты знаешь меня:
- 15. ВОПРОС 1( все вопросы письменно) При повышении температуры равновесие системы смещается в какую сторону 2SO3 2SO2
- 16. ВОПРОС 2. Каким образом можно сместить равновесие реакции в сторону исходных веществ (все в-ва – газы):
- 17. ВОПРОС 3. При повышении давления равновесие реакции смещается в какую сторону 2SO3 2SO2 + O2 -
- 18. ВОПРОС 4. Каким образом можно сместить равновесие в сторону продуктов реакции SO2 + 2H2S 3S +
- 19. ВОПРОС 5. При уменьшении концентрации SO2 равновесие реакции смещается H2SO3 SO2 + H2O -Q
- 20. ВОПРОС 6. При повышении температуры равновесие реакции сместится 2ZnS + O2 2ZnO + H2O + Q
- 21. Задача 1. Как надо изменить концентрации веществ, давление и температуру гомогенной системы PCl5 ↔ PCl3 +
- 22. ВОПРОС 7. В какой системе увеличение давления приведет к смещению химического равновесия в сторону прямой реакции?
- 23. Задача 2. Как сместиться химическое равновесие реакции 2СО + О2 ↔ 2СО2 + Q при а)
- 24. ВОПРОС 8. В какой системе увеличение давления приведет к смещению химического равновесия в сторону прямой реакции?
- 25. ВОПРОС 9. В какой системе увеличение давления приведет к смещению химического равновесия в сторону прямой реакции?
- 26. Задания на пятерку . 1. Условие необратимости химического превращения. а) образование слабого электролита б) поглощение большого
- 28. Скачать презентацию
























 Prezentatsia_Microsoft_PowerPoint
Prezentatsia_Microsoft_PowerPoint Карбоновые кислоты
Карбоновые кислоты Скорость химической реакции
Скорость химической реакции Межкристаллитная коррозия МКК
Межкристаллитная коррозия МКК Стерилизация технологических потоков и оборудования
Стерилизация технологических потоков и оборудования Научно-познавательное шоу Юный химик
Научно-познавательное шоу Юный химик Алканы
Алканы Основные классы неорганических соединений. Гидроксиды
Основные классы неорганических соединений. Гидроксиды Аспирин и его влияние на организм человека
Аспирин и его влияние на организм человека Алканы
Алканы Альдегиды. Строение молекул
Альдегиды. Строение молекул Техника безопасности при использовании различных видов топлива. Практическая работа № 3
Техника безопасности при использовании различных видов топлива. Практическая работа № 3 Сахароза (С12Н22О11)
Сахароза (С12Н22О11) Алюминий
Алюминий Презентация на тему Экологические риски при добыче и переработке нефти
Презентация на тему Экологические риски при добыче и переработке нефти  Дополнительный_материал_09.14_19.10.2022_b0aaa559
Дополнительный_материал_09.14_19.10.2022_b0aaa559 98675992
98675992 Классификация спиртов. Изомерия спиртов
Классификация спиртов. Изомерия спиртов Ионные уравнения реакций
Ионные уравнения реакций Презентация на тему Вопросы от …
Презентация на тему Вопросы от …  Классификация и номенклатура аминов. 11 класс
Классификация и номенклатура аминов. 11 класс Презентация на тему Оксиды
Презентация на тему Оксиды  06_Типы_химических_реакций_в_органической_химии
06_Типы_химических_реакций_в_органической_химии Гибридизация АО. Пространственное строение молекул (геометрия молекул)
Гибридизация АО. Пространственное строение молекул (геометрия молекул) Ионы кальция, как важное звено в нейроцитотоксическом действии кадмия
Ионы кальция, как важное звено в нейроцитотоксическом действии кадмия Строение электронной оболочки атома часть 2
Строение электронной оболочки атома часть 2 Основные законы и понятия химии. Основные классы неорганических соединений. Химический эквивалент. Закон эквивалентов
Основные законы и понятия химии. Основные классы неорганических соединений. Химический эквивалент. Закон эквивалентов Окислительновосстановительные процессы
Окислительновосстановительные процессы