Содержание
- 2. Соотнесите формулу и название: 1. H2 2. Fe2(SO4)3 3. HCl 4. H+ 5. Al3+ 6. FeSO4
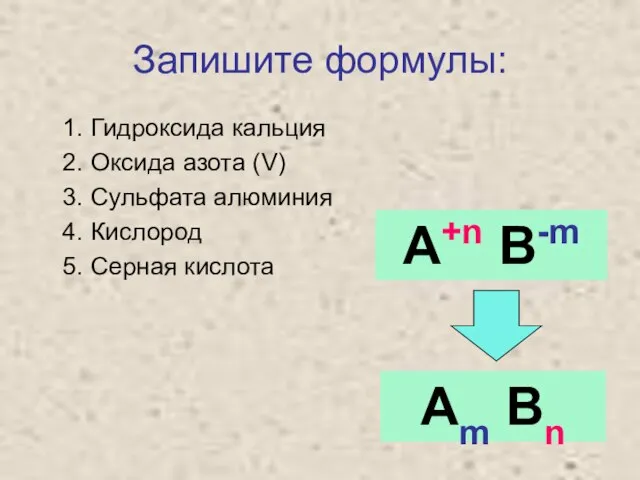
- 3. Запишите формулы: Гидроксида кальция Оксида азота (V) Сульфата алюминия Кислород Серная кислота А+n B-m Аm Bn
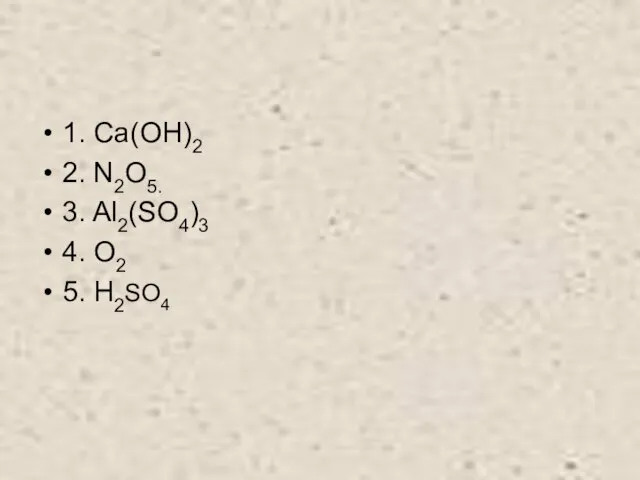
- 4. 1. Сa(OH)2 2. N2O5. 3. Al2(SO4)3 4. O2 5. H2SO4
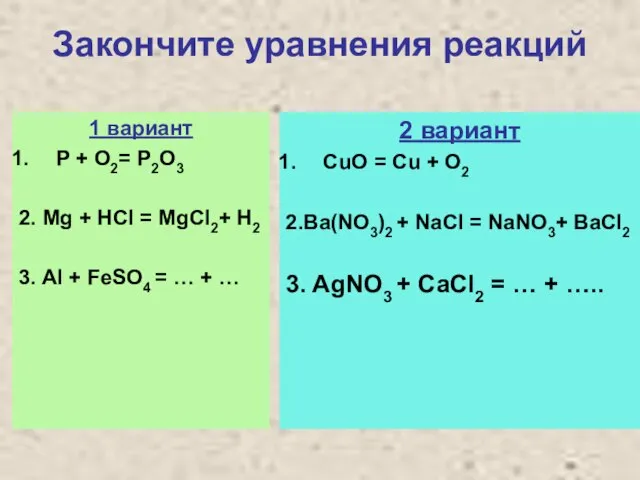
- 5. Закончите уравнения реакций 1 вариант P + O2= P2O3 2. Mg + HCl = MgCl2+ H2
- 6. Проверьте: 1 вариант 4P + 3O2= 2P2O3 Mg + 2HCl = MgCl2+ H2 2Al + 3FeSO4
- 7. Решение задач по уравнениям реакций Определите массу цинка, необходимого для взаимодействия с 73г соляной кислоты.
- 8. Алгоритм решения 1. Записать уравнение реакции 2. Определить количество вещества с известными данными n = m:M
- 10. Скачать презентацию




 Предельные углеводороды. Урок №4
Предельные углеводороды. Урок №4 Взаимодействие частиц конденсированной фазы, их срастание (коалесценция). Лекция 3
Взаимодействие частиц конденсированной фазы, их срастание (коалесценция). Лекция 3 Аналитическая химия как наука. Лекция 1
Аналитическая химия как наука. Лекция 1 Sinteticheskie_Materialy_I_Ikh_Rol_1
Sinteticheskie_Materialy_I_Ikh_Rol_1 Схема монооксигеназной цепи микросом
Схема монооксигеназной цепи микросом Презентация на тему Химические средства гигиены и косметика
Презентация на тему Химические средства гигиены и косметика  Презентация на тему Природные источники углеводородов
Презентация на тему Природные источники углеводородов  Превращение веществ. История химии. Автор: Рассказова Н.Л., учитель химии и биологии МОУ «СОШ №8».
Превращение веществ. История химии. Автор: Рассказова Н.Л., учитель химии и биологии МОУ «СОШ №8». Анализ образца доломита методами аналитической химии
Анализ образца доломита методами аналитической химии Электролиз воды
Электролиз воды Презентация на тему Ионные уравнения реакций (8 класс)
Презентация на тему Ионные уравнения реакций (8 класс)  Презентация на тему по химии витамины
Презентация на тему по химии витамины  Диссоциация кислот, щелочей, солей
Диссоциация кислот, щелочей, солей Химическая реакция
Химическая реакция Производные кислородсодержащих гетероциклов - пиранов
Производные кислородсодержащих гетероциклов - пиранов Химическое равновесие в растворах электролитов
Химическое равновесие в растворах электролитов Синтез и свойства кукурбитурилов
Синтез и свойства кукурбитурилов Подгруппа алюминия
Подгруппа алюминия Биологическое значение брома и йода
Биологическое значение брома и йода Полимеры. Функции полимеров
Полимеры. Функции полимеров Постулаты Онзагера
Постулаты Онзагера Карбоновые кислоты
Карбоновые кислоты Аномальные свойства воды
Аномальные свойства воды Выделение и модификация древесных полимеров с получением биоактивных полимеров и матриц
Выделение и модификация древесных полимеров с получением биоактивных полимеров и матриц Вода - самое удивительное вещество в природе. (8 класс)
Вода - самое удивительное вещество в природе. (8 класс) Характеристика химического элемента на основании его положения в Периодической системе Д. И. Менделеева
Характеристика химического элемента на основании его положения в Периодической системе Д. И. Менделеева Классификация реагентов и реакций в органической химии. (Лекция 4)
Классификация реагентов и реакций в органической химии. (Лекция 4) Нефть. Состав, свойства, переработка
Нефть. Состав, свойства, переработка