Содержание
- 2. Как же химики судят о том, является ли данное вещество кислотой? Растворы всех кислот на вкус
- 3. 1)Что такое индикаторы? 2)Какие индикаторы вы знаете? 3) Как индикаторы меняют цвет в щелочной среде?
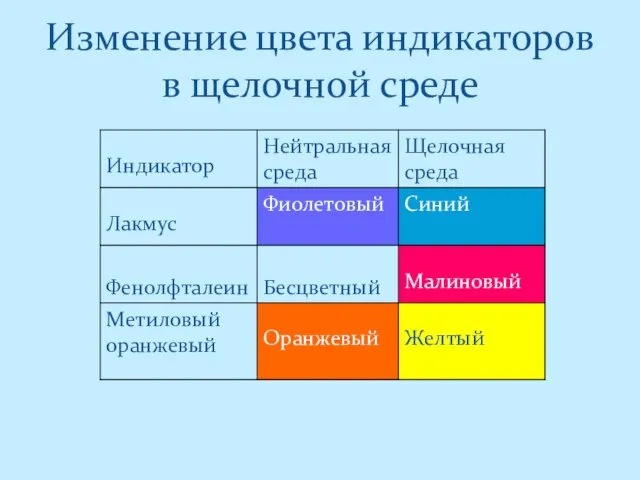
- 4. Изменение цвета индикаторов в щелочной среде
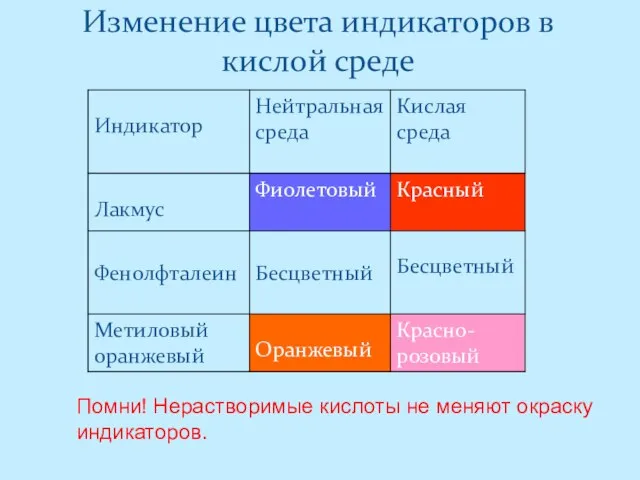
- 5. Изменение цвета индикаторов в кислой среде Помни! Нерастворимые кислоты не меняют окраску индикаторов.
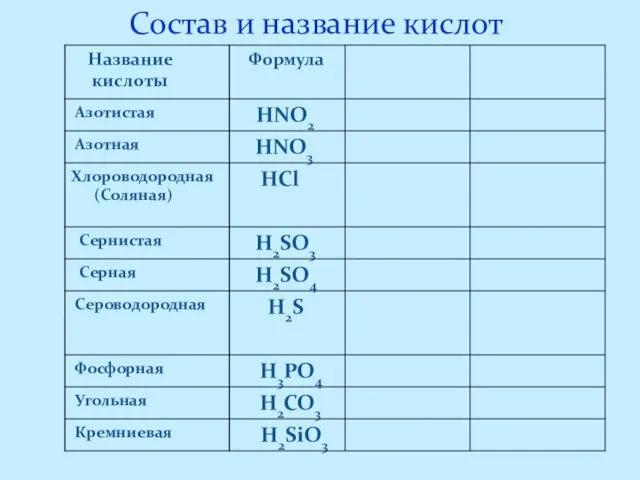
- 6. Состав и название кислот
- 7. Кислоты – это сложные вещества, молекулы, которых состоят из атомов водорода и кислотных остатков
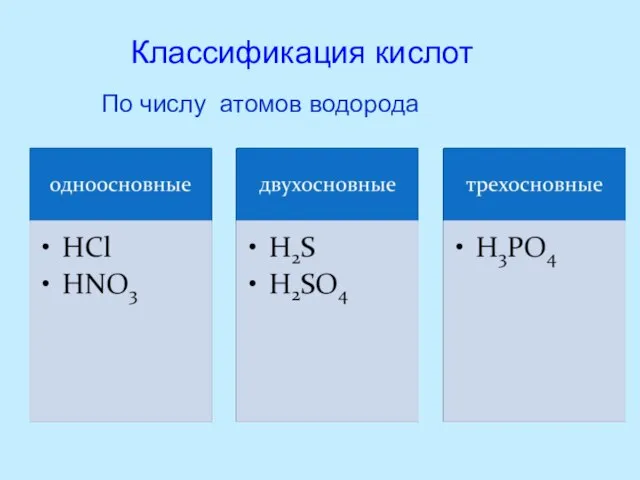
- 8. По числу атомов водорода Классификация кислот
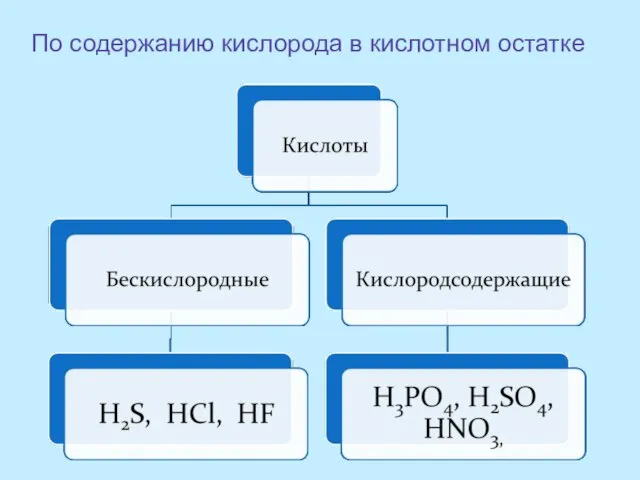
- 9. По содержанию кислорода в кислотном остатке
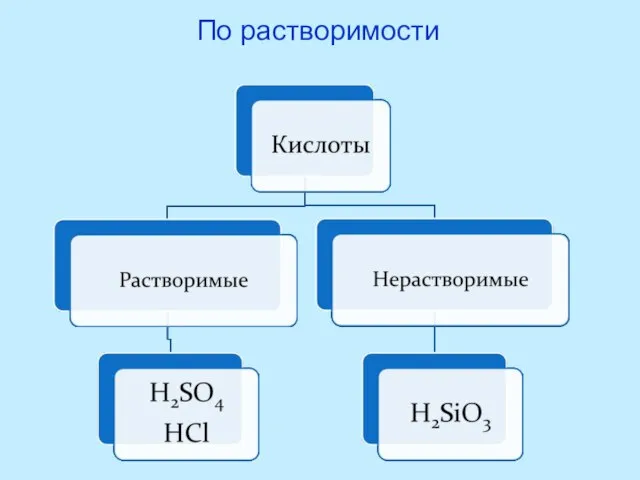
- 10. По растворимости
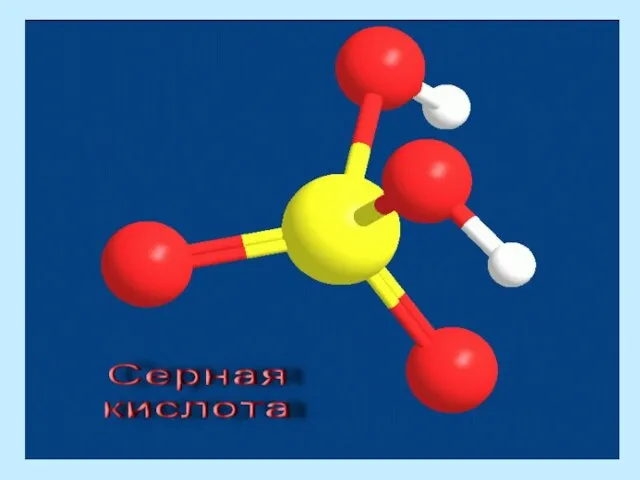
- 13. Серная кислота бесцветная , вязкая жидкость, без запаха, вдвое тяжелее воды, поглощает влагу из воздуха и
- 14. Обугливание лучинки серной кислотой
- 15. Обугливание сахара серной кислотой
- 16. Обугливание бумаги серной кислотой
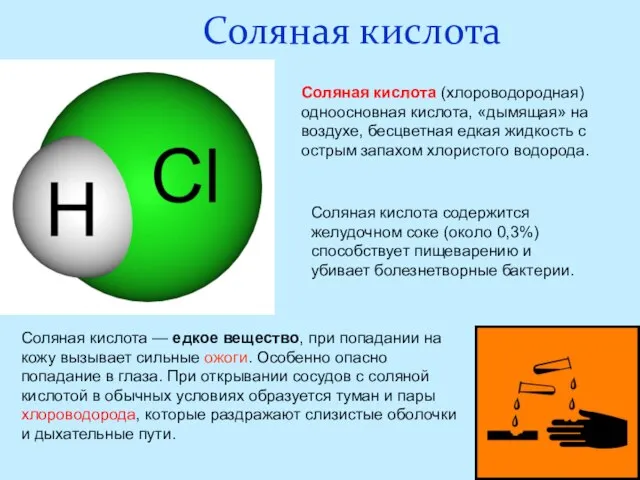
- 17. Соляная кислота Соляная кислота содержится желудочном соке (около 0,3%) способствует пищеварению и убивает болезнетворные бактерии. Соляная
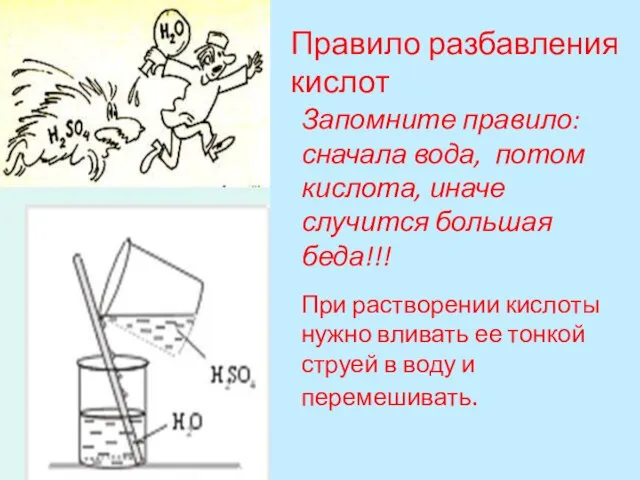
- 18. Правило разбавления кислот При растворении кислоты нужно вливать ее тонкой струей в воду и перемешивать. Запомните
- 20. ЕСЛИ КИСЛОТА ПОПАЛА НА КОЖУ. Пораженный участок кожи промывают сильно скользящей струей холодной воды в течение
- 21. H2CO3 → CO2↑ + H2O H2SO3 → SO2↑ + H2O В свободном виде не существуют. Они
- 22. Как узнать какие оксиды соответствуют данным кислотам? Помните, что суммарная степень окисления атомов всех элементов в
- 23. Проверь себя Выберите группу веществ, в состав которой входят только кислоты HCl, SO3, NaOH,CuCl2 HNO3, H2S,
- 24. Проверь себя Выберите группу веществ, в состав которой входят только двухосновные кислоты HNO3, H2S, HCl, H3PO4
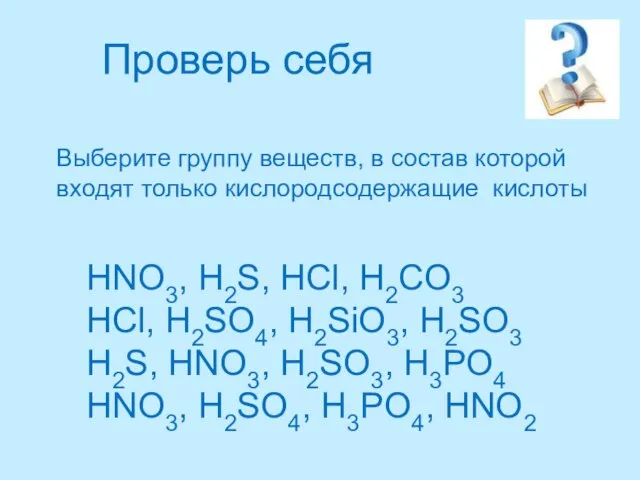
- 25. HNO3, H2S, HCl, H2CO3 HCl, H2SO4, H2SiO3, H2SO3 H2S, HNO3, H2SO3, H3PO4 HNO3, H2SO4, H3PO4, HNO2
- 26. Проверь себя В кислой среде синий лакмус становится: фиолетовым красным малиновым не изменяет окраску
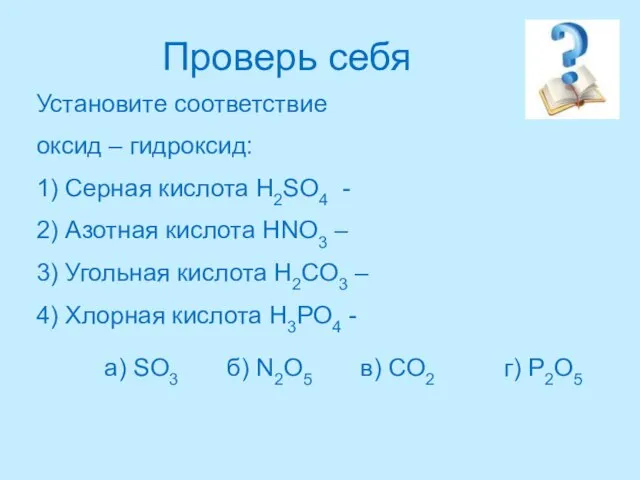
- 27. Проверь себя Установите соответствие оксид – гидроксид: 1) Серная кислота H2SO4 - 2) Азотная кислота HNO3
- 28. Вспомните правило разбавления кислот
- 30. Скачать презентацию















 Типы кристаллических решеток
Типы кристаллических решеток Судын оксидтермен реакциясы
Судын оксидтермен реакциясы Ионная химическая связь
Ионная химическая связь Классы неорганических соединений
Классы неорганических соединений Истина - дочь времени, а не авторитета
Истина - дочь времени, а не авторитета Презентация на тему Виды кристаллических решеток
Презентация на тему Виды кристаллических решеток 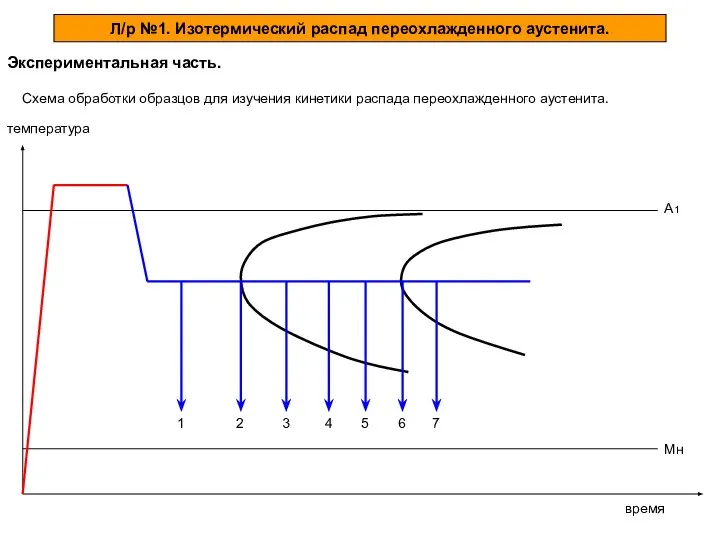 Изотермический распад переохлажденного аустенита. Экспериментальная часть
Изотермический распад переохлажденного аустенита. Экспериментальная часть Содержание варианта ЕГЭ
Содержание варианта ЕГЭ 11_.21
11_.21 Использование комплексно-ориентированных заданий на уроках
Использование комплексно-ориентированных заданий на уроках Окислительно-восстановительные реакции (ОВР)
Окислительно-восстановительные реакции (ОВР) Реакции окисления-восстановления в химическом анализе. (Лекция 7.2)
Реакции окисления-восстановления в химическом анализе. (Лекция 7.2) Алканы
Алканы Химия и автомобиль
Химия и автомобиль Общая характеристика элементов подгруппы углерода. Углерод – его строение и свойства
Общая характеристика элементов подгруппы углерода. Углерод – его строение и свойства Природный каучук
Природный каучук Классификация оксидов
Классификация оксидов Химические реакции
Химические реакции Образование и получение веществ. 6 класс
Образование и получение веществ. 6 класс Металлы
Металлы Закон сохранения массы веществ. Уравнения химических реакций.
Закон сохранения массы веществ. Уравнения химических реакций. Сравнительная характеристика стиральных порошков
Сравнительная характеристика стиральных порошков Валентность. Определение валентности по формулам
Валентность. Определение валентности по формулам Кроссворд. Плотность
Кроссворд. Плотность Алкены
Алкены Коррозия металлов
Коррозия металлов Вещества с атомной кристаллической решеткой
Вещества с атомной кристаллической решеткой Cкорость химических реакций
Cкорость химических реакций