Слайд 11 В мире ежегодно огромное количество различных металлов и сплавов, и примерно

10% этого количества разрушаются в результате коррозии. А из всего количества сплавов на основе железа теряется примерно 25%. Ржавеет только железо, а остальные металлы – корродируют.
Что же это за процесс – коррозия?
Коррозия (от латинского corrodere – «разъедать»)- самопроизвольное разрушение металлов и сплавов под влиянием окружающей среды.
Слайд 12Коррозию вызывают:
Вода
Кислород
Оксиды углерода и серы
Водные растворы солей (морская вода, грунтовые воды)

Слайд 13Виды коррозии.
1/Химическая – это разрушение металлов в результате их химического взаимодействия

с веществами окружающей среды.
Слайд 14Zn + 2HCl = ZnCl2 + H2
2K + 2H2O = 2KOH +
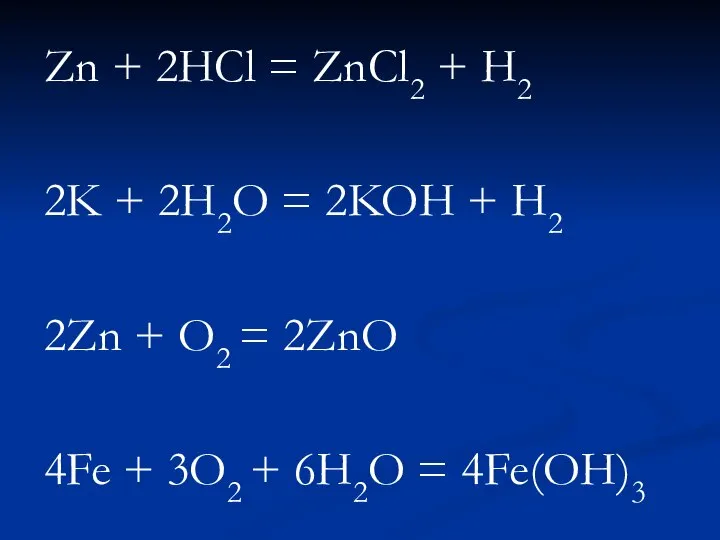
H2
2Zn + O2 = 2ZnO
4Fe + 3O2 + 6H2O = 4Fe(OH)3
Слайд 15 2/Электрохимическая – это разрушение металлов, которое сопровождается возникновением электрического тока. Наряду

с химическими процессами протекают электрические.
Слайд 16Fe – Cu
Анод: Fe0 – 2е- → Fe2+
Катод: 2H++2e- → H2↑
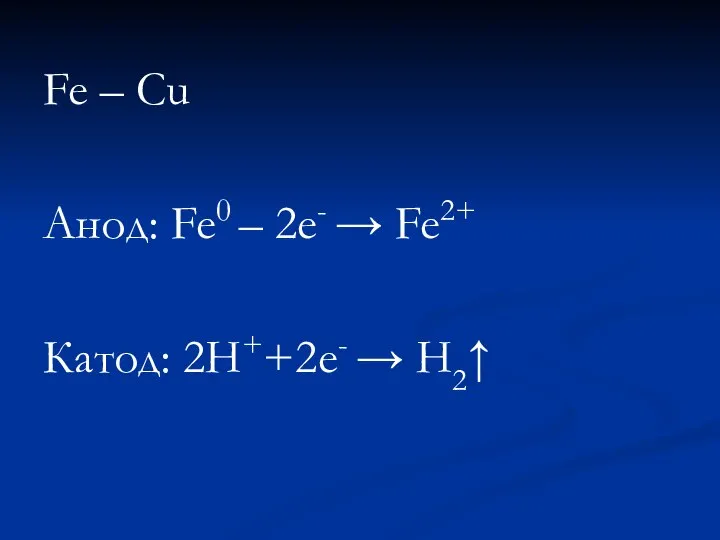
Слайд 18Закрепление
1. В подвале дома обнаружили ящик с гвоздями, но от неправильных условий

хранения многие из них были покрыты ржавчиной.
Что представляет собой ржавчина с химической точки зрения?
Каким простым способом можно удалить ржавчину?
Слайд 192. Молодая хозяйка повесила сушить бельё на железную проволоку, натянутую между стойками.

Когда бельё высохло, она с ужасом обнаружила на чистом белье желтые полосы.
Как объяснить появление полос на белье?
Как можно избавиться от этих пятен?
Слайд 203. В домашней мастерской всегда много инструментов, запчастей и материалов, которые в

основном изготовлены из металлов и их сплавов. Но вот беда – при хранении металлические изделия подвергаются коррозии.
Укажите условия хранения металлических изделий, которые продлят срок их службы.
Слайд 214. Соляная кислота с добавкой ингибитора нашла применение для очистки паровых котлов

от отложении накипи и удаления с поверхности металлов ржавчины и окалины.
Почему?












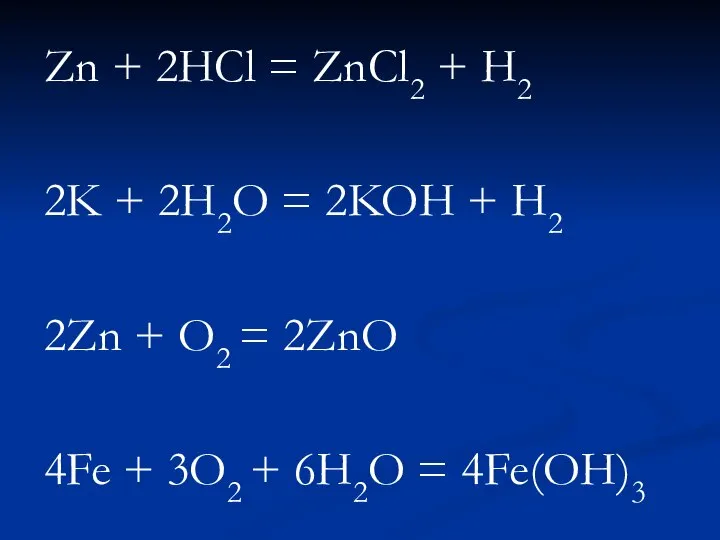

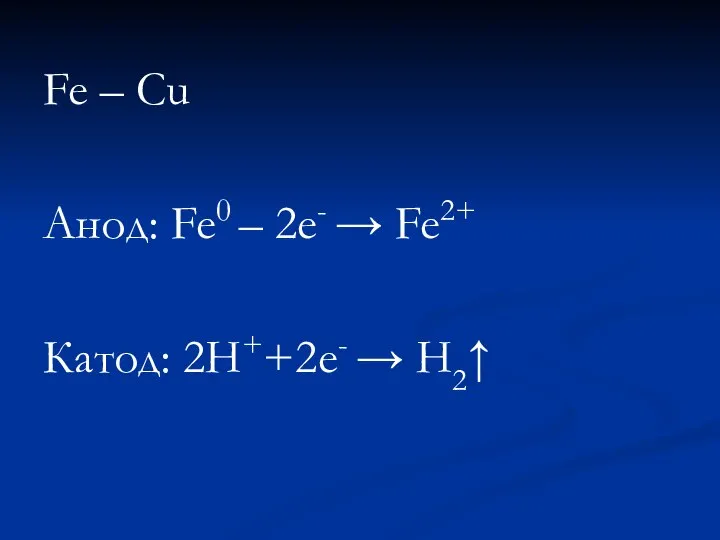





 Ароматические углеводороды
Ароматические углеводороды Простое вещество и химический элемент азот
Простое вещество и химический элемент азот Циклические эфиры (окиси)
Циклические эфиры (окиси) Смеси веществ
Смеси веществ Моноенаминирование 4-пиронов и 4-метилен-4н-пиранов
Моноенаминирование 4-пиронов и 4-метилен-4н-пиранов Диффузия в металлах и сплавах
Диффузия в металлах и сплавах Презентация на тему Физические и химические явления 8 класс
Презентация на тему Физические и химические явления 8 класс  Электролитическая диссоциация
Электролитическая диссоциация Аналитическая химия (ЛЕКЦИЯ 1)
Аналитическая химия (ЛЕКЦИЯ 1) Получение и химические свойства металлов
Получение и химические свойства металлов Презентация на тему Альдегиды, свойства, получение, применение
Презентация на тему Альдегиды, свойства, получение, применение  Кислоты. Кислоты в животном мире
Кислоты. Кислоты в животном мире Составление химических уравнений
Составление химических уравнений Биологическое значение брома и йода
Биологическое значение брома и йода Многообразие веществ
Многообразие веществ Презентация на тему Процессы в растворах электролитическая диссоциация
Презентация на тему Процессы в растворах электролитическая диссоциация  Олигосахариды и полисахариды
Олигосахариды и полисахариды Основания. Классификация. Химические и физические свойства
Основания. Классификация. Химические и физические свойства Железо и его соединения
Железо и его соединения агрегатные состояния вещества 7 класс
агрегатные состояния вещества 7 класс Узагальнення знань з теми Вуглеводні
Узагальнення знань з теми Вуглеводні Научно-исследовательская деятельность учащихся в процессе изучения химии
Научно-исследовательская деятельность учащихся в процессе изучения химии Приобретённые: недостаточность митохондрий,
Приобретённые: недостаточность митохондрий, Стекло. Виды стекла
Стекло. Виды стекла ТЕМА: БОЛЬШОЙ КРУГОВОРОТ ВЕЩЕСТВ
ТЕМА: БОЛЬШОЙ КРУГОВОРОТ ВЕЩЕСТВ Силикатная промышленность: Вчера, сегодня, завтра
Силикатная промышленность: Вчера, сегодня, завтра Органическая химия. Теория строения органических веществ
Органическая химия. Теория строения органических веществ Общая характеристика металлов
Общая характеристика металлов