Содержание
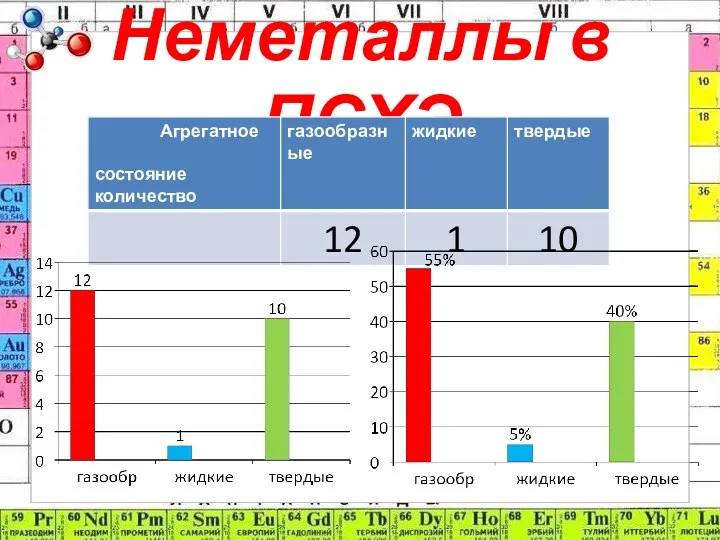
- 2. Неметаллы в ПСХЭ
- 4. Объемная доля компонента в газовой смеси Знать: формулу для расчета объемной доли газа в смеси; Уметь:
- 6. Задача 1 Сосуд заполнили 25 мл кислорода и 125 мл азота . Вычислите объемные доли кислорода
- 7. Задача 2 Анализ атмосферы Венеры показал, что в 50 мл венерианского «воздуха» содержится 48,5 мл углекислого
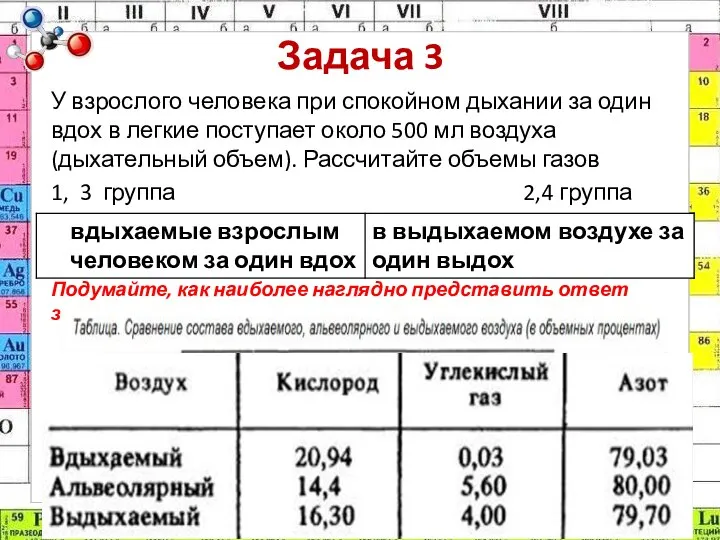
- 10. Задача 3 У взрослого человека при спокойном дыхании за один вдох в легкие поступает около 500
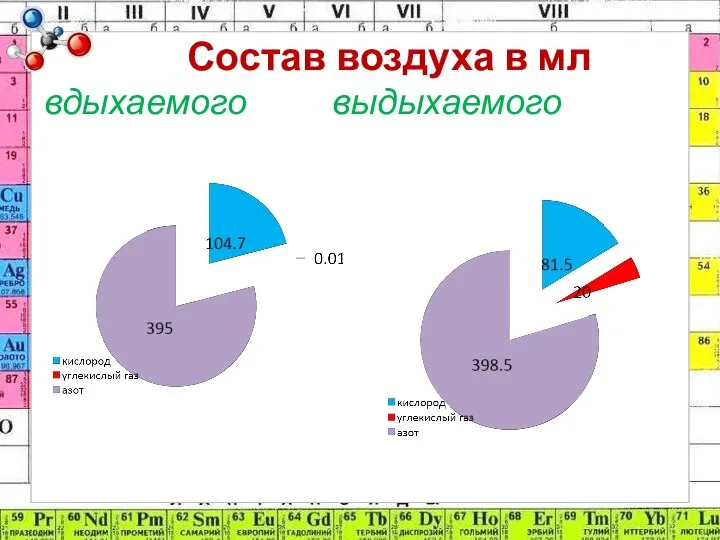
- 11. Состав воздуха в мл вдыхаемого выдыхаемого
- 12. Задача 4 1 баллон содержит 40 л кислорода. Какой объём воздуха необходимо затратить на его производство?
- 13. Задача 5 Человек начинает ощущать едкий запах сернистого газа (SO2), если в 1000 л воздуха содержится
- 14. Дано V(возд.)=1000л m (SO2) = 3,0 мг ρ (SO2)=2,86 г/л ? (SO2)=?
- 15. Задача 6 При сгорании одной сигареты образуется 16,8 мг угарного газа. 20% этого газа остается в
- 18. Водолазы дышат кислородно-гелевой смесью. Если содержание кислорода во вдыхаемом воздухе при нормальном давлении меньше 18%, то
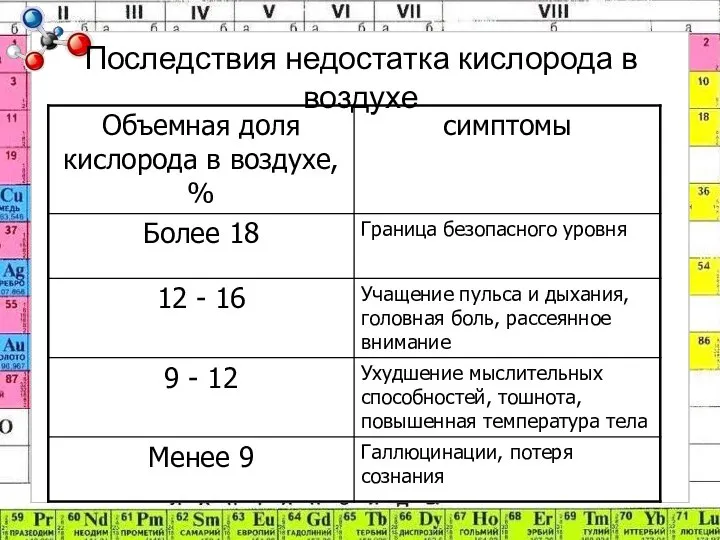
- 19. Последствия недостатка кислорода в воздухе
- 21. Скачать презентацию














 Химический состав живых организмов. Метаболизм
Химический состав живых организмов. Метаболизм Учебная дисциплина Естествознание. Раздел II. Химия
Учебная дисциплина Естествознание. Раздел II. Химия Классификация органических соединений
Классификация органических соединений Химия в быту
Химия в быту Вода. Классы неорганических соединений. 8 класс
Вода. Классы неорганических соединений. 8 класс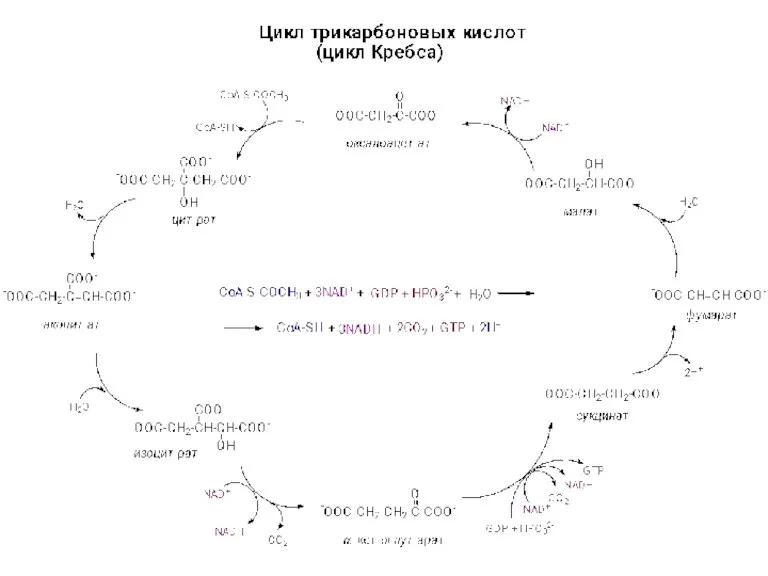 Цикл трикарбоновых кислот
Цикл трикарбоновых кислот Спирты, карбоновые кислоты
Спирты, карбоновые кислоты Вода И её значение
Вода И её значение Министерство сельского хозяйства Российской Федерации. Поляграфия и фотоэлектронная спектроскопия
Министерство сельского хозяйства Российской Федерации. Поляграфия и фотоэлектронная спектроскопия Презентация на тему Химический состав клетки. Неорганические соединения
Презентация на тему Химический состав клетки. Неорганические соединения  Подготовка выпускников к ГИА по химии: опыт, проблемы, перспективы
Подготовка выпускников к ГИА по химии: опыт, проблемы, перспективы Растворы. Квалификации химических веществ:
Растворы. Квалификации химических веществ: Металлические и неметаллические материалы. Типы и характеристики кристаллических решеток
Металлические и неметаллические материалы. Типы и характеристики кристаллических решеток Презентация на тему Полимеразная цепная реакция (ПЦР)
Презентация на тему Полимеразная цепная реакция (ПЦР)  Химический элемент кислород
Химический элемент кислород Химическая кинетика
Химическая кинетика Преобразование уравнения Нернста. Коэффициент Кда. Причины различия в значениях Кда для различных пород
Преобразование уравнения Нернста. Коэффициент Кда. Причины различия в значениях Кда для различных пород минералы_5_спайность
минералы_5_спайность Азотсодержащие органические соединения
Азотсодержащие органические соединения Изучение основного солевого состава брендов бутилированной воды, присутствующих на рынке России
Изучение основного солевого состава брендов бутилированной воды, присутствующих на рынке России Термодинамическое равновесие между фазами
Термодинамическое равновесие между фазами Алкены. Непредельные углеводороды
Алкены. Непредельные углеводороды Неньютоновская жидкость
Неньютоновская жидкость Неметаллы
Неметаллы Металлы. Тест с ответами
Металлы. Тест с ответами Презентация на тему Уголь
Презентация на тему Уголь  Опыт Пилатра де Розьера
Опыт Пилатра де Розьера В мире индикаторов
В мире индикаторов