Содержание
- 2. Расположите химические элементы в порядке увеличения атомного радиуса. 1) О, 2) Те, 3) Se, 4) S
- 3. Электроотрицательность химических элементов
- 4. Л. Полинг Электроотрицательность - это свойство атомов элемента оттягивать на себя электроны от атомов других элементов
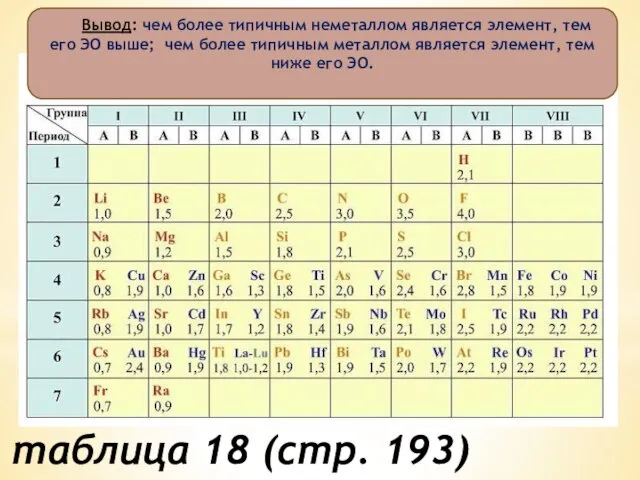
- 5. Вывод: чем более типичным неметаллом является элемент, тем его ЭО выше; чем более типичным металлом является
- 6. Расположите химические знаки перечисленных ниже элементов в порядке возрастания значений электроотрицательности: Магний, натрий, хлор, сера, кислород,
- 7. Химические элементы в порядке возрастания значений электроотрицательности : Mg -1,2 Na -0,9 Cl -3,0 S –
- 8. Не пользуясь таблицей электроотрицательностей, а только руководствуясь положением химических элементов в периодической таблице, расположите перечисленные элементы
- 9. С помощью знаков >или а) H Cl б) S O в) Na Cl г) Cu O
- 10. В приведенных ниже формулах подчеркните атомы наиболее ЭО химического элемента: СаСl2, К2O, N2, H2S, Al2O3
- 12. Скачать презентацию








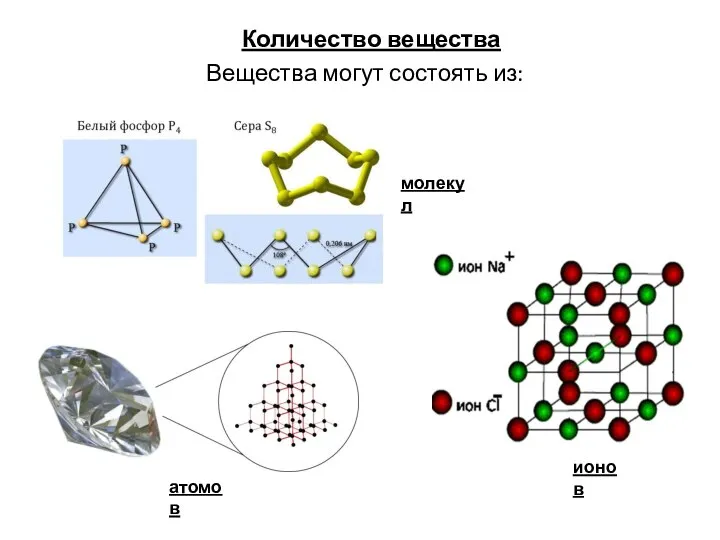 Количество вещества
Количество вещества Кислоты в химии
Кислоты в химии Алкадиены. Строение. свойства и применение
Алкадиены. Строение. свойства и применение Малотоннажные термопласты
Малотоннажные термопласты Органика из аптеки
Органика из аптеки Три секрета прочности волокнистых композитов
Три секрета прочности волокнистых композитов Определение качества дизельного топлива
Определение качества дизельного топлива Строение атома в ЭЖ (1)
Строение атома в ЭЖ (1) Основания, их классификация и свойства в свете теории электролитической диссоциации
Основания, их классификация и свойства в свете теории электролитической диссоциации Характеристика кислорода и серы
Характеристика кислорода и серы Химические реакции
Химические реакции Предельные одноосновные карбоновые кислоты. Сложные эфиры
Предельные одноосновные карбоновые кислоты. Сложные эфиры Количество вещества. Моль. Молярная масса
Количество вещества. Моль. Молярная масса Кислоты
Кислоты Классификация органических соединений
Классификация органических соединений Каскадный синтез пептидов
Каскадный синтез пептидов Халькогены. Электронное строение кислорода и серы
Халькогены. Электронное строение кислорода и серы Химия в быту
Химия в быту Презентация Повторение к СОЧ-10 кл (1)
Презентация Повторение к СОЧ-10 кл (1) Органическая химия. Подготовка к экзамену
Органическая химия. Подготовка к экзамену Алкины. Понятие об алкинах
Алкины. Понятие об алкинах Презентация на тему Производство стекла
Презентация на тему Производство стекла  Сeквенирование нуклеиновых кислот
Сeквенирование нуклеиновых кислот Химическое равновесие
Химическое равновесие Применение неметаллов
Применение неметаллов Тепловой эффект химических реакций
Тепловой эффект химических реакций Проект по химии. Минералы на нашей коже
Проект по химии. Минералы на нашей коже Основные классы неорганических соединений
Основные классы неорганических соединений