Содержание
- 3. На внешнем энергетическом уровне у большинства неметаллов (кроме водорода, гелия и бора) расположено от 4 до
- 4. Неметаллы в роли окислителей Неметаллы в роли восстановителей 2K + S = K2S 2Mg + O2
- 6. Неметаллы
- 7. Газообразные: H2, O2, F2, Cl2, N2, благородные газы Жидкие: Br2 Твёрдые: B, C, Si, P, S,
- 8. Для неметаллов характерно широкое разнообразие окрасок. Графит Бром Йод Хлор
- 9. -272 оС 3800 оС Температуры плавления неметаллов
- 10. Неметаллы способны образовывать два типа кристаллических решёток — молекулярные и атомные.
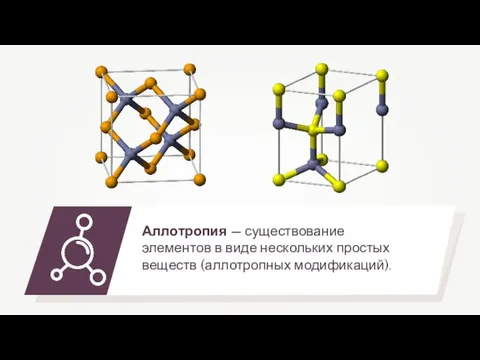
- 11. Аллотропия — существование элементов в виде нескольких простых веществ (аллотропных модификаций).
- 17. Воздух, свободный от переменных и случайных составных частей, прозрачен, лишен цвета, вкуса и запаха. При нормальных
- 19. Скачать презентацию
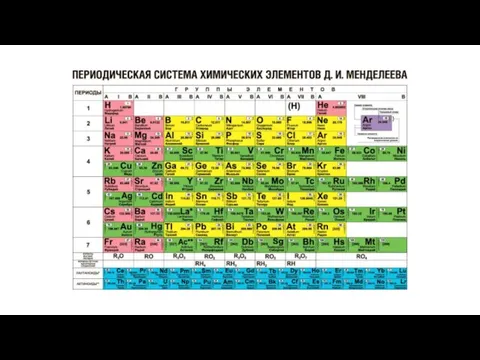


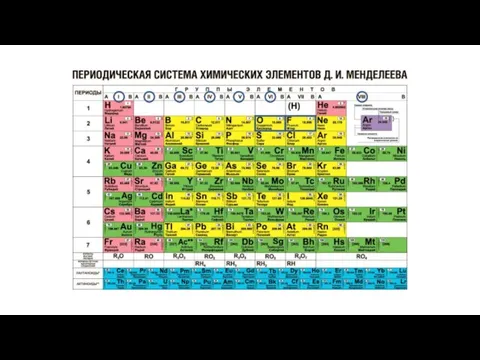




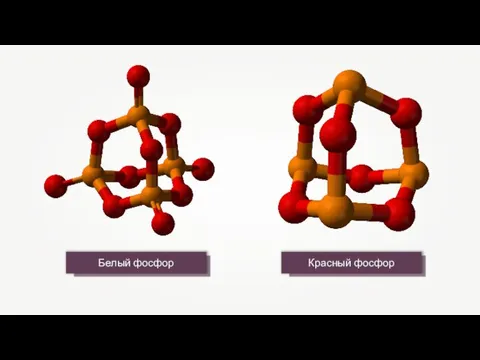





 Общая характеристика неметаллов
Общая характеристика неметаллов Изомерия. Классификация органических веществ.
Изомерия. Классификация органических веществ. Химия спирты одноатомные предельные
Химия спирты одноатомные предельные Композитные материалы
Композитные материалы Демокрит его вклад в развитие взглядов на строение вещества
Демокрит его вклад в развитие взглядов на строение вещества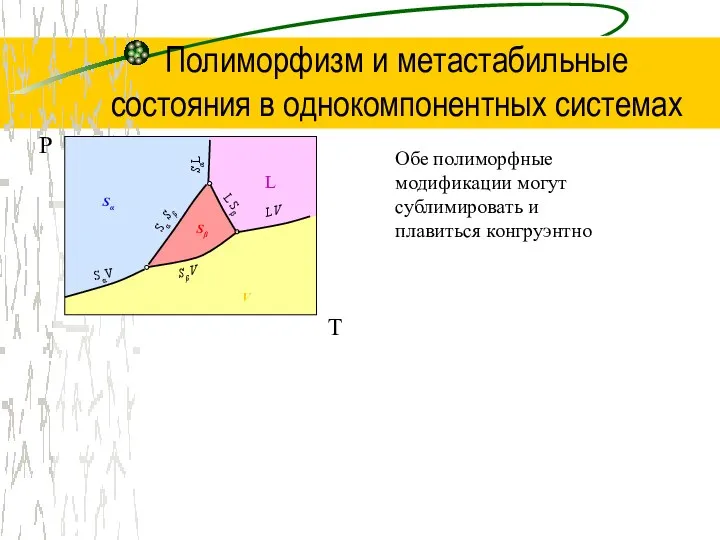 Полиморфизм и метастабильные состояния в однокомпонентных системах
Полиморфизм и метастабильные состояния в однокомпонентных системах Основи масообміну
Основи масообміну Количество вещества. Моль
Количество вещества. Моль Алюміній. Фізичні та хімічні властивості
Алюміній. Фізичні та хімічні властивості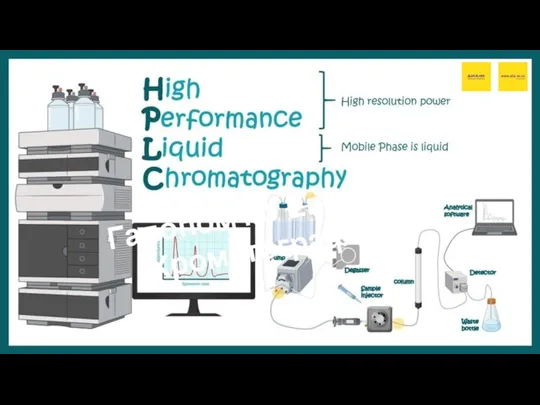 Хроматография
Хроматография Углеродистые конструкционные стали
Углеродистые конструкционные стали Жидкокристаллический эластомер как роторный актуатор
Жидкокристаллический эластомер как роторный актуатор Презентация на тему Игра по химии «Остров Периодическая Система»
Презентация на тему Игра по химии «Остров Периодическая Система»  Свойства растворов электролитов
Свойства растворов электролитов Производство аммиака
Производство аммиака Кислород. Общая характеристика, получение и свойства
Кислород. Общая характеристика, получение и свойства Презентация на тему Металлы
Презентация на тему Металлы  Количество вещества, число Авогадро, молярная масса, молярный объём, уравнение связи
Количество вещества, число Авогадро, молярная масса, молярный объём, уравнение связи Алкены
Алкены Презентация на тему Электронное и пространственное строение молекулы метана
Презентация на тему Электронное и пространственное строение молекулы метана  Циклоалканы. Физические свойства
Циклоалканы. Физические свойства Кислород
Кислород Синтетические органические соединения
Синтетические органические соединения Турнир Деда Мороза. Викторина по химии
Турнир Деда Мороза. Викторина по химии Презентация на тему Алмазы Индии
Презентация на тему Алмазы Индии  Алкены
Алкены Значимые личности в химии
Значимые личности в химии Стан електронів у атомі
Стан електронів у атомі