Содержание
- 2. «Железо не только основа всего мира, самый главный металл окружающей нас природы, оно – основа культуры
- 3. ЖЕЛЕЗО: ФИЗИЧЕСКИЕ И ХИМИЧЕСКИЕ СВОЙСТВА.
- 4. ОСОБЕННОСТИ СТРОЕНИЯ АТОМА ЖЕЛЕЗА Fe 26 2е 8е 14е 2е 1s22s22р63s23р63d64s2 возможные степени окисления: +2 и
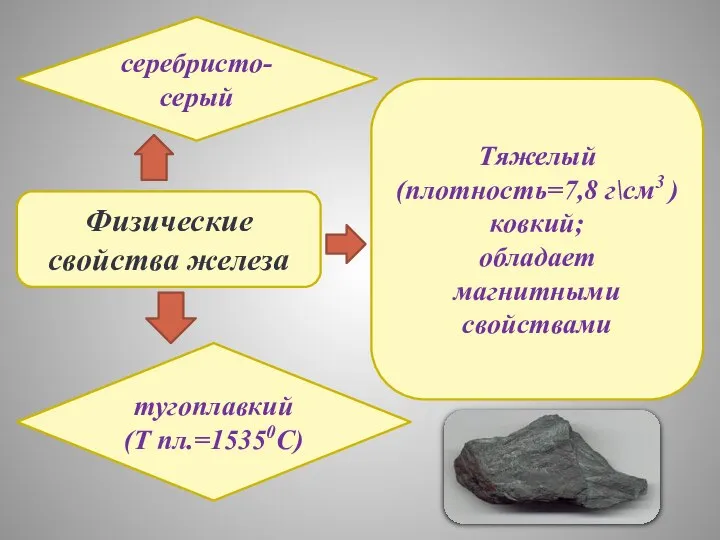
- 5. Физические свойства железа серебристо-серый тугоплавкий (Т пл.=15350C) Тяжелый (плотность=7,8 г\см3 ) ковкий; обладает магнитными свойствами
- 6. Железо сегодня Гидроэлектро- станции и опоры линий электропередач Трубопроводы для воды, нефти и газа Автомобили ,
- 7. ЖЕЛЕЗО КАК МАТЕРИАЛ ИСКУССТВА
- 8. ЖЕЛЕЗО КАК МАТЕРИАЛ ИСКУССТВА
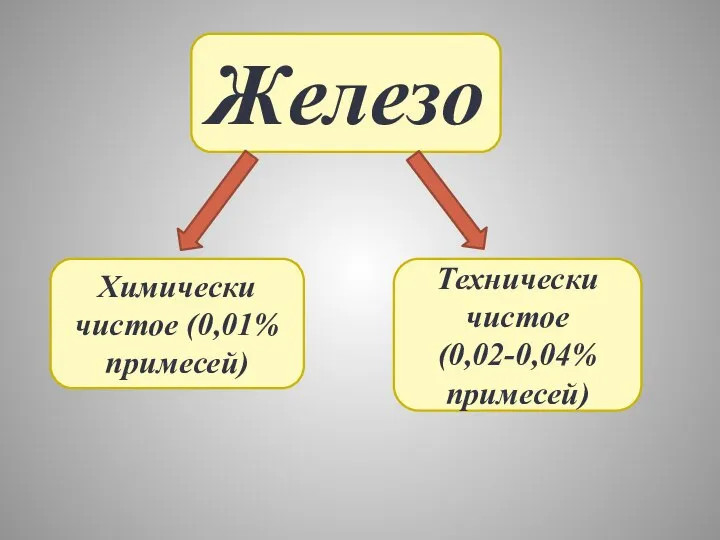
- 10. Железо Химически чистое (0,01% примесей) Технически чистое (0,02-0,04% примесей)
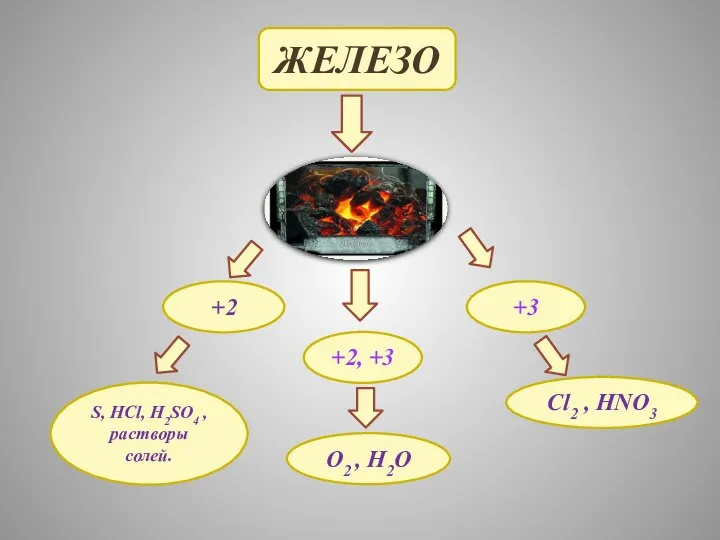
- 11. ЖЕЛЕЗО +2 +3 S, HCl, H2SO4 , растворы солей. O2 , H2O +2, +3 Cl2 ,
- 12. Химические свойства Реакции с простыми веществами Железо сгорает в чистом кислороде при нагревании:3Fe +2O2=Fe3O4 Реагирует с
- 13. Химические свойства Реакции со сложными веществами С кислотами: А) с соляной кислотой 2HCl + Fe =
- 14. Железо разрушается под действием окружающей среды, т.е. подвергается коррозии – «ржавлению». При этом на поверхности образуется
- 15. ЖЕЛЕЗО В ОРГАНИЗМЕ Железо в виде ионов присутствует в организмах всех животных и, конечно же, человека.
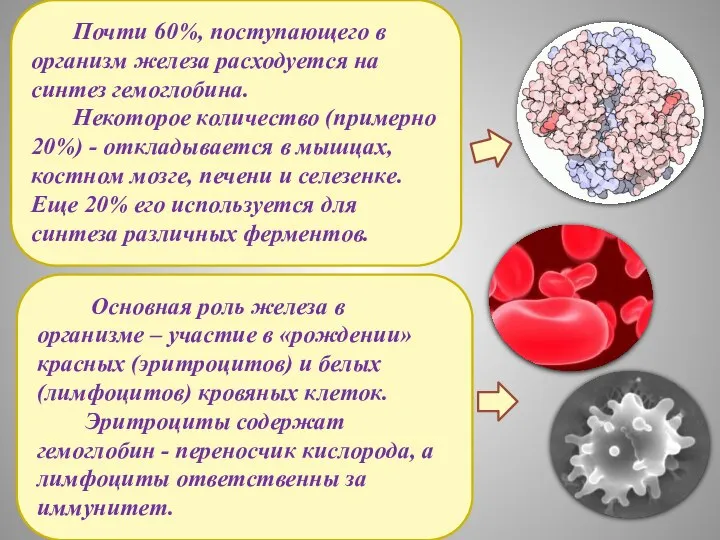
- 16. Основная роль железа в организме – участие в «рождении» красных (эритроцитов) и белых (лимфоцитов) кровяных клеток.
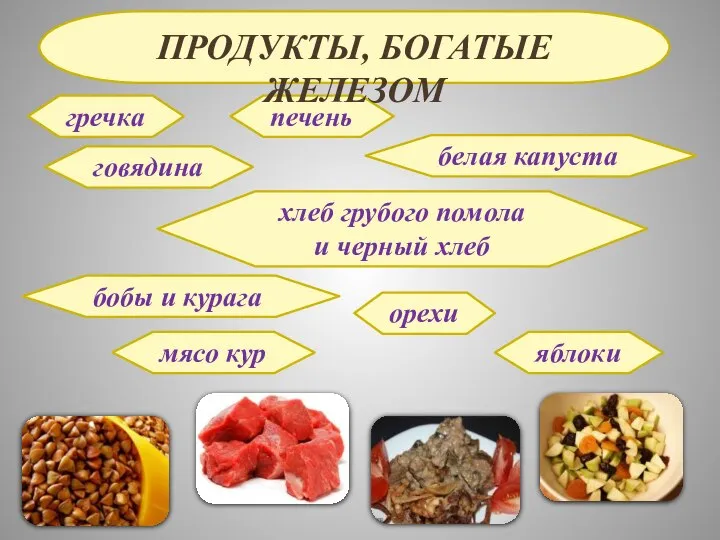
- 17. гречка говядина печень белая капуста хлеб грубого помола и черный хлеб бобы и курага орехи мясо
- 18. При анемии, для приготовления пищи, рекомендуется использовать чугунную посуду. Как показали эксперименты, приготовление и кипячение соуса
- 20. Скачать презентацию












 Коррозия металлов. Экзаменационные вопросы
Коррозия металлов. Экзаменационные вопросы Chemsheets AS 1009 (Electron arrangement)
Chemsheets AS 1009 (Electron arrangement) Обобщение по теме Теория химического строения органических веществ
Обобщение по теме Теория химического строения органических веществ Классификация процессов коррозии
Классификация процессов коррозии Обобщение и систематизация знаний по теме Углеводороды
Обобщение и систематизация знаний по теме Углеводороды Презентация на тему Галогены и здоровье человека
Презентация на тему Галогены и здоровье человека  Производство аммиака
Производство аммиака Хімія у вирішенні промислової проблеми
Хімія у вирішенні промислової проблеми Презентация на тему Металлы и неметаллы
Презентация на тему Металлы и неметаллы  Презентация на тему Мыло. Синтетические моющие средства
Презентация на тему Мыло. Синтетические моющие средства  Презентация на тему Палладий
Презентация на тему Палладий  Классификация НПВС (по химической структуре активности)
Классификация НПВС (по химической структуре активности) Растворы. Процесс растворения (1)
Растворы. Процесс растворения (1) Формирование универсальных учебных действий
Формирование универсальных учебных действий Строение атома
Строение атома ЛК 2_окислительно-восстановительные процессы
ЛК 2_окислительно-восстановительные процессы Презентация на тему Основные законы химии
Презентация на тему Основные законы химии  Предельные углеводороды Алканы
Предельные углеводороды Алканы Железо в продуктах питания
Железо в продуктах питания Презентация на тему: Чистые вещества и смеси
Презентация на тему: Чистые вещества и смеси Оксиды азота
Оксиды азота Органические вещества
Органические вещества Презентация на тему Альдегиды (10 класс)
Презентация на тему Альдегиды (10 класс)  Получение формальдегида методом дегидрирования метанола
Получение формальдегида методом дегидрирования метанола Окислительновосстановительные индикаторы. Задача 12 Команда: Мастера Беспорядка
Окислительновосстановительные индикаторы. Задача 12 Команда: Мастера Беспорядка Реакции этерификации
Реакции этерификации Проточные реакторы непрерывного действия. (Лекция 5)
Проточные реакторы непрерывного действия. (Лекция 5) Разминка
Разминка