Содержание
- 2. Общая характеристика металлов 27.09.2022
- 3. Количество металлов среди всех химических элементов
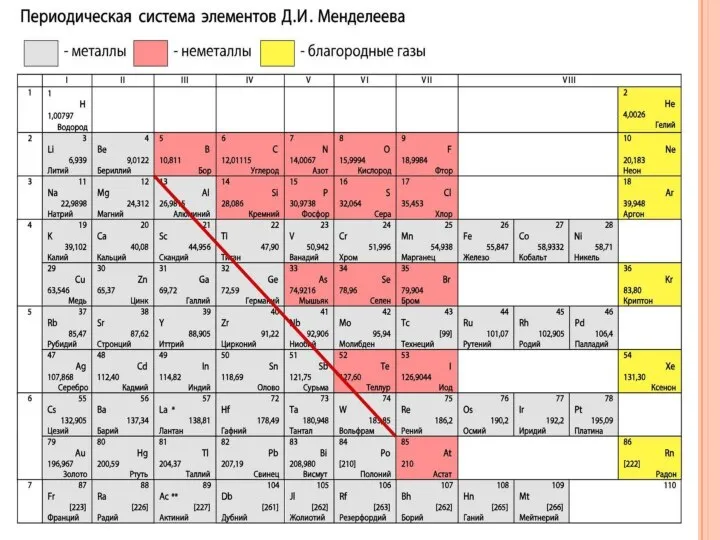
- 4. Расположение элементов – металлов в ПСХЭ: 1 группа главная подгруппа – щелочные металлы 2 группа главная
- 6. Большая часть металлов существует в природе в виде минеральных образований - руд Некоторые неактивные металлы существуют
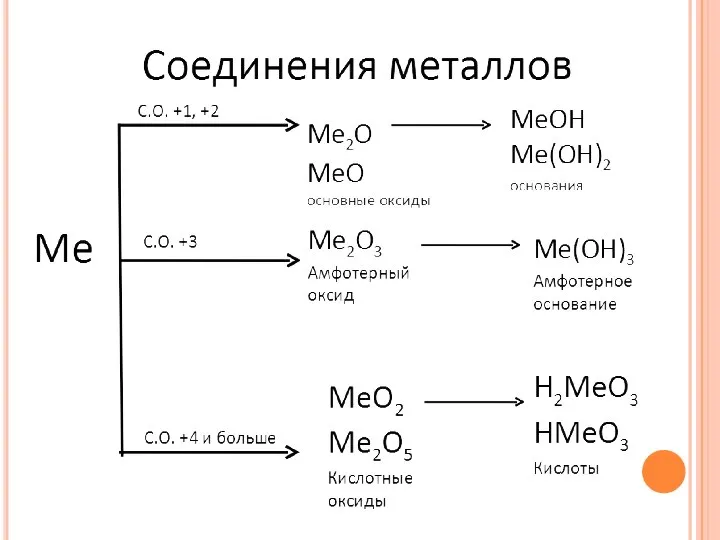
- 8. Металлы – это химические элементы, атомы которых отдают электроны внешнего ( предвнешнего) электронного слоя, превращаясь в
- 9. Главные особенности элементов металлов. Число валентных электронов (1-3 ). Сравнительно большие радиусы атомов. Небольшие значения электроотрицательности
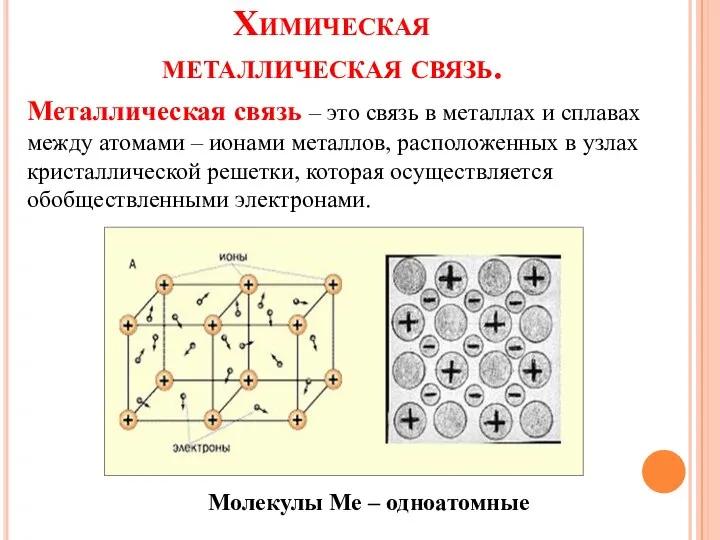
- 12. Химическая металлическая связь. Металлическая связь – это связь в металлах и сплавах между атомами – ионами
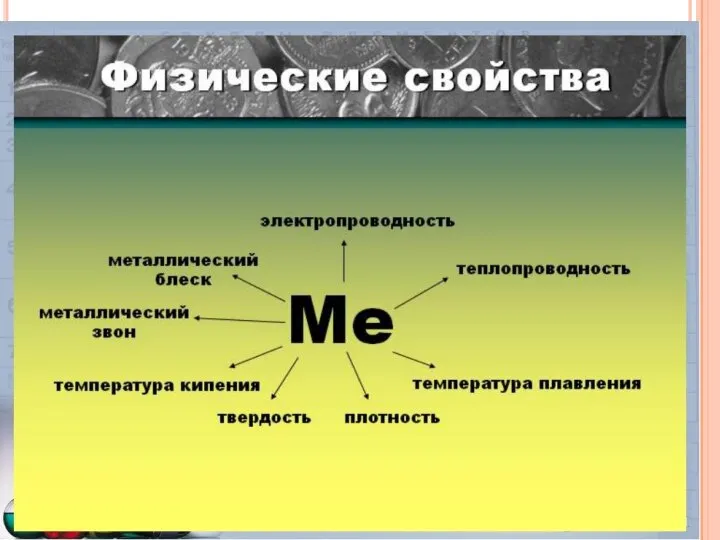
- 13. Металлы – простые вещества. Все металлы обладают общими физическими свойствами: Пластичность – смещение слоев ионов под
- 14. Металлы – простые вещества. Все металлы обладают общими физическими свойствами: Металлический блеск – наличие свободных электронов.
- 15. Металлы – простые вещества. Все металлы обладают общими физическими свойствами: Электро- и теплопроводность – обусловлена нахождением
- 16. Металлы – простые вещества. Все металлы обладают общими физическими свойствами: Твердость –свойство материала сопротивляться внедрению более
- 17. Металлы – простые вещества. Все металлы обладают общими физическими свойствами: Твердость –свойство материала сопротивляться внедрению более
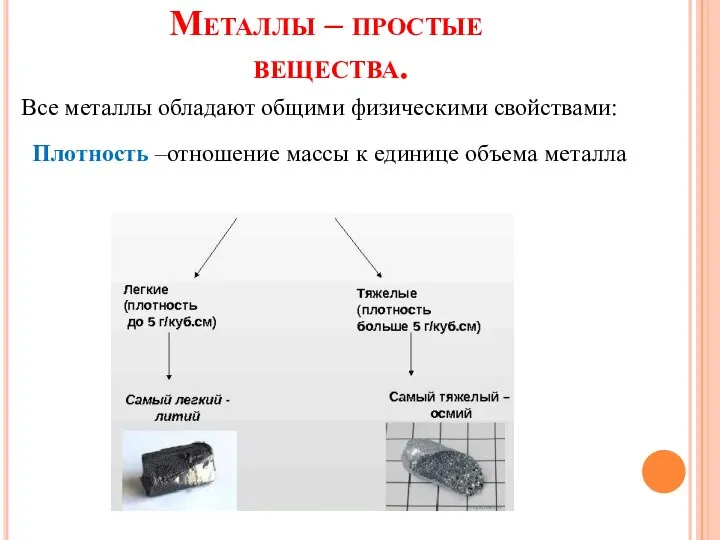
- 18. Металлы – простые вещества. Все металлы обладают общими физическими свойствами: Плотность –отношение массы к единице объема
- 19. Металлы – простые вещества. Все металлы обладают общими физическими свойствами: Цвет металла
- 20. Металлы – простые вещества. Все металлы обладают общими физическими свойствами: Температура плавления
- 22. Домашнее задание 1. Выучить записи в тетради 2. Дать характеристику металлов
- 23. Взаимодействие металлов с галогенами o +2 -1 2Са + Н 2О → 2Сa(ОН) o +3 -1
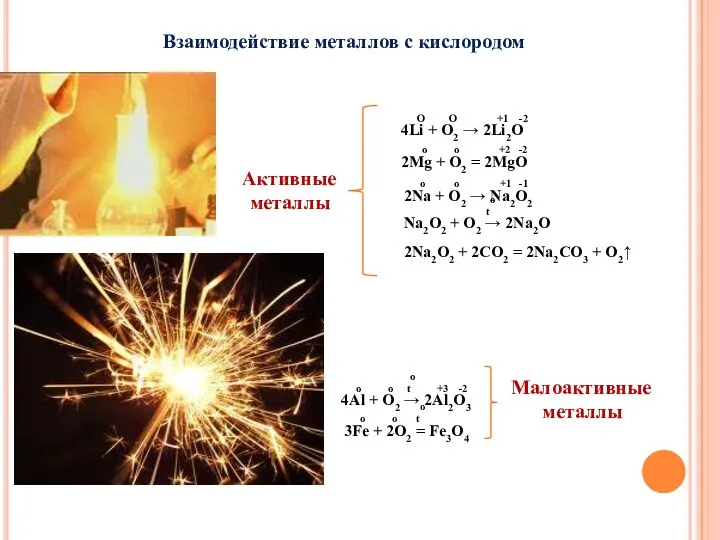
- 24. Взаимодействие металлов с кислородом Активные металлы O O +1 -2 4Li + O2 → 2Li2O o
- 25. o +1 -1 +2 -1 o Zn + 2HCl → ZnCl2 + H2 Взаимодействие металлов с
- 26. Химические свойства металлов 1. Все металлы проявляют только восстановительные свойства 2. Атомы металлов легко отдают электроны
- 27. Применение металлов
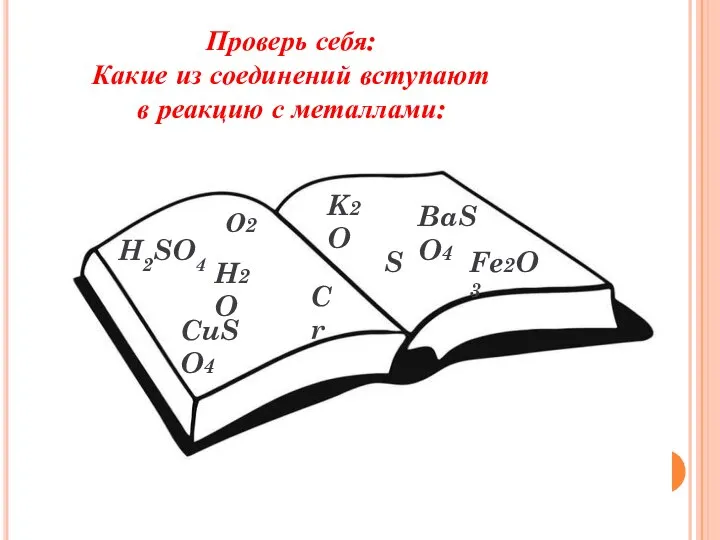
- 28. Проверь себя: Какие из соединений вступают в реакцию с металлами: О2 K2O CuSO4 H2O S BaSO4
- 30. Скачать презентацию




















 1_
1_ Планарные потенциометрические сенсоры на основе пилларарена -DNS-162
Планарные потенциометрические сенсоры на основе пилларарена -DNS-162 Ископаемые углеводороды
Ископаемые углеводороды Презентация на тему Сложные эфиры
Презентация на тему Сложные эфиры  Водород
Водород Кремний Полупроводники в электронике_Горб
Кремний Полупроводники в электронике_Горб Влияние пластифицирующих добавок на свойства декоративного мелкозернистого бетона
Влияние пластифицирующих добавок на свойства декоративного мелкозернистого бетона Переработка нефти
Переработка нефти Металлы. Контрольная работа
Металлы. Контрольная работа Электролитическая диссоциация
Электролитическая диссоциация Исследование физико-химических свойств щавелевой кислоты
Исследование физико-химических свойств щавелевой кислоты Природные источники углеводородов
Природные источники углеводородов Наблюдения в сходящемся свете. Коноскопия
Наблюдения в сходящемся свете. Коноскопия Презентация на тему Биополимеры
Презентация на тему Биополимеры  Разбор заданий
Разбор заданий Турнир знатоков химии
Турнир знатоков химии Неделя химии в МБОУ (викторина)
Неделя химии в МБОУ (викторина) Ліпіди і їх роль в життєдіяльності клітини
Ліпіди і їх роль в життєдіяльності клітини Ароматические углеводороды (арены)
Ароматические углеводороды (арены) Презентация на тему Классификация химических реакций
Презентация на тему Классификация химических реакций  Гидролиз. Виды гидролиза
Гидролиз. Виды гидролиза Применение хидких кристалов в промышленности
Применение хидких кристалов в промышленности Плотность вещества
Плотность вещества Соли в свете теории электролитической диссоциации
Соли в свете теории электролитической диссоциации Физические свойства металлов
Физические свойства металлов Водневий та металічний звязок
Водневий та металічний звязок Основания
Основания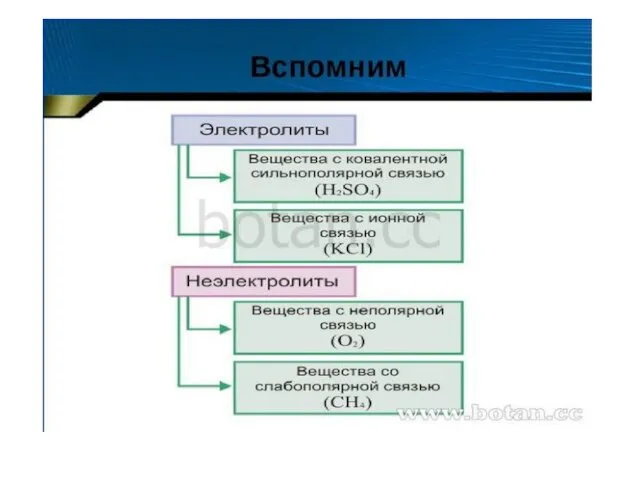 Диссоциация веществ
Диссоциация веществ