Содержание
- 2. Характеристики химической связи: 1. Длина химической связи (ℓсв) – это межъядерное расстояние в молекулах или кристаллах.
- 3. Ковалентная связь Ковалентная связь определяется силой электростатического притяжения двух соседних ядер к локализованной паре электронов, расположенной
- 4. Ковалентная связь бывает: 1. Неполярная 2. Полярная Ковалентная неполярная связь Если двухатомная молекула состоит из атомов
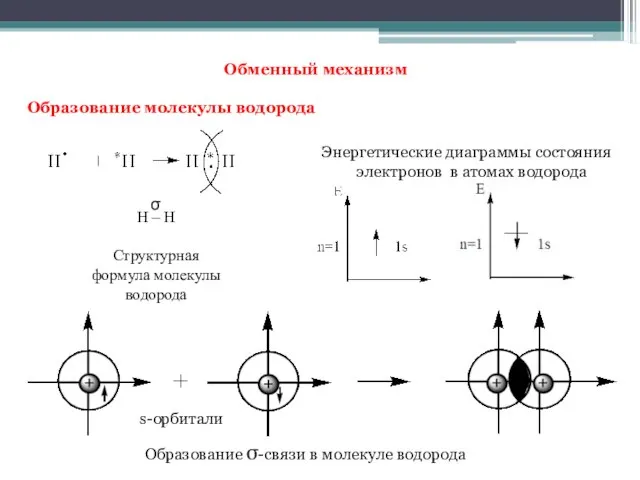
- 5. Обменный механизм Образование молекулы водорода s-орбитали Энергетические диаграммы состояния электронов в атомах водорода Образование σ-связи в
- 6. Образование химической связи между атомами водорода является результатом взаимопроникновения («перекрывания») электронных облаков, происходящего при сближении взаимодействующих
- 7. Энергетические диаграммы состояния электронов в атомах кислорода Образование молекулы кислорода
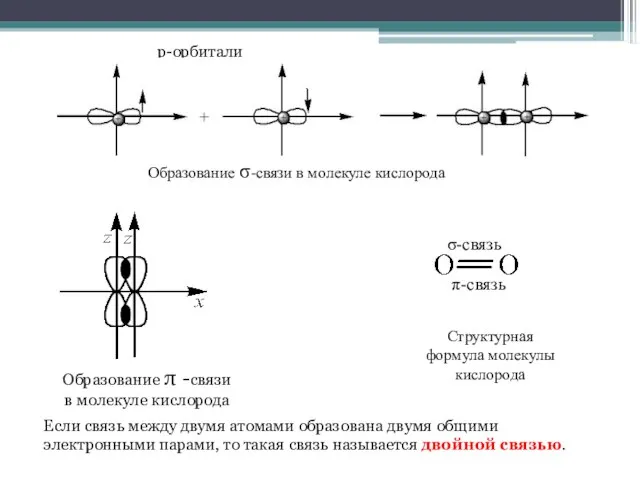
- 8. Образование σ-связи в молекуле кислорода Образование π -связи в молекуле кислорода π-связь σ-связь Структурная формула молекулы
- 9. Ковалентная полярная связь Если двухатомная молекула состоит из атомов различных элементов, то общее электронное облако смещено
- 10. Если молекула состоит из двух атомов, которые связаны полярной связью, то такая молекула является полярной молекулой,
- 11. Донорно-акцепторный механизм образования ковалентной связи донор акцептор Схема образования ковалентной связи по донорно-акцепторному механизму При образовании
- 12. Образование иона аммония Строение внешнего электронного слоя атома азота Донорно-акцепторный механизм образования иона аммония 1s0 Электронная
- 13. Атом бора в основном состоянии Атом бора в возбужденном состоянии Электронная конфигурация атома бора в основном
- 14. Зная строение атома бора, можем сказать, что бор в возбужденном состоянии имеет 3 неспаренных электрона, которые
- 15. Гибридизация атомных орбиталей бора
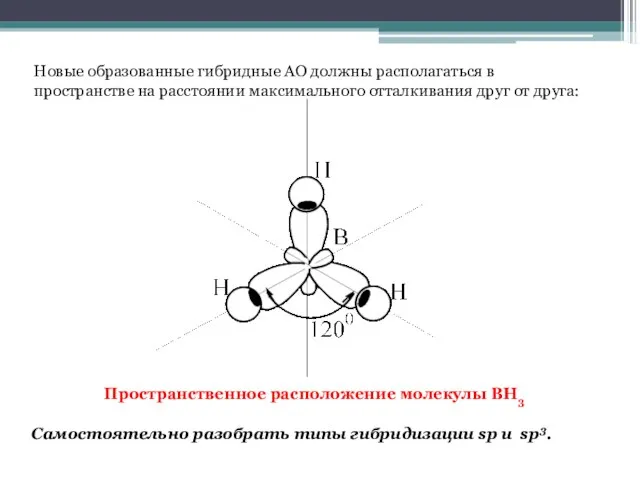
- 16. Пространственное расположение молекулы ВН3 Новые образованные гибридные АО должны располагаться в пространстве на расстоянии максимального отталкивания
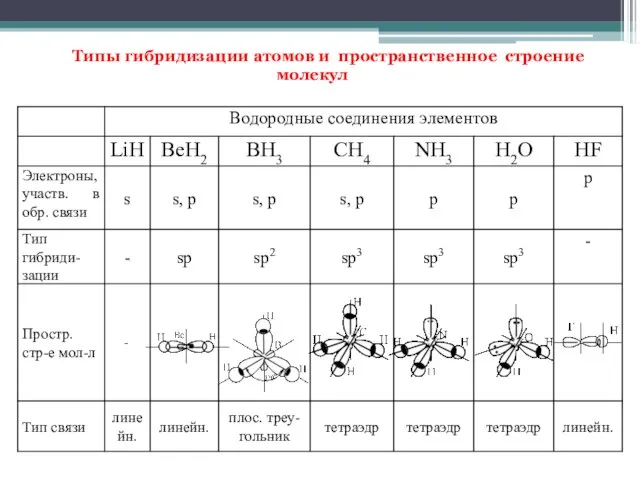
- 17. Типы гибридизации атомов и пространственное строение молекул
- 18. Пространственное строение молекул различного типа
- 19. Свойства ковалентной связи: Насыщаемость – способность атомов участвовать в образовании ограниченного числа ковалентных связей. Направленность –
- 20. Ионная связь Большой вклад в изучение ионной связи внес Коссель. Если связь образуется между атомами, которые
- 21. По свойствам ионная связь отличается от ковалентной связи. Силы электростатического взаимодействия направлены от данного иона во
- 22. Металлическая связь Металлическая связь – это электростатическая сила притяжения двух соседних ядер к делокализованным электронам, находящимся
- 23. Свойства металлов: 1. Электропроводность – в металлической решетке существует большое количество делокализованных электронов. Если к металлу
- 24. Водородная связь Водородная связь носит промежуточный характер между ковалентным и межмолекулярным взаимодействием. Она осуществляется между положительно
- 25. H+δ-F-δ, H+δ-O-δ, H+δ-N-δ Распределение зарядов между атомами H+δ-F-δ∙∙∙ H+δ-F-δ∙∙∙ H+δ-F-δ Водородные связи В образовании водородной связи
- 26. Силы Ван-дер-Ваальса Очень слабые силы притяжения между нейтральными атомами или молекулами, проявляющиеся на расстояниях, превосходящих размеры
- 27. Энергия всех трех слагаемых связана с дипольным взаимодействием различного происхождения: 1. Ориентационное взаимодействие (диполь-дипольное взаимодействие) возникает
- 29. Скачать презентацию






















 Графен. Нобелевская премия 2016
Графен. Нобелевская премия 2016 Основы теории сплавов. Типы сплавов (твердые растворы, сплавы-смеси, сплавы- химические соединения. Диаграммы
Основы теории сплавов. Типы сплавов (твердые растворы, сплавы-смеси, сплавы- химические соединения. Диаграммы Реакции ионного обмена
Реакции ионного обмена Презентация на тему Интересные факты из жизни великого учёного Д. И. Менделеева
Презентация на тему Интересные факты из жизни великого учёного Д. И. Менделеева  Основы материаловедения. Раздел 1
Основы материаловедения. Раздел 1 Электронная структура атома углерода. Лекция 3
Электронная структура атома углерода. Лекция 3 Типы химических реакций
Типы химических реакций Полимеры с включением атомов бора и карборановой группировки - полиборорганосилоксаны и поликарборанорганосилосксаны
Полимеры с включением атомов бора и карборановой группировки - полиборорганосилоксаны и поликарборанорганосилосксаны Гидролиз солей
Гидролиз солей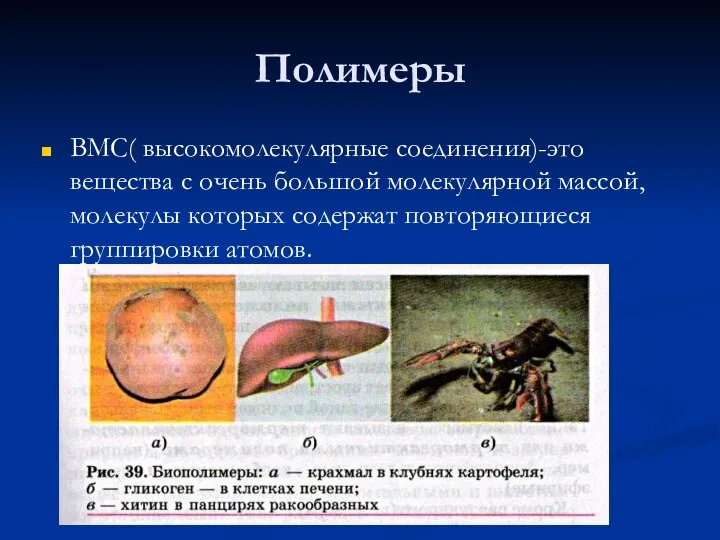 Полимеры
Полимеры Concise asymmetric total synthesis of lycopodine
Concise asymmetric total synthesis of lycopodine Основания. Равновесия в растворах
Основания. Равновесия в растворах Строение атома. Химическая связь
Строение атома. Химическая связь Демокрит его вклад в развитие взглядов на строение вещества
Демокрит его вклад в развитие взглядов на строение вещества Порох. Сера, халькогены
Порох. Сера, халькогены Сравнение активностей металлов
Сравнение активностей металлов Скорость химических реакций
Скорость химических реакций Химия в жизни общества
Химия в жизни общества Органическая химия
Органическая химия Возможности окрашивания поверхности стекла путем высокотемпературной ионообменной обработки с выбранными реагентами
Возможности окрашивания поверхности стекла путем высокотемпературной ионообменной обработки с выбранными реагентами Серная кислота и для чего используется
Серная кислота и для чего используется Превращения в нашей жизни: физические и химические
Превращения в нашей жизни: физические и химические Школа юных ученых. Соль
Школа юных ученых. Соль Соли
Соли Строение углеводородов
Строение углеводородов Электродные процессы. Электроды. Потенциометрия
Электродные процессы. Электроды. Потенциометрия Презентация на тему Интересные факты из жизни Д. И. Менделеева
Презентация на тему Интересные факты из жизни Д. И. Менделеева  Нефть и её переработка
Нефть и её переработка