Слайд 2Методы окислительно-восстановительного титрования
Окислительно-восстановительное титрование
– использует реакции, протекающие с изменением степени окисления реагирующих

веществ.
Слайд 3Классификация методов Red-Ox-метрии и способы титрования
Окислительно-восстановительное титрование или редоксиметрия (от латинского oxydatio

– окисление и reductio – восстановление) основано на реакциях окисления-восстановления. Если титрант – окислитель, то титрование называют окислительным (оксидиметрия). Если титрант – восстановитель, то титрование восстановительное (редуктометрия)
Слайд 5Схемы основных реакций, используемых в Red-Ox-метрии

Слайд 6Каждую окислительно-восстановительную реакцию можно представить как сумму двух полуреакций. Одна реакция отражает

превращение окислителя, а вторая – восстановителя:
Ox1+ ne– = Red1
Red2 – ne– = Ox2
Молярная масса эквивалента окислителя или восстановителя в реакции зависит от числа принятых или отданных одной молекулой окислителя (восстановителя) электронов. Молярная масса эквивалента окислителя (восстановителя) равна произведению фактора эквивалентности данного вещества на его молярную массу:
Слайд 7M (fэкв (В)В) = fэкв (В) М (В),
где M (fэкв (В)В) – молярная масса эквивалента

вещества В
М (В) – молярная масса вещества В
fэкв (В) – фактор эквивалентности вещества.
fэкв (В) = 1/n,
n – число электронов, принятых или отданных одной молекулой окислителя (восстановителя) в данной реакции.
Слайд 8Требования к реакциям в Red-Ox-метрии
К реакциям, применяемым в окислительно-восстановительном титровании, предъявляются следующие требования:
а)

Реакции должны протекать до конца, являться необратимыми, не сопровождаться побочными процессами.
б) В ходе реакции должны образовываться продукты определенного известного состава.
в) Реакции должны протекать быстро.
г) Должна быть возможность фиксировать точку эквивалентности.
Слайд 9К недостатком окислительно-восстановительных реакций в большинстве случаев относится их невысокая скорость, что

затрудняет процесс титрования.
Для ускорения реакций применяют нагревание. Если нагревание использовать нельзя (вещество разлагается или улетучивается), то увеличивают концентрацию вещества или используют катализаторы.
Слайд 10Редокс-титрование может быть выполнено различными способами: прямое титрование, обратное титрование и заместительное

титрование.
Окислительно-восстановительные индикаторы
Для определения точки эквивалентности в Red-Ox-метрии используют различные индикаторы:
1) Окислительно-восстановительные индикаторы (редокс-индикаторы), изменяющие цвет при изменении окислительно-восстановительного потенциала системы.
Слайд 112) Специфические индикаторы, изменяющие свой цвет при появлении избытка титранта или исчезновении

определяемого вещества. Специфические индикаторы применяют в некоторых случаях.
Так крахмал – индикатор на присутствие свободного йода, вернее трииодид-ионов I–3. В присутствии I–3 крахмал при комнатной температуре синеет.
Слайд 12Редокс-индикаторы делятся на: обратимые и необратимые.
Обратимые индикаторы – обратимо изменяют свой цвет

при изменении потенциала системы. Необратимые индикаторы – подвергаются необратимому окислению или восстановлению, в результате чего цвет индикатора изменяется необратимо.
Редокс-индикаторы существуют в двух формах окисленной (Indoкисл) и восстановленной (Indвосст.), причем цвет одной формы отличается от цвета другой.
Слайд 13Перманганатометрия
В сильнокислой среде перманганат-ионы обладают высоким окислительно-восстановительным потенциалом, восстанавливаясь при этом до

Mn(II).
Поэтому перманганат калия применяют для определения многих восстановителей.
Окисление восстановителей можно проводить в различных средах.
Перманганат калия в кислой среде восстанавливается до ионов Mn2+, в нейтральной – до марганца(IV) или диоксида марганца MnO2, в щелочной среде – до марганца(VI) или манганата калия K2MnO4.
Слайд 14В методе перманганатометрии титрование чаще проводят в кислой среде:
MnO4– + 8H+ + 5e– → Mn2+ +

4H2O
E0 = 1,51 B; M(1/5 KMnO4) = 31,608 г/моль
Поскольку в данной полуреакции участвуют 5 электронов, то фактор эквивалентности перманганат-иона равен 1/z=1/5.
Слайд 15Реже используют титрование в нейтральной среде:
MnO4– + 2H2O + 3e– → MnO2 + 4OH–
E0 = 0,60

B; M (1/3 KMnO4) = 52,68 г/моль
Перманганат-ион восстанавливается до диоксида марганца MnO2 . Фактор эквивалентности MnO4– равен 1/z=1/3.
При титровании перманганатом не применяют индикаторы, так как титрант сам окрашен и является чувствительным индикатором: 0,1 мл 0,01 М раствора KMnO4 окрашивает 100 мл воды в бледно-розовый цвет.
Слайд 16В то время как при титровании в кислой среде образуются бесцветные ионы

Mn2+, в щелочной или нейтральной среде выпадает темно-бурый осадок, затрудняющий фиксирование точки эквивалентности по окраске небольшого избытка перманганата.
В качестве рабочего раствора в методе перманганатометрии применяют 0,02 н – 0,05 н растворы KMnO4.
Использование перманганата калия дает возможность фиксировать точку эквивалентности без применения индикатора, т. к. добавление лишь одной капли избытка стандартного раствора KMnO4 окрашивает титруемый раствор в розовый цвет.
Слайд 17Рабочий раствор KMnO4 нельзя готовить путем взятия точной навески и растворения ее

в определенном объеме воды. Обычно берут приблизительную навеску KMnO4 и приготовленный раствор стандартизируют.
Для стандартизации раствора перманганата калия применяют H2C2O4 · 2H2O, (NH4)2C2O4 · H2O, Na2C2O4, As2O3, K4[Fe(CN)6], металлическое железо и некоторые другие вещества. Наиболее удобны как установочные вещества щавелевая кислота и ее соли, т. к. они могут быть легко очищены от примесей перекристаллизацией из водных растворов.
Слайд 18Методом перманганатометрии можно определять:
Восстановители (методом прямого титрования): низкозарядные ионы, способные давать соединения

высших степеней окисления (Fe2+, Sn2+, Ti3++, Cr2+ и др.);
отрицательно заряженные ионы неметаллов (S2-, I-, Br-); комплексные анионы-восстановители (SCN - , CN -, SO3 2-, S2O32-, NO2-, C2O42- и др.).
Окислители (методом обратного титрования):NO3- , C2O82-, Cr2O72-, MnO2,PbO2 и др.
Вещества, не обладающие окислительно-восстановительными свойствами (методом косвенного титрования) : Ca2+-, Bi3+-, Zn2+-ионы и др.
Слайд 20Приготовление 0,1 н. (0,05 н.) раствора перманганата калия
Титрованный раствор перманганата калия по

точной навеске кристаллического KMnO4 приготовить нельзя, так как в нем всегда содержится некоторое количество MnO2 и других продуктов разложения. Поэтому раствор перманганата калия относится к вторичным стандартным растворам. Первоначально готовят раствор KMnO4, концентрация которого приблизительно равна необходимой концентрации.
Слайд 21Навеску берут на технохимических весах несколько больше расчетной величины. Так как KMnO4 является

сильным окислителем и изменяет свою концентрацию в присутствии различных восстановителей, то приготовленный раствор перманганата калия выдерживают 7–10 дней в темном месте для того, чтобы прошли все окислительно-восстановительные процессы с примесями, содержащимися в воде. Затем раствор фильтруют.
Только после этого концентрация раствора становится постоянной и его можно стандартизировать по щавелевой кислоте или по оксалату аммония.
Слайд 22Растворы KMnO4 следует хранить в бутылях из темного стекла. Приготовленный таким способом раствор

перманганата калия с молярной концентрацией эквивалента 0,05 моль/л и выше не изменяет свой титр довольно продолжительное время.
Слайд 23Стандартизация раствора перманганата калия по щавелевой кислоте или оксалату аммония (натрия)
Способ определения основан

на окислении щавелевой кислоты перманганат-ионами в кислой среде:
5H2C2O4 + 2KMnO4 + 3H2SO4 → 2MnSO4 + 10CO2 + K2SO4 + 8H2O
При этом полуреакции окисления и восстановления имеют вид:
H2C2O4 – 2e– = 2CO2 + 2H+
MnO2– + 8H+ + 5e– = Mn2+ + 4H2O
Тогда fэкв (H2C2O4) = 1/2; fэкв (KMnO4) = 1/5
Слайд 24При комнатной температуре эта реакция протекает медленно. И даже при повышенной температуре

скорость ее невелика, если она не катализирована ионами марганца(II).
Нагревать кислоту выше 70-80 °С нельзя, так как при этом часть кислоты окисляется кислородом воздуха:
H2C2O4 + O2 → 2CO2 + H2O2
2H2O2 → 2H2O + O2
Слайд 25Реакция взаимодействия перманганата калия со щавелевой кислотой относится к автокаталитическим реакциям. Реакция

окисления щавелевой кислоты протекает в несколько стадий. Первые капли перманганата калия даже в горячем растворе обесцвечиваются очень медленно. Для ее начала необходимо присутствие в растворе хотя бы следов Mn2+:
1. MnO4– + MnC+O4 → MnO42- + MnC2O4+
Слайд 26Образовавшийся манганат-ион MnO42- в кислом растворе быстро диспропорционирует:
2. Mn (VI) + Mn (II)

= 2 Mn (IV)
3. Mn (IV) + Mn(II) = 2Mn (III)
Марганец (III) образует оксалатные комплексы состава [Mn(C2O4) n] (3-2n)+, где n = 1,2,3; эти комплексы медленно разлагаются с образованием Mn2+ и CO2
Слайд 27Таким образом, пока в растворе не накопится в достаточных концентрациях марганец (II),

реакция между MnO4– и С2O42- протекает медленно. Когда концентрация марганца(II) достигает определенной величины, реакция начинает протекать с большой скоростью.
Интенсивная окраска раствора перманганата калия осложняет измерение объемов титранта в бюретке. На практике удобно за уровень отсчета принимать поверхность жидкости, а не нижнюю часть мениска.
Слайд 28Для установки концентрации (титра или молярной концентрации эквивалентов) стандартного раствора перманганата калия

рассчитывают навеску щавелевой кислоты H2С2O4 · 2H2O или оксалата аммония (NH4)2C2O4, необходимую для приготовления раствора с молярной концентрацией эквивалента 0,1 моль/л (или 0,05 н.). Рассчитанное количество кислоты (или соли) взвешивают на аналитических весах.
Взвешенную массу кислоты (или соли) растворяют в воде в мерной колбе, раствор тщательно перемешивают. Затем титруют раствор KMnO4.
Слайд 29Расчет концентрации перманганата калия во всех случаях проводят на основании закона эквивалентов:
N

(1/2 H2C2O4) = n (1/5 KMnO4)
Тогда C (1/2 H2C2O4 · 2H2O) · V (H2C2O4 · 2H2O) = C (1/5 KMnO4) · V (KMnO4)
Поскольку ион MnO–4 является сильным окислителем (особенно в кислой среде), то метод перманганатометрии применяется для определения различных восстановителей таких как: H2O2, Fe2+, NO–2, некоторых органических веществ.




























 Презентация на тему Предельные углеводороды
Презентация на тему Предельные углеводороды  Презентация на тему Полисахариды. Крахмал и целюлоза
Презентация на тему Полисахариды. Крахмал и целюлоза  Получение металлов в промышленности. Чёрная металлургия
Получение металлов в промышленности. Чёрная металлургия Строение атома. Строение электронных оболочек атомов
Строение атома. Строение электронных оболочек атомов Презентация на тему Металлы тоже воевали
Презентация на тему Металлы тоже воевали  8-11 2 валентность
8-11 2 валентность Химическая связь и строение вещества
Химическая связь и строение вещества Решение задач на смеси, растворы и сплавы
Решение задач на смеси, растворы и сплавы Теория электролитической диссоциации
Теория электролитической диссоциации Пространственная изомерия органических соединений
Пространственная изомерия органических соединений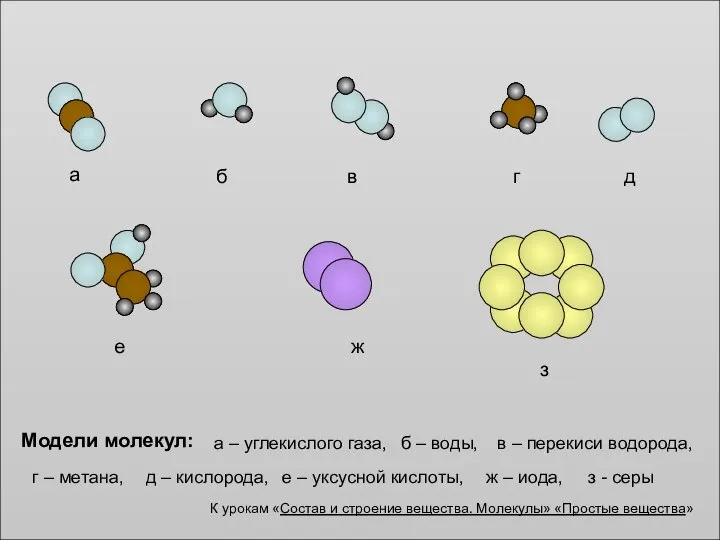 Модели молекул
Модели молекул Вода
Вода Применение обратимых и необратимых реакций в быту
Применение обратимых и необратимых реакций в быту Спирты. Классификация спиртов
Спирты. Классификация спиртов Коррозия металлов
Коррозия металлов Химический тренажер
Химический тренажер Кислород и сера
Кислород и сера Презентация на тему Зеленая химия и проблемы устойчивого развития
Презентация на тему Зеленая химия и проблемы устойчивого развития  Химическое вещество золото
Химическое вещество золото Фосфор туралы
Фосфор туралы Кислородные соединения углерода
Кислородные соединения углерода Химическая термодинамика. Термодинамические потенциалы
Химическая термодинамика. Термодинамические потенциалы Классификация реакций. Теория-кинетика
Классификация реакций. Теория-кинетика Алканы
Алканы Неметаллы. 8 класс
Неметаллы. 8 класс Изготовление слайма в домашних условиях
Изготовление слайма в домашних условиях Кислота
Кислота Тест по химии
Тест по химии