Содержание
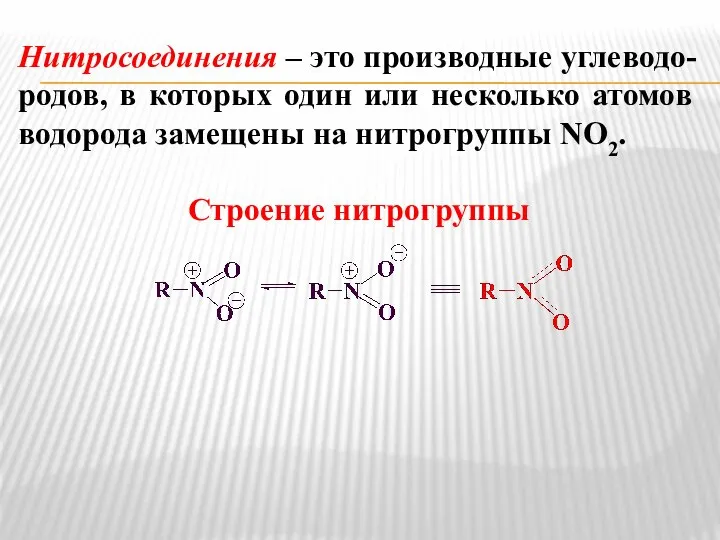
- 2. Нитросоединения – это производные углеводо-родов, в которых один или несколько атомов водорода замещены на нитрогруппы NO2.
- 3. Способы получения нитросоединений Нитрование алканов Нитрование аренов Взаимодействие галогеналканов с нитритами (нуклеофильное замещение) Окисление первичных аминов
- 4. Первичные и вторичные нитросоединения являются СН-кислотами и в растворах щелочей образуют соли – нитронаты, которые при
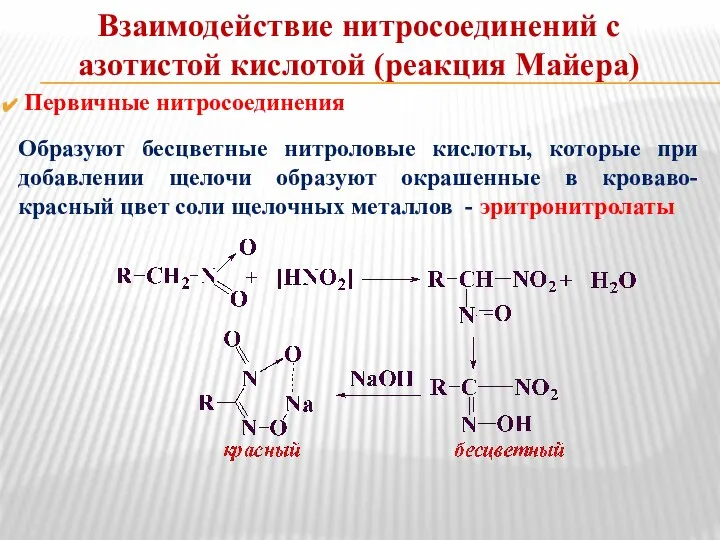
- 5. Первичные нитросоединения Образуют бесцветные нитроловые кислоты, которые при добавлении щелочи образуют окрашенные в кроваво-красный цвет соли
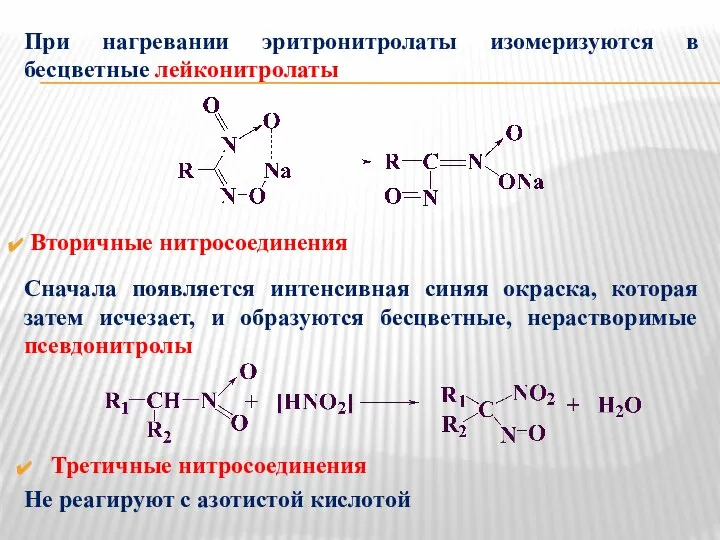
- 6. При нагревании эритронитролаты изомеризуются в бесцветные лейконитролаты Вторичные нитросоединения Сначала появляется интенсивная синяя окраска, которая затем
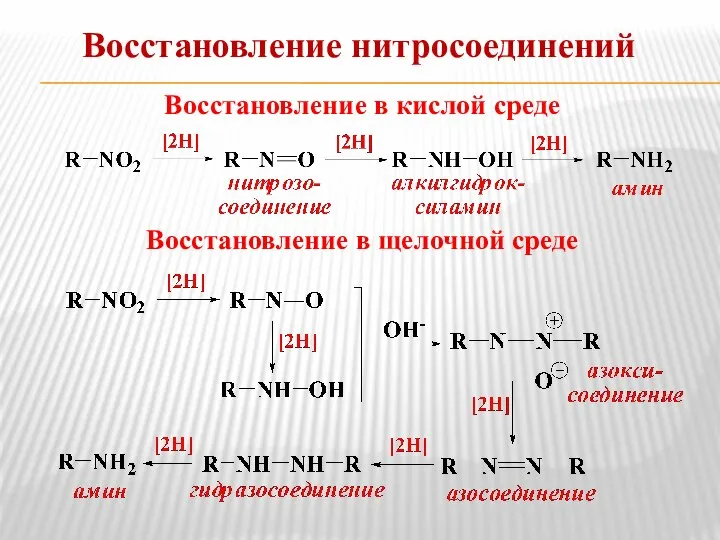
- 7. Восстановление в кислой среде Восстановление в щелочной среде Восстановление нитросоединений
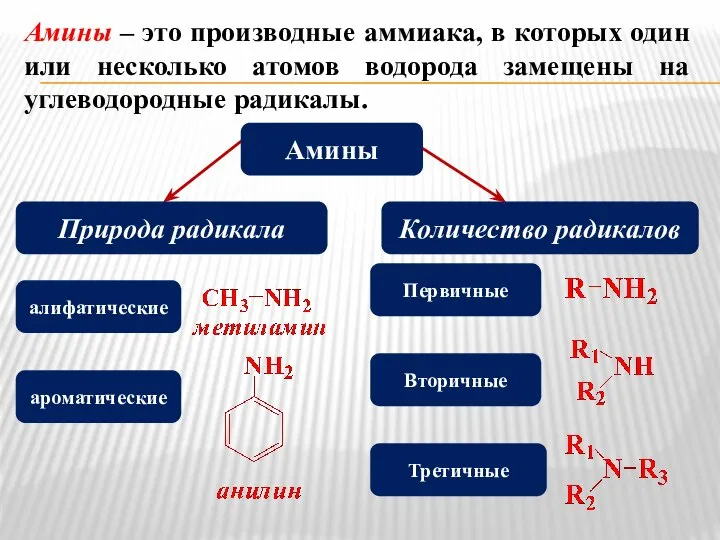
- 8. Амины – это производные аммиака, в которых один или несколько атомов водорода замещены на углеводородные радикалы.
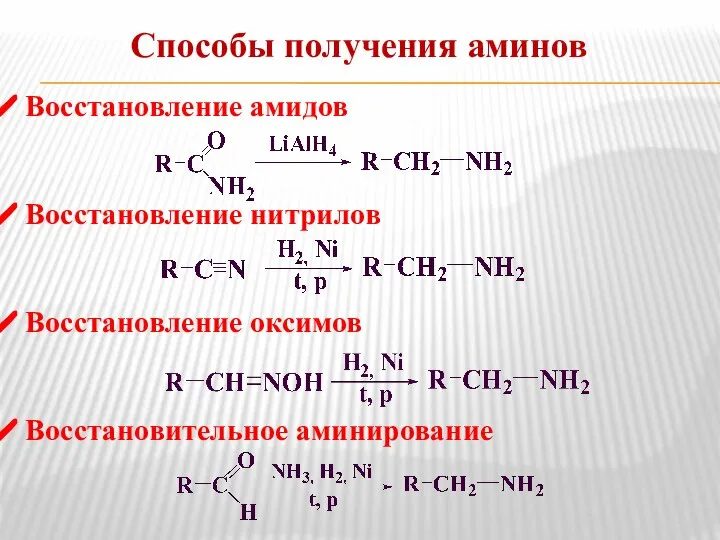
- 9. Способы получения аминов Восстановление амидов Восстановление нитрилов Восстановление оксимов Восстановительное аминирование
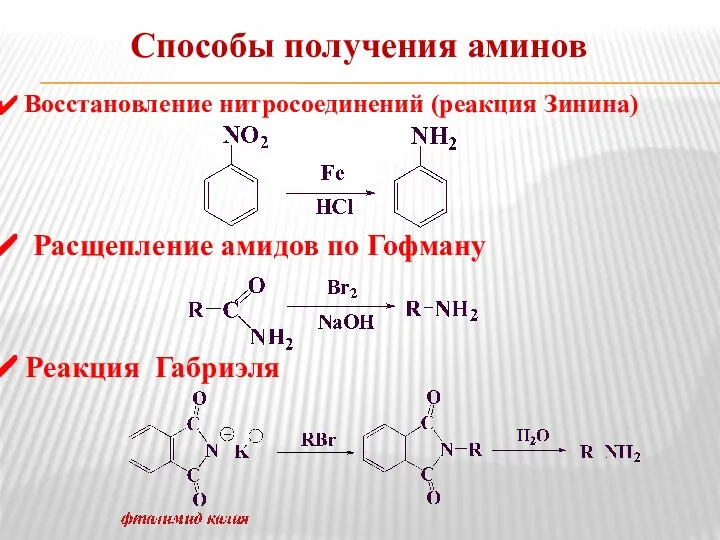
- 10. Способы получения аминов Восстановление нитросоединений (реакция Зинина) Расщепление амидов по Гофману Реакция Габриэля
- 11. Способы получения аминов Алкилирование аммиака
- 12. Реакционные центры в аминах NН-кислотный центр n-Основный и нуклеофильный центры
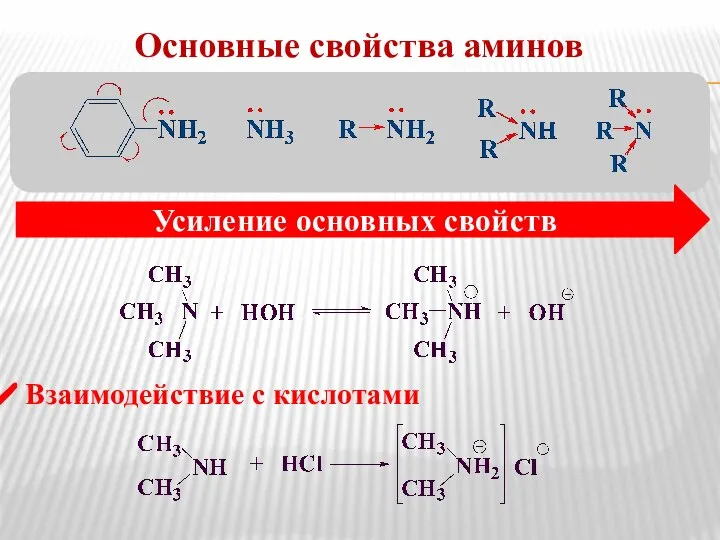
- 13. Основные свойства аминов Взаимодействие с кислотами Усиление основных свойств
- 14. Нуклеофильные свойства аминов Взаимодействие с алкилгалогенидами Взаимодействие с хлорангидридами Взаимодействие с карбонильными соединениями Взаимодействие с эпоксидами
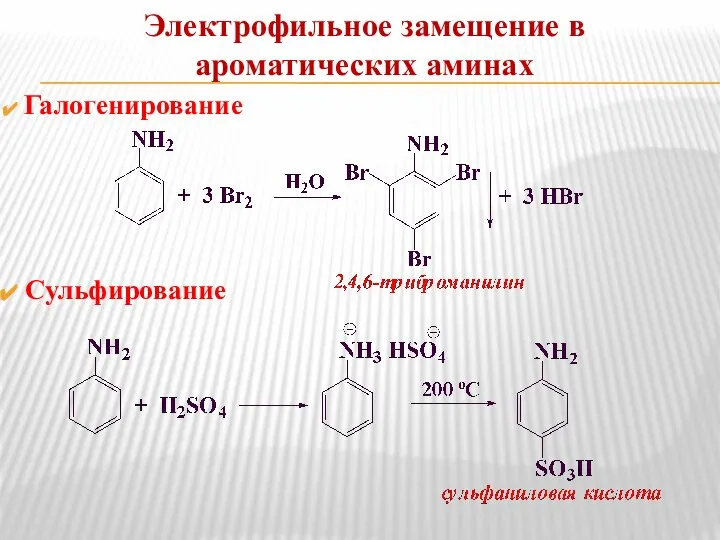
- 15. Электрофильное замещение в ароматических аминах Галогенирование Сульфирование
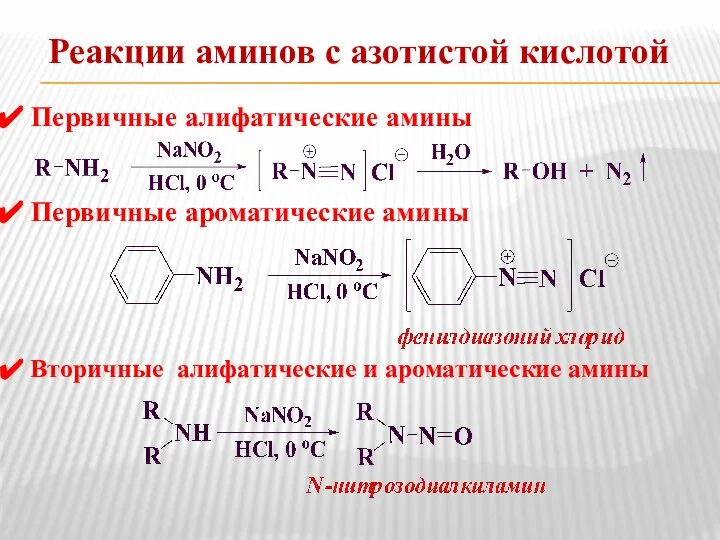
- 16. Реакции аминов с азотистой кислотой Первичные алифатические амины Первичные ароматические амины Вторичные алифатические и ароматические амины
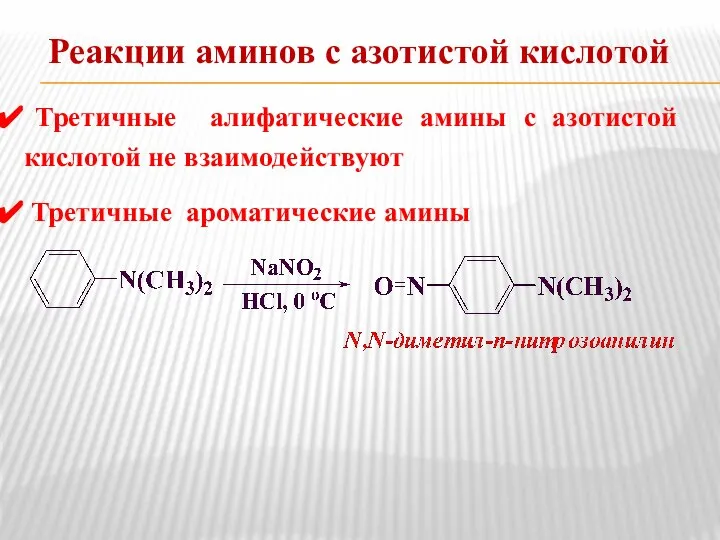
- 17. Реакции аминов с азотистой кислотой Третичные алифатические амины с азотистой кислотой не взаимодействуют Третичные ароматические амины
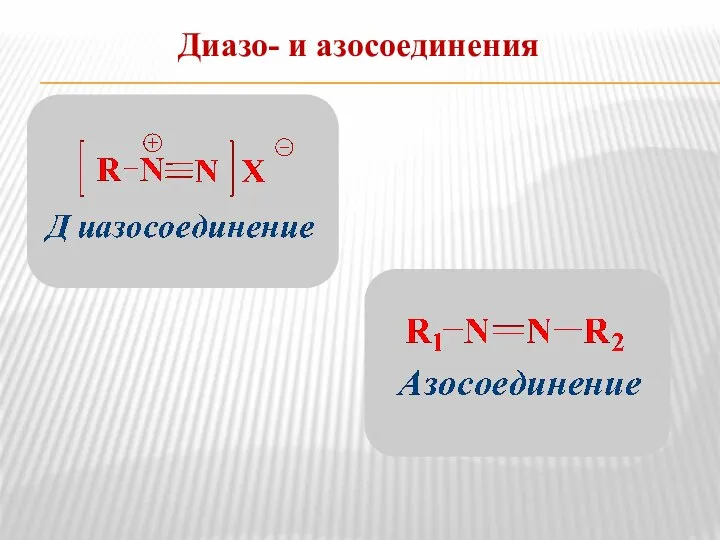
- 18. Диазо- и азосоединения
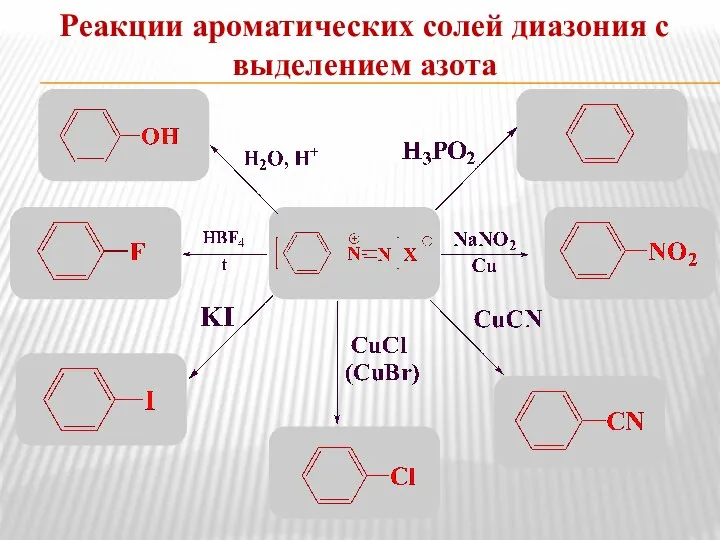
- 19. Реакции ароматических солей диазония с выделением азота
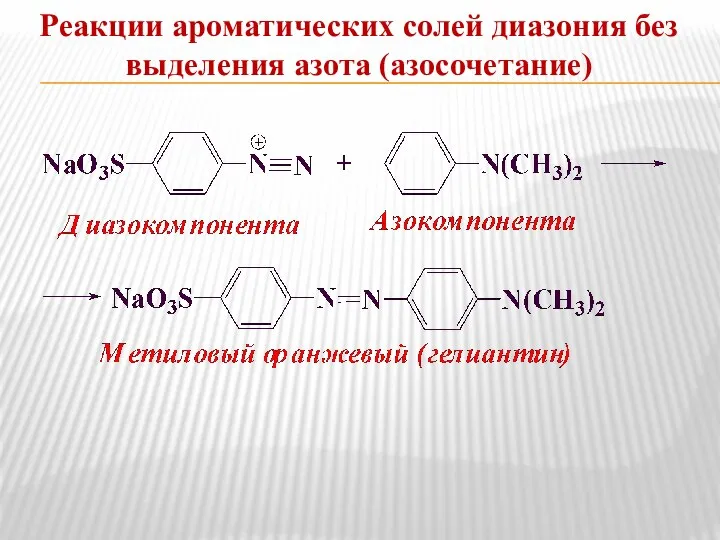
- 20. Реакции ароматических солей диазония без выделения азота (азосочетание)
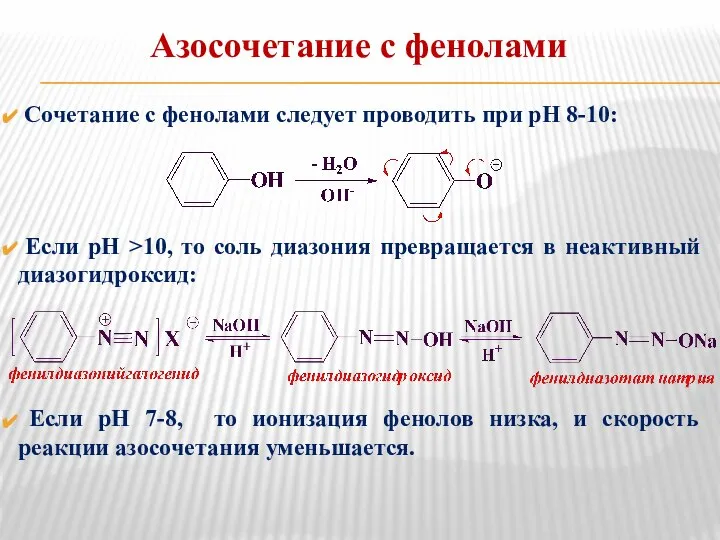
- 21. Сочетание с фенолами следует проводить при рН 8-10: Если рН >10, то соль диазония превращается в
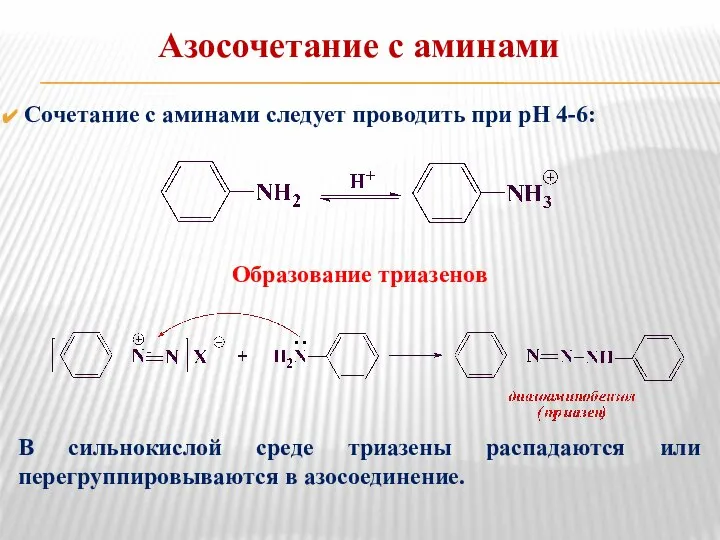
- 22. Азосочетание с аминами Сочетание с аминами следует проводить при рН 4-6: Образование триазенов В сильнокислой среде
- 24. Скачать презентацию





 Электролиз. Правила электролиза
Электролиз. Правила электролиза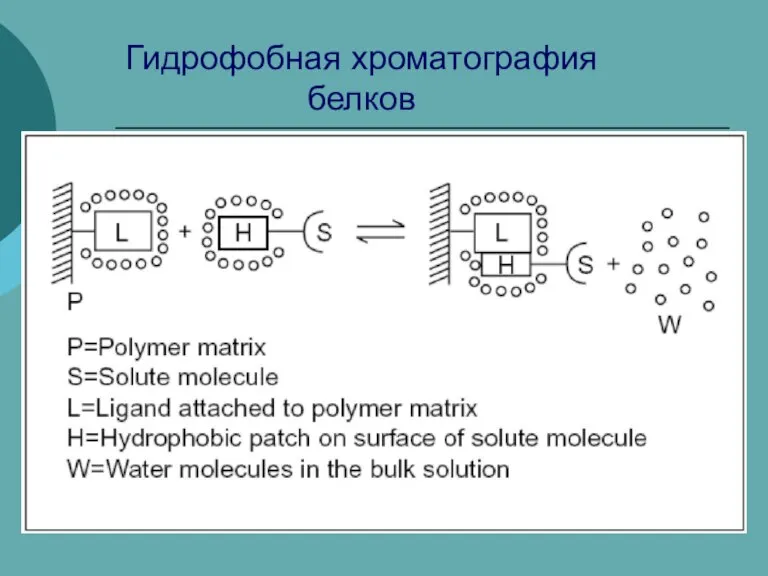 Гидрофобная хроматография белков
Гидрофобная хроматография белков 7609f31d31514fe19b6df19a98197139 (1)
7609f31d31514fe19b6df19a98197139 (1) Бикомпонентные покрытия
Бикомпонентные покрытия Сера и ее соединения
Сера и ее соединения Презентация на тему Строение атома Химическая связь
Презентация на тему Строение атома Химическая связь  Взаимодействие плазмы с поверхностью. Проблемы термоядерного реактора
Взаимодействие плазмы с поверхностью. Проблемы термоядерного реактора Определение времени прохождения диффузии
Определение времени прохождения диффузии Презентация на тему Сплавы металлов
Презентация на тему Сплавы металлов  Химия. Спирты
Химия. Спирты Углерод и его аллотропные модификации. Органическая химия - химия углерода
Углерод и его аллотропные модификации. Органическая химия - химия углерода Газообразные (газ)
Газообразные (газ) Химические свойства алкенов. Получение
Химические свойства алкенов. Получение Хлорорганические соединения
Хлорорганические соединения Химические элементы
Химические элементы Соли: получение
Соли: получение Азотная кислота
Азотная кислота Белки-1 2020
Белки-1 2020 Основания (Ме+n(ОН)-n)
Основания (Ме+n(ОН)-n) Расчётно-графическая работа по теме Мыловарение
Расчётно-графическая работа по теме Мыловарение Альдегиды. Получение и применение
Альдегиды. Получение и применение Презентация на тему Изотопы
Презентация на тему Изотопы  Типы химических реакций
Типы химических реакций Растительные жиры. Пальмовое масло
Растительные жиры. Пальмовое масло Химия в быту
Химия в быту Кристаллическое строение металлов и сплавов. Аморфные и кристаллические тела
Кристаллическое строение металлов и сплавов. Аморфные и кристаллические тела Алкены. Ҳимические свойства алкенов
Алкены. Ҳимические свойства алкенов Порядок в жидкостях
Порядок в жидкостях